гипергаммаглобулинемия что это такое
Newmed
лечение в Израиле
Почему пациенты из стран СНГ
выбирают «НьюМед Центр»?
Лечение гипергаммаглобулинемии в Израиле
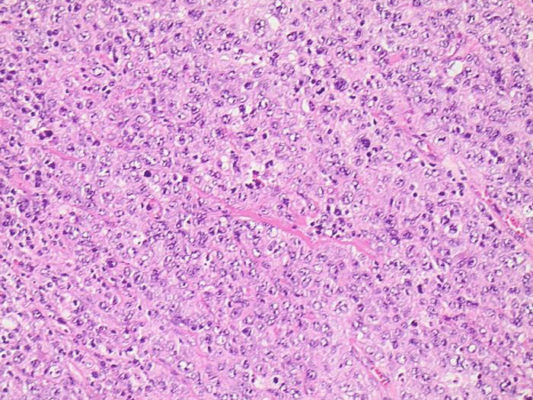
Инновационные методы обследования гипергаммаглобулинемии в Израиле
Компания NewMed Center предлагает пациентам оптимальную лечебно-диагностическую программу, реализация которой обеспечит выявление причины патологического состояния и его устранение. По отзывам о лечении гипергаммаглобулинемии в Израиле, ценой и уровнем услуг пациенты остаются довольны.
Первый шаг в диагностических мероприятиях – это оценка специалистом анамнеза и клинической картины, в которой выделяются специфические признаки заболевания. Геморрагический диатез проявляется петихиальными высыпаниями на теле, спонтанными кротечениями из носа и кровоподтеками на деснах. Развивается он на фоне нормального уровня тромбоцитов в крови.
Ключевые пункты плана и составляющая часть стоимости диагностики гипергаммаглобулинемии в больницах – лабораторные проверки. Прежде всего, назначается общее и биохимическое исследование крови, которое дает возможность определить уровень гамма-глобулина. Для оценки гемостаза и свертываемости крови проводится гемостазиограмма и аутокоагулограмма.
Значимая проверка среди обследований – протеинограмма. Исследование позволяет определить процентное соотношение фракций белка в сыворотке крови. В частности, оценивается фракция гамма-глобулинов (IgG, IgA, IgM, IgE).
Новейшие методы лечения гипергаммаглобулинемии в Израиле
Специалисты клиник в лечении гипергаммаглобулинемии ставят перед собой задачу нормализировать текущее состояние пациента, и устранить факторы, которые являются потенциальной угрозой рецидива в дальнейшем. Зачастую речь идет о лечении патологического состояния, которое является первопричиной гипергаммаглобулинемии.
В основе лечебных программ – экстракорпоральная очистка крови посредством плазмафореза. Проведение процедуры обеспечивает общую детоксикацию организма и устранение отклонений в гомеостазе. Плазмафорез представляет собой механическое удалении части плазмы из крови пациента с последующим ее очищением и возвращением в кровоток. Подобным способом удаляются содержащиеся в плазме компоненты, которые вызвали заболевание, в частности – избыточные иммуноглобулины.
В израильских медцентрах используются высокотехнологичные методики плазмафореза – каскадная и гравитационная. Инновационные плазмафильтры и центрифуги обеспечивают высокую эффективность процедуры. Квалификация специалистов и контроль стерильности в помещениях гарантирует полную безопасность.
Ответы докторов на вопросы пациентов
Среди таких заболеваний можно выделить патологии печени (циррозы, хронические гепатиты), аутоиммунные процессы (ревматоидный артрит, красная волчанка), онкологические поражения (саркоидоз, остеосаркомы, хронический лимфолейкоз), а также туберкулез и ишемическая болезнь сердца.
Каскадный плазмафорез – это разновидность фильтрационной методики. Обе эти техники экстракорпоральной очистки крови предусматривают использование специальных полупроницаемых фильтров, которые задерживают определенные патогенные компоненты.
Заручитесь поддержкой экспертов по организации лечения в Израиле – специалистов NewMed Center!
ГИПЕРГАММАГЛОБУЛИНЕМИЯ
гипергаммаглобулинемия (hypergammaglobulinaemia; гипер- + гаммаглобулинемия) — повышенное содержание в крови иммуноглобулинов; наблюдается вследствие интенсивной иммунизации, введения некоторых адъювантов или в связи с заболеванием.
гипергаммаглобулинемия дискретная (h. discreta) — см. Гипергаммаглобулинемия моноклональная.
гипергаммаглобулинемия диффузная (h. diffusa) — см. Гипергаммаглобулинемия поликлональная.
гипергаммаглобулинемия моноклональная (h. monoclonalis; греч. monos один + klon росток, побег, ветвь; син.: гаммапатия моноклональная, Г. дискретная) — Г., характеризующаяся повышенным синтезом одного из классов иммуноглобулинов (чаще IgM) или одного из фрагментов иммуноглобулинов (легких и тяжелых цепей, Fc-фрагментов и т. д.); наблюдается чаще при злокачественной пролиферации какого-либо клона B-лимфоцитов.
гипергаммаглобулинемия поликлональная (h. polyclonalis; греч. poly- много + klon росток, побег, ветвь; син.: гаммапатия поликлональная, Г. диффузная) — Г., характеризующаяся увеличением синтеза нескольких или всех классов иммуноглобулинов; наблюдается при хронических инфекциях, аутоиммунных процессах, коллагеновых болезнях и т. д.
Смотреть что такое ГИПЕРГАММАГЛОБУЛИНЕМИЯ в других словарях:
ГИПЕРГАММАГЛОБУЛИНЕМИЯ
(hypergammaglobulinaemia; Гипер- + гаммаглобулинемия)повышенное содержание в крови иммуноглобулинов; наблюдается вследствие интенсивной иммунизации, вв. смотреть
ГИПЕРГАММАГЛОБУЛИНЕМИЯ
ГИПЕРГАММАГЛОБУЛИНЕМИЯ
(hypergammaglobulinaemia; гипер- + гаммаглобулинемия) повышенное содержание в крови иммуноглобулинов; наблюдается вследствие интенсивной иммунизации, введения некоторых адъювантов или в связи с заболеванием. смотреть
Агаммаглобулинемия – это наследственно обусловленное заболевание, при котором развивается тяжелый первичный иммунодефицит (дефект иммунной защиты организма) с выраженным снижением уровня гамма-глобулинов в крови. Проявляется болезнь обычно в первые месяцы и годы жизни ребенка, когда начинают развиваться повторные бактериальные инфекции: отит, синусит, пневмонии, пиодермии, менингит, сепсис. При обследовании в периферической крови и костном мозге практически отсутствуют сывороточные иммуноглобулины и B-клетки. Лечение агаммаглобулинемии заключается в пожизненной заместительной терапии.
МКБ-10
Общие сведения
Агаммаглобулинемия (наследственная гипогаммаглобулинемия, болезнь Брутона) – врожденный дефект гуморального иммунитета, обусловленный мутациями в геноме клеток, что приводит к недостаточности синтеза B-лимфоцитов. В результате нарушается образование иммуноглобулинов всех классов, и их содержание в крови резко снижается вплоть до полного отсутствия, развивается первичный иммунодефицит. Низкая реактивность иммунной системы приводит к развитию тяжелых повторных гнойно-воспалительных заболеваний ЛОР-органов, бронхов и легких, желудочно-кишечного тракта и мозговых оболочек. Болезнь Брутона встречается исключительно у мальчиков и наблюдается примерно у 1-5 человек из миллиона новорожденных, независимо от расы и этнической группы.
Причины
X-сцепленная форма наследственной агаммаглобулинемии возникает вследствие повреждения одного из генов X-хромосомы (расположен на Xq21.3-22.2). Этот ген ответственен за синтез фермента тирозинкиназы, участвующего в процессе образования и дифференцировки B-клеток. В результате мутаций этого гена и блокировки синтеза брутоновской тирозинкиназы нарушается формирование гуморального иммунитета. При агаммаглобулинемии молодые формы (пре-B-клетки) присутствуют в костном мозге, а их дальнейшая дифференцировка и поступление в кровеносное русло нарушена.
Классификация
Выделяют три формы наследственной агаммаглобулинемии:
Симптомы агаммаглобулинемии
Сниженная реактивность гуморального иммунитета при агаммаглобулинемиях приводит к развитию повторных гнойно-воспалительных заболеваний уже на первом году жизни ребенка (как правило, после прекращения грудного вскармливания – в 6-8 месяцев). При этом защитные антитела от матери в организм ребенка уже не поступают, а свои иммуноглобулины – не вырабатываются. К 3-4 летнему возрасту воспалительные процессы переходят в хроническую форму со склонностью к генерализации. Гнойная инфекция при агаммаглобулинемии может поражать различные органы и системы.
Со стороны ЛОР-органов нередки гнойные гаймориты, этмоидиты, отиты, причем гнойный отит чаще развивается на первом году жизни ребенка, а синуситы – в 3-5 лет. Из заболеваний бронхолегочной системы наблюдаются повторные бронхиты, пневмонии, абсцессы легкого. Часто встречается поражение желудочно-кишечного тракта с упорной диареей (поносами), вызванной хроническим инфекционным энтероколитом (основные возбудители – кампилобактерии, лямблии, ротавирус). На кожных покровах обнаруживается импетиго, микробная экзема, рецидивирующий фурункулез, абсцессы и флегмоны.
Нередким бывает поражение глаз (гнойные конъюнктивиты), полости рта (язвенные стоматиты, гингивиты), костно-мышечной системы (остеомиелиты, гнойные артриты). В целом клиническая картина агаммаглобулинемии характеризуется сочетанием общих симптомов, наблюдаемых при гнойной инфекции (высокая температура тела, озноб, боли в мышцах и головная боль, общая слабость, нарушение сна и аппетита и т. д.) и признаков поражения конкретного органа (кашель, одышка, затруднение носового дыхания, гнойное отделяемое, диарея и т. п.).
Осложнения
Любое инфекционное и соматическое заболевание у больного иммунодефицитом протекает тяжело, длительно и сопровождается осложнениями. Тяжелое течение агаммоглобулинемии может осложняться развитием менингита, вирусного энцефаломиелита, поствакцинального паралитического полиомиелита, сепсиса. На фоне заболевания повышена вероятность развития аутоиммунных и онкологических заболеваний. Гибель пациентов часто наступает от инфекционно-токсического шока.
Диагностика
При клиническом осмотре пациента врачом аллергологом-иммунологом выявляются признаки гнойно-воспалительного поражения того или иного органа (ткани) и симптомы, подтверждающие сниженную реактивность иммунной системы: гипоплазия миндалин, уменьшение периферических лимфатических узлов. Выражены и признаки отставания в физическом развитии ребенка.
Лабораторное исследование крови выявляет выраженное снижение уровня иммуноглобулинов в иммунограмме (IgA и IgM
Дифференциальная диагностика наследственной агаммаглобулинемии проводится с другими первичными и вторичными иммунодефицитными состояниями (генетическими нарушениями, ВИЧ и цитомегаловирусной инфекцией, врожденной краснухой и токсоплазмозом, злокачественными новообразованиями и системными нарушениями, иммунодефицитом вследствие интоксикации лекарственными препаратами и др.).
Лечение агаммаглобулинемии
Необходима пожизненная заместительная терапия антителосодержащими препаратами. Обычно используется введение внутривенного иммуноглобулина, а при его отсутствии – нативной плазмы от здоровых постоянных доноров. При впервые установленном диагнозе агаммаглобулинемии заместительное лечение проводится в режиме насыщения до достижения уровня иммуноглобулина IgG выше 400 мг/дл, после чего при отсутствии активного гнойно-воспалительного процесса в органах и тканях можно переходить к поддерживающей терапии с введением профилактических доз препаратов, содержащих иммуноглобулины.
Любой эпизод бактериальной гнойной инфекции, независимо от локализации воспалительного процесса, требует проведения адекватной антибактериальной терапии, которая выполняется одновременно с заместительным лечением. Чаще при агаммаглобулинемии используются антибактериальные средства из группы цефалоспоринов, аминогликозидов, макролидов, а также антибиотики пенициллинового ряда. Продолжительность лечения при этом в несколько раз превышает стандартную при данном заболевании.
Симптоматическое лечение проводится с учетом конкретного поражения того или иного органа (промывание околоносовых пазух носа антисептиками, выполнение вибрационного массажа грудной клетки и постурального дренажа при бронхитах и пневмониях и т. д.).
Прогноз
Если агаммаглобулинемия обнаружена в раннем возрасте до наступления тяжелых осложнений, и адекватная состоянию пациента заместительная терапия начата своевременно, возможно сохранение нормального образа жизни в течение многих лет. Однако в большинстве случаев диагностика наследственных нарушений гуморального иммунитета осуществляется слишком поздно, когда уже развились необратимые хронические гнойно-воспалительные заболевания органов и систем организма. В этом случае прогноз при агаммаглобулинемии неблагоприятный.
Василенко В.В., Виноградов Д.Л., Бурлакова А.С. IgG4-сопряженная патология: состояние проблемы. Архивъ внутренней медицины. 2017;7(2): 95-106.
IgG4-сопряженная патология: состояние проблемы
В.В. Василенко, Д.Л. Виноградов*, А.С. Бурлакова
Первый МГМУ им. И.М. Сеченова, Москва, Россия
IgG4-related disease: condition of the problem
V. Vasilenko, D. Vinogradov*, A. Burlakova
I.M. Sechenov First Moscow State Medical University, Moscow, Russia
Резюме
Физиологическая роль IgG4 еще не до конца изучена. Известно, что они, как и другие антитела, участвуют в инактивации и удалении из организма веществ, идентифицированных иммунной системой, как чужеродные антигены. Также IgG4 реализуют эффекторные механизмы: связывание со специализированными иммунными клетками, осуществляющими после такого взаимодействия фагоцитоз чужеродных агентов или уничтожение зараженных клеток организма за счет зависимой от антител цитотоксичности. Мнения относительно способности IgG4 активировать комплемент зачастую противоречивы. Повышение концентрации иммуноглобулинов данного подкласса может свидетельствовать не только о развитии инфекционных и аллергических состояний, но и о наличии у пациента IgG4-сопряженной патологии. IgG4-сопряженная патология (IgG4-СП) — относительно недавно выделенная группа патологических состояний, и ее изучение становится все более актуальным. Это связано с тем, что она включает в себя состояния, которые ранее считались самостоятельными нозологическими единицами. В последние годы IgG4-СП диагностируется все чаще, так как получает все большее признание у медицинской общественности. Данный обзор включает новейшую информацию из последних зарубежных публикаций.
Ключевые слова: IgG4-сопряженная патология, IgG4-СП, лимфоплазмоцитарная инфильтрация, фиброз
Для цитирования: В.В. Василенко, Д.Л. Виноградов, А.С. Бурлакова. IGG4-сопряженная патология: состояние проблемы. Архивъ внутренней медицины. 2017;7(2): 95-106. DOI: 10.20514/2226-6704-2017-7-2-95-106
Abstract
The physiological role of IgG4 is poorly understood yet. It is known, that they, like other antibodies, are involved in the inactivation and removal of organism agent, which are identified as foreign antigens by immune system. IgG4 also release effector mechanisms: contact with the specialized immune cells, which perform phagocytosis foreign antigens or destruction of the infected cells by antibody-dependet cytotoxicity, after this interaction. Opinions about the ability to activate complement system are divided. The elevation concentration of that subclass immunoglobulins can be an indicator not only of development of infectious and allergic conditions, but also the presence of the IgG4-related disease in a patient´s organism. IgG4-RD is a recently selected group of pathological conditions and it is becoming relevant to study. It is because they include the conditions, which have been thought to be separate nosology previously. In recent years IgG4-RD has been diagnosed more often, because it has been increasingly being recognized in the medical community. This review includes the latest information from the latest foreign publication.
—
Key words: IgG4-related disease, IgG4-RD, lymphoplasmacytic infiltration, fibrosis
For citation: Vasilenko V., Vinogradov D., Burlakova A. IgG4-related disease: condition of the problem. Archive of internal medicine. 2017; 7(2): 95-106. [In Russian]. DOI: 10.20514/2226-6704-2017-7-2-95-106. DOI: 10.20514/2226-6704-2017-7-2-95-106
IgG4-СП — IgG4-сопряженная патология, Tregs — регуляторные Т-клетки, АИП — аутоиммунный панкреатит, ГН — гломерулонефрит, ИССХ — IgG4-сопряженный склерозирующий холангит, ПСХ — первичный склерозирующий холангит, ТИН — тубулоинтерстициальный нефрит, ЭРХПГ — эндоскопическая ретроградная холангиопанкреатография
*Контакты/Contacts. E-mail: wind007@ mail.ru
Введение
Иммуноглобулины G составляют 75% от общего количества циркулирующих антител, а все остальные классы иммуноглобулинов — суммарно около 25%. IgG продуцируются и накапливаются в организме в больших количествах, чем IgM. Кроме того, они обладают более высоким специфическим сродством к соответствующим детерминантам антигенов и образуют с ними более прочные иммунные комплексы. IgG, как правило, являются основными факторами гуморального звена иммунной защиты, противодействующего развитию инфекционного процесса в организме. Наличие специфических иммуноглобулинов класса G, появившиеся у человека в результате перенесенной болезни или вакцинации, в большинстве случаев свидетельствует о формировании у него иммунитета к соответствующей инфекции.
Иммуноглобулины всех классов имеют одинаковые легкие цепи, но строение тяжелых цепей у них различается. У IgG существует 4 типа тяжелых цепей и, в зависимости от наличия той или иной из них, они подразделяются на 4 подкласса: IgG1, IgG2, IgG3, IgG4.
Относительная концентрация IgG4 в сыворотке крови в норме ниже, чем других подклассов, и составляет всего 4%. Повышение концентрации данного подкласса встречается при различных бактериальных (хламидии, пилорический хеликобактер), вирусных (гепатит В, вирус Эпштейна-Барр) и паразитарных (эхинококкоз, аскаридоз, клонорхоз) инфекциях. Кроме того, количество IgG4 в сыворотке крови повышается при некоторых аллергических состояниях, в частности при атопических экземе и дерматите. Недавно опубликованные результаты исследований свидетельствуют о защитном механизме действии IgG4, препятствующем эффективному связыванию IgE с аллергеном [5].
Повышение концентрации IgG4 обнаруживалось при многих болезнях и синдромах, которые теперь объединены в IgG4 — связанную патологию. Клинические исследования проводятся во многих странах, однако существует еще множество нерешенных вопросов относительно этиологии, патогенеза, диагностики, лечения и прогноза IgG4-СП. В отечественной литературе проблема IgG4-СП неоднократно освещалась во многих публикациях, особенно в работах Седышева С.Х. и соавт. [7, 8], а также в публикации Лысенко Г.И. и соавт. [5]. Клинические случаи данного заболевания подробно описаны в публикациях Гаврилиной Н.С. и соавт. [2], и Винокуровой Л.В. и соавт. [1]. В данном обзоре за основу взята информация из зарубежных публикаций [23, 28].
Предпочтительным названием для подобного состояния является IgG4-сопряженная патология. Однако существует ряд других названий, описывающих суть патологии [32, 42]. Они включают:
• IgG4-связанное заболевание
• IgG4-связанное системное заболевание
• IgG4-синдром
• IgG4-ассоциированное заболевание
• IgG4-связанная склерозирующая болезнь
• IgG4-связанная системная склерозирующая болезнь
• IgG4-связанное аутоиммунное заболевание
• IgG4-позитивный мультиорганный лимфопролиферативный синдром
• Гипер-IgG4 болезнь
• Системный IgG4-связанный плазмоцитарный синдром
• Системный IgG4-связанный склерозирующий синдром
• Мультифокальный фибросклероз
• Мультифокальный идиопатический фибросклероз.
Описание и гистология
Главным критерием IgG4–СП является наличие лимфоплазмоцитарной инфильтрации ткани с преобладанием IgG4–положительных плазматических клеток и CD4+ Т-лимфоцитов, сопровождающейся фиброзом, облитерирующим флебитом и повышением уровня IgG4 в сыворотке крови [13]. У значительной части пациентов, примерно 40% в некоторых группах [57], концентрация IgG4 в сыворотке крови была в норме еще до начала терапии, несмотря на наличие типичных гистопатологических изменений в тканях [16]. Характерно улучшение состояния при проведении терапии глюкокортикоидами, особенно при небольших фиброзных изменениях в тканях [42].
Фиброз, ассоциированный с IgG4-СП, приобретает характерный вид «мраморного» 2 узора, в связи с появлением в ткани упорядоченных фибробластов и воспалительных клеток (рис. 1) [13]. Также в ткани присутствует умеренное количество эозинофилов.
Эпидемиология
IgG4-СП чаще встречается у мужчин пожилого и среднего возраста. Это в первую очередь справедливо для таких расстройств как аутоиммунный панкреатит (АИП), ретроперитонеальный фиброз, IgG4-сопряженный тубулоинтерстициальный нефрит (ТИН). Тем не менее, распределение заболеваемости среди представителей разного пола несколько отличается при патологии органов головы и шеи. К примеру, IgG4-сопряженный сиалоаденит и IgG4-сопряженные псевдоопухоли орбиты в равной степени встречаются как у мужчин, так и у женщин [32,59].
В исследовании 114 пациентов, имеющих IgG4-CП, с ограниченным поражением одной области (голова и шея, торакальная, гепатопанкреатобилиарная и ретроперитонеальная) и с системным поражением (более одной области), было проведено сравнение с учетом демографических и клинических признаков. В каждой группе пациенты были примерно одного возраста, от 59 до 68 лет (диапазон от 42 до 79) [59]. Во всех группах, кроме пациентов с поражением головы и шеи, были преимущественно мужчины (75-86%), но в группах с заболеванием головы и шеи болезнь распределялась практически поровну (48% мужчин).
Несмотря на имеющиеся данные, необходимо дальнейшее изучение эпидемиологии IgG4-СП. Первоначально возникали трудности в исследовании этой патологии из-за отсутствия четких данных, неполной номенклатуры и недостаточной осведомленности клинических специалистов и патологоанатомов о данном заболевании. Эти проблемы постепенно преодолеваются, что должно способствовать получению большего представления об эпидемиологии IgG4-СП.
Хотя IgG4-СП чаще встречается у мужчин, стадии болезни и тяжесть течения практически не различаются у представителей разного пола. В группе 125 пациентов с IgG4-CП, подтвержденной биопсией, число вовлеченных в патологический процесс органов, степень повышения сывороточного IgG4 и общее состояние организма аналогичны как у мужчин, так и у женщин [57].
Патогенез
Патогенез IgG4-СП мало изучен; по некоторым данным это аутоиммунное расстройство с аллергическим компонентом [13, 43]. Было высказано предположение, что IgG4 играют определенную роль в развитии толерантности к аллергенам и ответной реакции на некоторые инфекционные агенты, однако их физиологическое значение до конца не изучено. Аутоиммунность IgG4 не была доказана, и поэтому неясно, являются ли они патогенными [22]. Формирующийся консенсус свидетельствует, что IgG4-антитела не являются патогенными, скорее регулируют ответную реакцию организма на другой первичный процесс(ы) [36].
Признаки, позволившие предположить аутоиммунную природу, обнаруживаются при АИП и связаны со специфическим классом антигенов гистосовместимости II класса [43]. Кроме того, иногда можно выявить антинуклеарные антитела и антитела к лактоферрину и карбоангидразе II. Некоторые исследования показали возможное развитие иммунного ответа на антигены Helicobacter pylori (по механизму молекулярной мимикрии) [60]. Было выявлено отложение иммунных комплексов в поджелудочной железе, почках и некоторых других пораженных тканях [19]. Тем не менее, результаты исследований оказались весьма противоречивыми, и нельзя дать четкого ответа на вопрос о роли аутоиммунных процессов в развитии АИП.
О наличии аллергической реакции свидетельствует повышение уровня цитокинов Th2 в пораженных тканях и повышение IgE в сыворотке крови. Кроме того, как указывалось выше, у многих пациентов с IgG4-СП можно обнаружить аллергический ринит и бронхиальную астму. В периферической крови увеличивается количество регуляторных Т-клеток (Tregs), в пораженных тканях увеличивается уровень цитокинов, производимых Tregs, включая интерлейкин–10 и трансформирующий фактор роста (TGF)–бета. Th2 цитокины, Tregs и ИЛ-10 участвуют в продукции IgG4 [10]. До 40% пациентов с IgG4-СП имеют эозинофилию периферической крови.
Клиническая картина
При IgG4-СП может поражаться один или несколько органов. Чаще встречаются пациенты с развитием очагового образования в пораженном органе (например, псевдоопухоль глазницы, почечная патология, напоминающая почечно-клеточную карциному, узловые образования в легких) или диффузного увеличения органа (например, поджелудочная железа) [32]. Поражение сразу нескольких органов встречается у 60-90% всех пациентов с IgG4-СП [42, 46]. Независимо от органа во всех поврежденных тканях можно обнаружить сходные патологические, серологические и клинические признаки.
Увеличение лимфатических узлов является частым явлением, симптомы астмы и аллергии встречаются примерно в 40% случаев. Зачастую в момент постановки диагноза пациенты чувствуют себя хорошо [13]. Правда, пациенты с полиорганной патологией до постановки верного диагноза в течение нескольких месяцев теряют в массе тела от 20 до 30 фунтов (около 9-14 кг).
Недавно обнаружено, что около 1/3 пациентов имеют различные симптомы сухости глаз и рта, артралгии, повышенную СОЭ, гипергаммаглобулинемию, невысокие титры ревматоидного фактора (РФ) и антинуклеарных антител [8].
Клиницисты также должны быть готовы, что IgG4-CП может имитировать аутоиммунные ревматические болезни, такие как системная красная волчанка, синдром Шегрена, гранулематоз Вегенера [48]. Можно заподозрить диагноз IgG4-СП при обнаружении гистологических признаков или при выявлении изменений на результатах радиологических исследований.
Проявления IgG4-СП
Ранее описывались состояния, которые являются проявлениями IgG4-СП. Номенклатура, если не указано иное, включает [32, 42]:
На данный момент изучается частота встречаемости различных проявлений заболевания и их комбинаций при системном поражении. В качестве примера, при исследовании пациентов с АИП были выявлены поражения других органов, в том числе лимфаденопатия внутригрудных лимфатических узлов (в 80% случаев), поражение внепанкреатических сегментов желчных протоков (74%), слезных и слюнных желез (39%), гипотиреоз (22%), ретроперитонеальный фиб роз (13%) [24]. Однако АИП был обнаружен только у 17% обследованных пациентов с IgG4-СП слезной, околоушной и поднижнечелюстной желез, также в этой группе были выявлены интерстициальный нефрит (17%) и интерстициальный пневмонит (9%).
Лимфаденопатия
Бессимптомная IgG4-сопряженная генерализованная лимфаденопатия встречается у 80% пациентов с АИП [24]. Увеличение лимфатических узлов, как правило, совпадает с другими клиническими и лабораторными проявлениями синдрома, но также может являться начальным и единственным признаком болезни [15]. Для постановки диагноза IgG4-СП биопсия лимфатических узлов нецелесообразна, так как они редко подвергаются характерному фиброзу, а большое количество IgG4-положительных клеток можно обнаружить и при других заболеваниях. Поэтому для верификации диагноза необходимо проводить биопсию других органов.
В исследовании 114 пациентов с поражением различных органов лимфаденопатия встречалась в 41% случаев [60]. Иногда симптомы возникают из-за давления увеличенного лимфатического узла на окружающие ткани, отдельные узлы, как правило, не более 2 см в диаметре, но могут достигать и 5 см [15].
Как правило, в процесс вовлечены несколько групп лимфатических узлов; наиболее часто поражаются медиастинальные, грудные, внутрибрюшные и подмышечные, что легко обнаруживается при сканировании с галлием-67 [44]. Лимфаденопатия, как правило, не прогрессирует, а сами узлы эластичные.
У пациентов с лимфаденопатией может быть обнаружено повышение уровня IgG4, сывороточных IgG и IgE, поликлональная гипергаммаглобулинемия и повышение скорости оседания эритроцитов.
Дифференциальную диагностику генерализованной лимфаденопатии проводят с такими состояниями как саркоидоз, мультицентрическая болезнь Кастлемана4, инфекционные заболевания (например, туберкулез), лимфомы или другие злокачественные новообразования. IgG4-сопряженная лимфаденопатия отличается от перечисленных заболеваний умеренным увеличением лимфатических узлов, гистологической картиной, отсутствием клинических признаков, и хорошей реакцией на терапию глюкокортикоидами [13]. У пациентов с двусторонней внутригрудной лимфаденопатией можно заподозрить саркоидоз.
Аутоиммунный панкреатит
АИП тип 1 является самым типичным проявлением IgG4-СП. Распространенность его в Японии составляет 0,82 на 100 000 человек, но вероятно этот показатель значительно выше, так как признание это нозологической единицы началось относительно недавно [41]. На данный момент выделено 2 типа АИП; тип 1 — IgG4-сопряженный АИП, также обозначается как лимфоплазмоцитарный склерозирующий панкреатит [46].
АИП встречается примерно у 2% пациентов с хроническим панкреатитом. Чаще всего он проявляется очаговым образованием в поджелудочной железе или безболезненной желтухой, и может ошибочно приниматься за злокачественный процесс. АИП типа 1 проявляется острым, рецидивирующим или хроническим панкреатитом, часто ассоциированным с сахарным диабетом. При использовании инструментальных методов диагностики обращает на себя внимание диффузное увеличение поджелудочной железы, ее «колбасовидная» структура, и обширный периферический отек. Эти особенности хорошо видны при компьютерной томографии органа. В большинстве случаев присутствуют и другие сопутствующие проявления IgG4-CП, например IgG4–сопряженный склерозирующий холангит, лимфаденопатия, вовлечение в процесс слюнных или слезных желез.
Дифференцировать АИП от карциномы поджелудочной железы иногда затруднительно из-за схожести клинических проявлений. При онкологическом заболевании в ткани поджелудочной железы также могут быть обнаружены IgG4-положителные плазматические клетки, хотя и в меньшей степени, чем при АИП. У некоторых пациентов с карциномой поджелудочной железы возможно повышение уровня сывороточного IgG4 (> 135 мг/дл), хотя он, как правило, менее чем в два раза превышает верхнюю границу референсного значения. Таким образом, при повышении содержания IgG4 в крови нельзя однозначно исключить злокачественное новообразование [41]. Ретроспективный анализ демонстрирует выполнение панкреатодуоденальных резекций у больных АИП в связи с подозрением на опухоль поджелудочной железы. В США, например, ретроспективно, по результатам гистологических исследований после резекции поджелудочной железы, АИП был выявлен в 10-11% случаев. Анализ данных зарубежных клиник и института хирургии имени А.В. Вишневского показал, что все резекции поджелудочной железы, выполненные по поводу АИП, сопровождались большей технической сложностью, кровопотерей, продолжительностью и большим числом осложнений по сравнению с операциями по поводу рака поджелудочной железы [1].
IgG4-сопряженный склерозирующий холангит
IgG4-сопряженный склерозирующий холангит (ИССХ) является гепатобилиарным вариантом IgG4-СП и часто связан с АИП тип 1 (70%). Наиболее частые клинические симптомы при ИССХ — желтуха (77%), потеря веса (51%), умеренная абдоминальная боль (26%), стеаторея (15%) и вновь сформировавшийся диабет (8%) [3].
К сожалению, клиническое различие между первичным склерозирующим холангитом (ПСХ) и/или холангиокарциномой и ИССХ может быть затруднено. Биопсия ткани осуществляется при помощи эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) и не всегда удается получить материал для определения гистологической картины [10].
При ИССХ может быть значительно повышен уровень IgG4 в сыворотке крови. На холангиограммах видны сегментарные стриктуры и стриктуры дистальных желчных протоков, в то время как при ПСХ определяются «бусо-подобные» стриктуры. Развитие патологических изменений в других органах и хорошая реакция на терапию глюкокортикоидами также позволяет заподозрить ИССХ [3].
В одном из исследований показано, что у пациентов с холангиокарциномой в отличие от пациентов с IgG4-сопряженным склерозирующим холангитом чаще обнаруживаются желтуха, увеличение поджелудочной железы и лимфатических узлов. Кроме того, у таких пациентов, как правило, более высокие концентрации билирубина и онкомаркера СА 19-9 в сыворотке крови [51].
Поражение слюнных и слезных желез
Поражение слюнной железы является частым проявлением IgG4-CП. У пациентов это проявляется увеличением слезных и слюнных желез (околоушных и/или поднижнечелюстных) или односторонним или двусторонним склерозирующим сиалоаденитом поднижнечелюстных желез. Ранее эти состояния называли болезнью (или синдромом) Микулича и опухолью Кюттнера соответственно, и ошибочно считали разновидностью синдрома Шегрена. У множества пациентов был описан синдром Шегрена ассоциированный с аутоиммунным панкреатитом, и, вероятно, это была IgG4-СП.
Было проведено исследование пациентов, которые по критериям попадали и под синдром Шегрена и под IgG4-СП. Повышение уровня IgG4 в сыворотке крови было обнаружено у 7,5% в когорте из 133 пациентов с ясно выраженными клиническими признаками первичного синдрома Шегрена [39]. У пациентов с повышенным уровнем IgG4 отмечается высокая частота выявления клинических признаков IgG4-СП (аутоиммунный панкреатит, аутоиммунный холангит и интерстициальный нефрит), а также более низкие показатели антинуклеарных, anti-Ro/SSA и anti-La/SSB аутоантител. Кроме того у 2,3% пациентов при биопсии губных слюнных желез было обнаружено большое количество IgG4-положительных плазматических клеток. Вероятно, у большинства этих пациентов была IgG4-СП, а диагноз синдром Шегрена им поставили ошибочно.
Клинические признаки, которые характеризуют IgG4-сопряженный сиалоаденит и позволяют отличить его от синдрома Шегрена, включают [37]:
• Меньшее число пациентов с сухостью во рту, сухостью глаз или артралгиями (38%, 33% и 16% по сравнению с 87%, 94% и 48% соответственно). Несмотря на значительное увеличение слезных и слюнных желез, пациенты испытывают незначительную сухость глаз и сухость во рту
• Более высокая частота аллергического ринита и бронхиальной астмы (41% и 14% по сравнению с 7% и 3% соответственно)
• Более высокая частота АИП и интерстициального нефрита (17% и 17% по сравнению с 0% и 7% соответственно)
• Более низкие концентрации аутоантител, в том числе ревматоидного фактора, антинуклеарных антител, anti-SSA, anti-SSB (27%, 23%, 2% и 0% по сравнению с 87%, 90%, 100% и 100% соответственно).
Также было проведено исследование пациентов с IgG4–сопряженной патологией слезных желез (IgG4-сопряженный дакриоаденит) [47]. Характерно двустороннее поражение слезных желез, хотя начало заболевания может быть асинхронным. Гистологические и серологические результаты аналогичны тем, что наблюдаются при сиалоадените и других формах болезни.
По некоторым данным, IgG4-СП составляют от 25 до 50% от всех орбитальных псевдоопухолей, в том числе и тех, которые до определения IgG4-СП были диагностированы как доброкачественная лимфоидная гиперплазия. Также IgG4-СП признается как причина орбитального миозита (IgG4-сопряженный орбитальный миозит), который зачастую приводит к развитию экзофтальма у пациентов с данным заболеванием [40].
Нельзя определенно сказать предрасполагает ли IgG4-СП к развитию МАLT-лимфомы или других лимфом придатков глаза. Было зарегистрировано несколько таких случаев, но необходимы дальнейшие исследования [52].
Ретроперитонеальный фиброз и связанные с ним расстройства
Ретроперитонеальный фиброз является одной из наиболее часто встречающихся форм IgG4-СП. Результаты нескольких серий исследований позволяют предположить, что IgG4-СП является причиной большинства случаев ретроперитонеального фиброза, который ранее рассматривался как «идиопатический». По разным данным от 30 до 60 случаев ретроперитонеального фиброза является проявлением IgG4-СП. При данном заболевании разрастания фиброзной ткани с выраженным воспалительным инфильтратом наиболее часто обнаруживают в области брюшной аорты, подвздошных артерий, поджелудочной железы, мочеточников и почечных артерий. Клинически это проявляется компрессией различных анатомических структур разрастаниями фиброзной ткани [6]. В некоторых случаях эффективна терапия глюкокортикоидами. Постановка диагноза IgG4-СП может быть затруднена из-за обширных фиброзных изменений.
Во всех 14 случаях IgG4-сопряженного ретроперитонеального фиброза, собранных в одном обзоре, присутствует поражение других органов, в том числе поджелудочной железы (11 пациентов), слюнных желез (3 пациента), лимфатических узлов (2 пациента), в одном случае поражение гипофиза, и еще в одном случае медиастинальный периаортит [50]. Также описаны случаи изолированного IgG4-сопряженного ретроперитонеального фиброза.
Описаны случаи, когда IgG4-СП стала причиной развития склерозирующего мезентерита, склерозирующего медиастинита и мультифокального фибросклероза [25].
Аортит и периаортит
IgG4-СП была признана одной из причин неинфекционного аортита [50]. Среди пациентов, которым была проведена резекция участка аорты, в ретроспективных патологоанатомических исследованиях были выявлены больные с лимфоплазмоцитарным аортитом, воспалительной аневризмой брюшного отдела аорты и брюшным периаортитом [31, 49, 50].
IgG4-сопряженный торакальный аортит. В течение 5 лет в североамериканской больнице проводилось исследование 638 пациентов, перенесших резекцию фрагмента аорты, трем из четырех пациентов с лимфоплазмоцитарным аортитом на основании гистологии выставлен диагноз IgG4-СП [49]. Эти 3 пациента составили 9% из 33 случаев неинфекционного аортита и 0,5% от всех случаев резекций аорты. Эти три пациента были мужчинами в возрасте от 65 до 76 лет [50].
В больнице Японии также были выявлены 2 пациента (1,6%) с IgG4-сопряженным аортитом среди 120 больных, перенесших операцию на аорте [30]. В дополнение у 3 пациентов с атеросклеротическими изменениями, но без других проявлений IgG4-СП, были обнаружены аналогичные инфильтраты с IgG4-положительными плазматическими клетками. Следует ли пациентов с явными атеросклеротическими изменениями относить к группе пациентов с IgG4-СП окончательно не выяснено [30, 50].
IgG4-сопряженный абдоминальный аортит. По результатам исследования в медицинском центре Японии за период 15 лет, 4 из 10 пациентов с воспалительной аневризмой брюшной аорты страдают IgG4-СП, что подтверждается наличием инфильтрата с IgG4-положительными плазматическими клетками и повышением IgG4 в сыворотке крови [31]. Все пациенты в возрасте от 58 до 72 лет. Воспалительный абдоминальный аортит связан с ретроперитонеальным фиброзом [50].
Заболевания щитовидной железы
Заболевания легких и плевры
Было зафиксировано множество случаев IgG4-сопряженных заболеваний легких, которые могут протекать бессимптомно или проявляться кашлем, кровохарканием, одышкой, плевритом или болью за грудиной. Возможны псевдоопухоли и интерстициальная пневмония ассоциированные с АИП [60]. Может наблюдаться утолщение висцеральной и париетальной плевры, в пораженных тканях обнаруживаются лимфоплазмоцитарные инфильтраты, обогащенные IgG4-положительными плазматическими клетками, с очагами характерного фиброза. При IgG4-СП облитерирующий артериит чаще встречается в легких, чем в других органах [59]. Были описаны четыре типа поражения легких:
• Твердый узелок
• Бронховаскулярный (с утолщением бронховаскулярных пучков и междольчатых перегородок)
• Альвеолярно-интерстициальный («сотовое» легкое, бронхоэктазы, симптом «матового стекла»)
• Образования округлой формы, затемнения в виде «матового стекла».
Значительные трудности представляет дифференциальная диагностика IgG4-СП с саркоидозом. Проводилось исследование пациентов с подозрением на саркоидоз, у которых были выявлены двустороннее увеличение внутригрудных лимфатических узлов и/или узелки в легких при КТ-исследовании грудной клетки. У некоторых пациентов обнаружены высокие уровни IgG4 в сыворотке крови, причем уровни бронхоальвеолярных IgG4, IgG4/IgG, IgG4/IgG3 у таких больных значительно выше, чем у пациентов с нормальным уровнем сывороточного IgG4 [53].
Болезни почек
Описано множество случаев поражения почек у людей с IgG4-СП; чаще всего это тубулоинтерстициальный нефрит (ТИН). Как правило, данная форма заболевания поражает мужчин среднего возраста и пожилых. Гистологические и лабораторные признаки аналогичны таковым при АИП. Имеют место очаговые поражения ткани, имитирующие злокачественные новообразования.
Из нескольких медицинских центров Японии собрали 153 человека с подозрением на IgG4-СП для ретроспективного исследования и обнаружили у 23 пациентов (15%) вторичный ТИН [45]. За исключением одного человека, все пациенты (96% с ТИН) имели и другие проявления IgG4-СП. К этим проявлениям относились: сиалоаденит (83%), лимфаденопатия (44%), АИП (39%), дакриоаденит (30%), поражения легких (26%), а также поражение других органов. Помимо ТИН у 3 из 23 пациентов был обнаружен умеренный мезангиопролиферативный гломерулонефрит (ГН), в 1 случае были обнаружены мембранозная нефропатия и очаговая сегментарная интракапиллярная гиперклеточность.
Почечные нарушения были выявлены при нарушении функции органа и/или с помощью инструментальных методов: изменение почечного рисунка на КТ и усиленное поглощение почкой цитрата галлия на сцинтиграфии.
У пациентов с IgG4-сопряженным ТИН была выраженная гипокомплементемия, уровни сывороточного С3 и С4 как при системной красной волчанке и смешанной криоглобулинемии [57]. Причина развития гипокомплементемии не совсем ясна, так как сам IgG4 связывается с комплементом плохо.
IgG4-сопряженная мембранозная нефропатия встречается намного реже чем ТИН. Иногда их можно обнаружить одновременно [9]. В исследовании 9 пациентов с IgG4-сопряженным мембранозным ГН у 5 выявлен IgG4-сопряженный ТИН, у 7 присутствовали другие проявления IgG4-СП [89]. Ни у одного из пациентов при биопсии не выявлено аутоантител к рецепторам фосфолипазы А2, хотя они определяются у всех пациентов с первичный мембранозным ГН.
Поражение других органов и тканей
Дополнительно было описано несколько случаев поражения других органов и тканей:
• Кожные заболевания, в том числе кожная псевдолимфома. Повреждения обычно проявляются на коже головы, лица, шеи и ушной раковины [14].
• IgG4-сопряженные поражения печени, напоминающие аутоиммунный гепатит и воспалительную псевдоопухоль печени [56].
• Лимфоплазмоцитарный гастрит, связанный с аутоиммунным панкреатитом [54].
• Склерозирующий мастит и воспалительные псевдоопухоли молочной железы [12].
• Поражения ЦНС, гипопитуитаризм, ассоциированный с IgG4-сопряженным повреждением гипофиза, наиболее частое проявление — пахименингит [27].
• Простатит [55].
• Констриктивный перикардит [32].
• Назофарингеальные заболевания [21].
• Срединное деструктивное поражение [17]
Диагностика
Диагностика IgG4-СП основана на гистопатологических и иммунногистохимических результатах биопсии. Они включают в себя: лимфоплазмоцитарную инфильтрацию ткани, в основном IgG4-положительными плазматическими клетками и лимфоцитами, очаги фиброза с характерным узором и облитерирующий флебит. Можно выявить умеренную эозинофилию. В обязательном порядке измеряют уровень сывороточных IgG4, хотя их повышение не всегда является диагностическим критерием IgG4-СП. Гистопатологические и иммуногистохимические особенности IgG4-СП схожи во всех пораженных органах и тканях.
Показания к диагностике — проведение мероприятий по диагностике IgG4-СП целесообразно при клинической картине поражения органов, характерного для IgG4-СП.
Пациенты имеют повышенный риск наличия IgG4-СП, при любом из следующих условий:
• Панкреатит неизвестной этиологии
• Склерозирующий холангит
• Двустороннее увеличение слюнных и/или слезных желез
• Ретроперитонеальный фиброз
• Орбитальная псевдоопухоль или экзофтальм.
Вероятность того, что у пациента IgG4-СП при наличии хотя бы одного из этих условий значительно повышается, если, кроме того, повышен уровень сывороточного IgG4, имеются симптомы аллергии и/или в организме выявляются другие фиброзные процессы.
Диагностические исследования
Биопсия ткани. Выбор процедуры зависит от конкретного пораженного органа и доступности патологического очага. В основном применяют сердцевинную биопсию5, тонкоигольная аспирационная биопсия не может обеспечить достаточного количества ткани [13, 59]. При наличии нетипичных патоморфологических и клинических признаков, совместимых с IgG4-СП, биопсия других органов, не проводится, особенно при положительном эффекте терапии глюкокортикоидами.
Сывороточный IgG4. В исследовании 114 пациентов, у 86% было выявлено увеличение уровня IgG4 в сыворотке крови (> 135 мг/дл) [59]. Степень повышения IgG4 не коррелирует со степенью активности процесса. Однако, увеличение титров IgG4, позволяет заподозрить у пациента IgG4-СП. Концентрация данных иммуноглобулинов увеличивается при вовлечении в патологический процесс большего числа органов, и уменьшается при терапии глюкокортикоидами [13, 29].
В одном учреждении в течение 10 лет (с 2001 по 2011 г.г.) проводилось исследование по измерению концентрации IgG4 в сыворотке крови [11]. В течение этого времени у 190 пациентов были повышены концентрации сывороточного IgG4 (> 135 мг/дл). Для сравнения были отобраны еще 190 человек с нормальными показателями IgG4. Исследование показало:
• В группе из 72 пациентов с диагностированной или предполагаемой IgG4-СП 65 имели высокие концентрации сывороточного IgG4 (в среднем: 405 мг/дл; диапазон: 140-2000 мг/дл). Диагностическая чувствительность — 90%.
• Среди 308 испытуемых без IgG4-СП, у 125 пациентов были повышены уровни IgG4 (в среднем: 234 мг/дл, диапазон: 135-1180 мг/дл), у 183 нормальные уровни иммуноглобулина. Диагностическая специфичность — 60%.
• Прогностическая ценность отрицательных результатов анализа на концентрацию сывороточного IgG4 составила 96%, прогностическая ценность положительных результатов лишь 34%.
• Увеличение верхней границы нормы вдвое повысило специфичность (91%), но снизило чувствительность до 35%. Анализ соотношения IgG4/IgG не улучшил диагностическую значимость исследования.
Плазмобласты крови как биомаркеры. Концентрация в сыворотке крови плазмобластов может быть более значимым биомаркером, чем концентрация IgG4, причем как для диагностики IgG4-СП, так и для определения активности процесса. У пациентов с IgG4-СП до начала лечения брали образцы крови, в которых были обнаружены высокие уровни плазмобластов. Плазмобласты были обнаружены с помощью проточной цитометрии стробированием на клетках CD19low CD38+ CD20- CD27+ [38]. В исследовании принимали участие 37 нелеченных пациентов с IgG4-СП, в контрольной группе 35 человек, в том числе абсолютно здоровых (n=14) и с другими активными нелеченными воспалительными заболеваниями (n=21). У пациентов с IgG4-СП, даже при нормальных уровнях сывороточных IgG4, концентрация плазмобластов будет повышена. Поэтому их считают потенциально полезными биомаркерами для диагностики и оценки эффективности лечения. Необходимы дополнительные исследования плазмобластов, в частности, результаты исследования «IgG4+плазмобласты» могут оказаться полезными для оценки реакции клеток на лечение и для прогнозирования рецидивов заболевания.
Диагностические критерии
В соглашении межнациональной многопрофильной группы экспертов по IgG4-СП описаны рекомендации по диагностике и гистологические признаки, необходимые для постановки диагноза [20, 33]. Четкие диагностические критерии ранее были описаны только для АИП. Плотный лимфоплазмоцитарный инфильтрат, характерный фиброз и облитерирующий флебит являются главными гистопатологическими критериями для постановки диагноза. Наличие в инфильтрате эозинофилов и IgG4-положительных плазматических клеток подтверждает диагноз IgG4-СП.
Количество IgG4-положительных плазматических клеток может отличаться в разных типах тканей. Подсчет IgG4-положительных клеток в ткани и коэффициента отношения IgG4 к IgG-положительным клеткам в диагностическом плане считают вторичным, по сравнению с гистопатологической картиной [13, 20, 32, 37, 59]. Как правило, для большинства тканей минимальный уровень IgG4-положительных клеток от 30 до 50 в 1 стандартном поле зрения. В некоторых органах и тканях, например почках и других органах, минимальный уровень IgG4-положительных клеток 10 в 1 стандартном поле зрения.
Диагноз не может основываться исключительно на количестве IgG4-положительных плазматических клеток, так как они могут встречаться и при других заболеваниях. Нельзя ставить диагноз на основании высокой концентрации сывороточного IgG4, данный показатель является ни достаточно чувствительным, ни достаточно специфическим для IgG4-СП. Поэтому для подтверждения диагноза, если есть возможность, необходимо провести биопсию пораженного органа. Определение концентрации плазмобластов, особенно «IgG4+плазмобласты», не является широкодоступным методом.
Лечение
Оптимальное лечение IgG4-СП официально не утверждено. Имеет место консенсус по следующим пунктам [33]:
• Всем пациентам с симптомами активной IgG4-СП требуется лечение, некоторым в срочном порядке. Подгруппе пациентов с бессимптомным течением IgG4-СП также требуется лечение.
• Глюкокортикоиды являются препаратами выбора у всех пациентов с активной нелеченной IgG4-СП, при отсутствии противопоказаний.
• После успешного завершения курса индукционной терапии, следует продолжать прием препаратов в поддерживающих дозах.
• Повторное лечение глюкокортикоидами проводят пациентам с рецидивами в том случае, если после первого курса терапии была достигнута ремиссия. После рецидива, необходимо проводить стероид сберегающую терапию для поддержания ремиссии.
Те же эксперты, которые согласились с приведенными выше решениями, разделились во мнении относительно следующего утверждения: «Некоторым пациентам необходимо начинать терапию с комбинации глюкокортикоидов и стероид-сберегающих препаратов. Потому что глюкокортикоидная монотерапия, в конечном счете, может оказаться неэффективной, а длительное применение этих препаратов, повышает риск развития тяжелых осложнений» [33]. Такое расхождение во мнениях в значительной степени отражается в практике лечения в различных странах, 80% (16 из 20) экспертов из Японии не согласны с ранним использованием второго средства, а 76% (13 из 17) экспертов из других регионов (Северная Америка, Европа, Корея, Китай) согласны.
Большинство пациентов реагируют на терапию в течение нескольких недель, как правило, наблюдается смягчение симптоматики, уменьшаются размеры очаговых образований либо самого увеличенного органа, улучшается его функция, и снижается уровень сывороточного IgG4. В некоторых случаях требуется несколько месяцев для достижения эффекта. Были зафиксированы случаи, когда пациенты слабо реагируют на терапию или не реагируют совсем. Предполагается, что пациенты, которые слабо реагируют на терапию, имеют более распространенные фиброзные изменения, но это не доказано.
Несколько типов лимфом были зарегистрированы у пациентов с IgG4-СП как в Японии, так и в США [13, 47, 52]. В ходе исследования в США, в котором участвовали 111 пациентов с IgG4-СП (91% с АИП), у 3 пациентов в течение 3-5 после постановки диагноза были обнаружены неходжкинские лимфомы [52].
В серии исследований 108 человек с IgG4-сопряженным панкреатитом, у 15 пациентов (14%) были обнаружены 18 видов злокачественных новообразований; средний период наблюдения составил 3,3 года [26]. Наиболее распространенной патологией был рак желудка, также встречались злокачественные новообразования легких, простаты, толстой кишки, желчных протоков, щитовидной железы и неходжкинские лимфомы. Из 8 пациентов, которым делали биопсию новообразования перед началом лечения IgG4-сопряженного панкреатита глюкокортикоидами, у 6 в гистологическом препарате ткани опухоли были обнаружены инфильтраты с IgG4-положительными плазматическими клетками. Ни у одного из пациентов не наблюдалось рецидивов IgG4-сопряженного панкреатита после успешного лечения рака, в связи с этим решается вопрос о том, может ли у некоторых пациентов IgG4-СП протекать как неопластический синдром. Также сообщалось о нескольких случаях рака поджелудочной железы, карциномы слюнных протоков, аденокарциномы легких, мелкоклеточного рака легких, светлоклеточной саркомы желудочно-кишечного тракта [13]. Необходимы дальнейшие исследования для определения степени риска развития этих и других злокачественных новообразований.
Выводы
1. IgG4-СП получает все большее признание во врачебном сообществе; этиология ее неизвестна; чаще страдают люди среднего и пожилого возраста. Проявляется совокупностью нарушений, имеющих специфические патологические, серологические и клинические признаки. У одного пациента можно обнаружить несколько проявлений болезни, хотя ранее эти патологии считались не связанными между собой:
• Аутоиммунный панкреатит тип 1 и IgG4-сопряженный склерозирующий холангит
• Болезнь Микулича и склерозирующий сиалоаденит (опухоль Кюттнера), воспалительная псевдоопухоль орбиты и склерозирующий дакриоаденит
• Идиопатический ретроперитонеальный фиброз и связанные с ним патологии
• Хронический склерозирующий аортит и периаортит
• Тиреоидит Риделя и тиреоидит Хашимото
• IgG4-сопряженный интерстициальный пневмонит и воспалительные псевдоопухоли легких
• IgG4-сопряженное заболевание почек, особенно ТИН
2. Признаками IgG4-СП являются лимфоплазмоцитарная инфильтрация ткани, преимущественно IgG4-положительными плазматическими клетками и лимфоцитами, фиброз, облитерирующий флебит, зачастую повышение концентрации сывороточного IgG4. У пациентов часто обнаруживается образование в пораженном органе или диффузное увеличение органа. Часто выявляется увеличение лимфатических узлов, симптомы астмы и аллергии. Характерна хорошая терапевтическая реакция на глюкокортикоиды.
3. Диагноз IgG4-СП выставляется по характерным гистопатологическим результатам биопсии. Уровень сывороточного IgG4 должен быть изменен; в отдельных случаях повышение концентрации иммуноглобулина в крови является полезным для диагностики, но не является диагностическим критерием. Поражение других органов при IgG4-СП можно обнаружить при тщательном сборе анамнеза, объективном обследовании, при использовании рутинных лабораторных анализов и инструментальных методов исследования.
4. Рекомендуется начинать лечение с глюкокортикоидов.
5. Течение болезни и прогноз до конца не изучены. Иногда можно наблюдать спонтанные улучшения, но без лечения болезнь часто рецидивирует.
Примечания.
1 Эотаксин-1 представляет собой белок, состоящий из 72 аминокислот, который может продуцироваться самыми разными клетками (в том числе эозинофилами, эпителиальными клетками, фибробластами, клетками эндотелия, Т-лимфоцитами, моноцитами и макрофагами) после их активации провоспалительными медиаторами. Является активным лигандом рецептора 3 хемокина СС (CCR3), который постоянно экспрессируется на эозинофилах. В недавнем времени было показано, что CCR3 экспрессируется на базофилах и Т-хелперах 2 типа, что позволяет сделать предположение о том, что CCR3 может играть определенную роль в запуске и сохранении воспаления.
2 В некоторых отечественных источниках можно встретить термин «муароформный» фиброз: Циммерман Я.С. Аутоиммунный панкреатит — особая форма хронического панкреатита; РЖГГК. 2013; 23(3): 9-15.
3 Midline destructive lesion (MDL) — также известное как «летальная срединная гранулема», представляет собой фиброзно-деструктивный процесс, характеризующийся прогрессирующей эрозией носа, придаточных пазух и неба
4 Болезнь Кастлемана (ангиофолликулярная гиперплазия лимфатических узлов) — редкое доброкачественное лимфопролиферативное заболевание с длительным бессимптомным течением, ассоциированное с широким спектром аутоиммунных и онкологических заболеваний и риском развития неходжкинской лимфомы. Мультицентрическая болезнь Кастлемана — редкий вариант БК. Клинически проявляется периферической лимфаденопатией и органомегалией (гепатоспленомегалия встречается в 63% случаев). Из других проявлений, позволяющих заподозрить МБК — лихорадка, похудение, болевой синдром, кожный зуд, одышка, диспептические расстройства. Диагноз ставится на основании специфической иммуногистохимической картины в пораженном лимфатическом узле.
5 Сердцевинная биопсия (core-биопсия) — забор мягких тканей при помощи трепана с гарпунной системой.
Конфликт интересов/Conflict of interests
Авторы заявляют, что данная работа, её тема, предмет и содержание не затрагивают конкурирующих интересов/The authors state that this work, its theme, subject and content do not affect competing interests