впо что это такое в медицине расшифровка
Роспотребнадзор
Роспотребнадзор
Вниманию медицинских работников о ситуации по выявлению больных с ОВП
Вниманию медицинских работников о ситуации по выявлению больных с ОВП
Под ОВП понимают любой случай остро возникшего паралича (пареза) в одной или нескольких конечностях у детей до 15 лет.
Выявление больных с синдромом ОВП осуществляется на всех этапах оказания медицинской помощи больному при его обращении (ФАП, амбулатория, поликлиника, стационар, скорая помощь и др.), а также при проведении активного эпидемиологическ ого надзора в ЛПО, в которых могут находиться больные с ОВП (педиатрические, инфекционные, неврологические стационары или отделения больниц, дома ребенка, детские дома, санатории по реабилитации неврологических больных и др).
Синдром ОВП может встречаться при многих инфекционных и неинфекционных патологиях. К наиболее часто встречающимся нозологическим формам относятся:
— острый паралитический полиомиелит;
— полинейропатии (включая синдром Гийена-Барре);
— мононейропатии, в т.ч. травматические (постинъекционны е) и т.д.
В целях ликвидации полиомиелита с 1996 года в нашей стране введен эпидемиологическ ий надзор за ОВП среди детей до 15 лет.
Наиболее существенными мероприятиями в борьбе с полиомиелитом на современном этапе являются:
— увеличение уровня охвата профилактическим и прививками населения (не менее 95%) с помощью плановой, дополнительной и подчищающей иммунизации;
— улучшение качества лабораторной диагностики с вирусологическим подтверждением каждого случая заболевания
полиомиелитом и постоянного проведения эпидемиологическ ого надзора
за острыми вялыми параличами (ОВП) среди детей до 15 лет.
Проведение эпидемиологическ ого надзора за острыми вялыми
параличами является особенно важным, т.к. это позволяет выявить и
не пропустить ни одного случая полиомиелита, вызванного «диким»
полиовирусом местного или импортированного из другой страны.
В Российской Федерации ежегодно регистрируется от 300 и более случаев ОВП. В Северной –Осетии за 2013-2014гг. было зарегистрировано по 2 случая ОВП. За 10 месяцев 2015 года республика является «молчащей» территорией т.е. не выявлено ни одного случая ОВП, что свидетельствует о недостаточной настороженности медицинских работников в отношении острых вялых параличей.
Искусственная вентиляция легких (ИВЛ): инвазивная и неинвазивная респираторная поддержка
К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
Инвазивная вентиляция легких
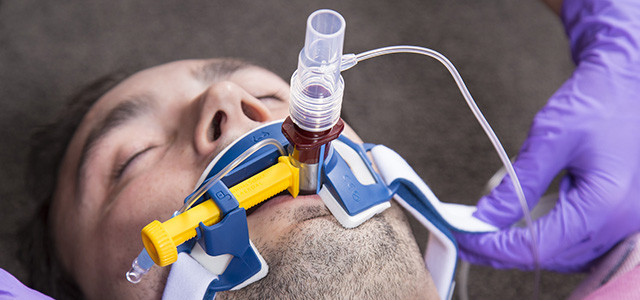
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
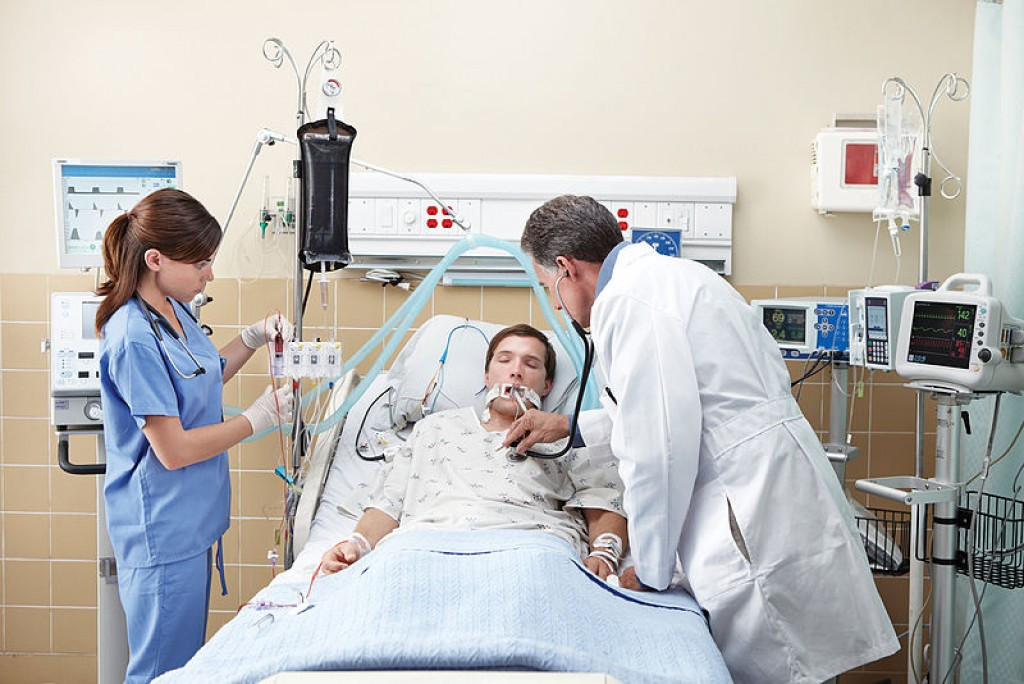
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
Неинвазивная вентиляция легких
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
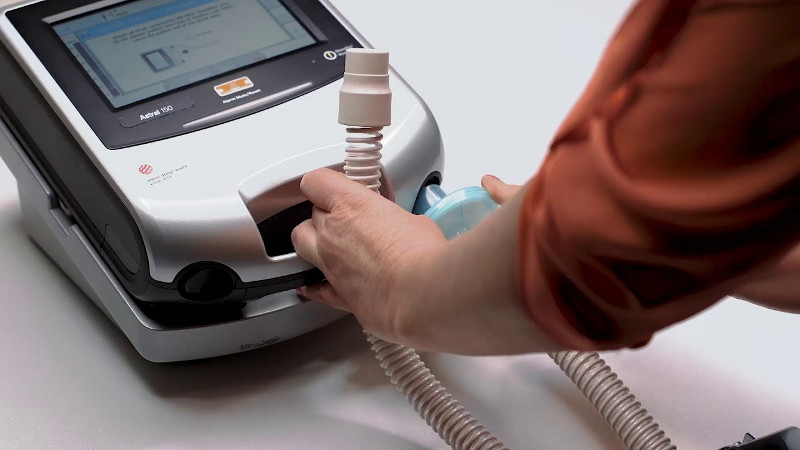
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
Сравнительный анализ использования высокопоточной и традиционной оксигенотерапии у пациентов с тяжелой внебольничной пневмонией
1 ФГБВОУ ВО «Военно-медицинская академия имени С.М. Кирова» МО РФ, Санкт-Петербург, Россия
2 ФГКУ «442 Военно-клинический госпиталь» МО РФ, Санкт-Петербург, Россия
Для корреспонденции: Грачев Иван Николаевич — преподаватель кафедры военной анестезиологии и реаниматологии Военно-медицинской академии имени С.М. Кирова, Санкт-Петербург; е-mail: GrachewIN@mail.ru
Для цитирования: И.Н. Грачев, В.И. Шаталов, А.Г. Климов, И.В. Блинда, И.А. Кочкин, К.А. Цыганков, А.В. Щеголев. Сравнительный анализ использования высокопоточной и традиционной оксигенотерапии у пациентов с тяжелой внебольничной пневмонией. Вестник интенсивной терапии им. А.И. Салтанова. 2020;3:95–103. DOI: 10.21320/1818-474X-2020-3-95-103
Реферат
Актуальность. Для пациентов с сохраненным спонтанным дыханием и дыхательной недостаточностью разработаны различные способы доставки газовой смеси в дыхательные пути. Открытым остается вопрос о выборе оптимальной методики при гипоксии у пациентов с тяжелой внебольничной пневмонией. Применение высокопоточной оксигенотерапии является альтернативой ингаляции кислорода через стандартные канюли.
Цели исследования. Экспериментальное изучение механизмов воздействия высокопоточной оксигенотерапии и оценка ее клинической эффективности в сравнении с традиционной оксигенотерапией у пациентов с тяжелой внебольничной пневмонией.
Материалы и методы. При проведении экспериментального этапа исследования определен уровень среднего давления в дыхательных путях в зависимости от потока газовой смеси с использованием модели легких с параметрами биомеханики дыхания, характеризующими «здоровые легкие», «легкие со сниженной растяжимостью» и «легкие с высоким сопротивлением дыхательных путей».
При проведении клинического этапа осуществлен сравнительный анализ эффективности респираторной поддержки в группах пациентов с тяжелой внебольничной пневмонией с использованием высокопоточной и традиционной оксигенотерапии.
Результаты. При проведении экспериментального исследования определен поток газовой смеси 30 л/мин, при котором значимо увеличивается среднее давление в дыхательных путях, регистрируемое на моделях «здоровых» легких и легких с измененной биомеханикой дыхания.
В ходе проведения клинического этапа исследования установлено значимое снижение частоты инициации искусственной (инвазивной и неинвазивной) вентиляции легких, увеличение показателей оксигенации (насыщение гемоглобина кислородом, парциальное давление кислорода в артериальной крови) и парциального давления углекислого газа в артериальной крови с одновременным снижением частоты дыхания.
Выводы. Величина потока газовой смеси более 30 л/мин значимо увеличивает среднее давление в дыхательных путях в эксперименте при моделировании «здоровых легких», «легких со сниженной растяжимостью» и «легких с высоким сопротивлением дыхательных путей». Однако клиническое значение данного показателя несущественно.
Использование высокопоточной оксигенотерапии у пациентов с тяжелой внебольничной пневмонией в сравнении со стандартной методикой уменьшает частоту применения искусственной (инвазивной и неинвазивной) вентиляции легких при увеличении показателей оксигенации. При этом уменьшается гипервентиляция, что подтверждается увеличением парциального давления углекислого газа в артериальной крови и снижением частоты дыхания.
Ключевые слова: высокопоточная оксигенотерапия, терапия ингаляцией кислорода, пневмония
Поступила: 30.02.2020
Введение
Внебольничная пневмония (ВБП) — одно из распространенных заболеваний органов дыхания, представляющее актуальную проблему в интенсивной терапии и связанное с высокой летальностью как среди взрослых, так и среди детей [1–3]. Заболеваемость в Европе составляет от 1,6 до 10,6 % [4, 5]. При этом в Российской Федерации за январь — апрель 2018 г., по данным Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, зарегистрировано около 300 000 случаев ВБП (2,01 %) [6].
Острая дыхательная недостаточность (ОДН) часто осложняет ВБП и является основным фактором, определяющим госпитализацию пациентов в отделение реанимации и интенсивной терапии (ОРИТ). Внутрилегочное шунтирование и нарушение вентиляционно-перфузионных отношений в легких — основные патофизиологические механизмы развития гипоксемии при пневмонии [7]. Оксигенотерапия оказывает незначительное воздействие на шунтирование, однако при этом значительно ухудшаются вентиляционно-перфузионные отношения вследствие гипоксической легочной вазоконстрикции. У пациентов с тяжелой ВБП данный факт может стать причиной увеличения физиологического мертвого пространства [8]. В настоящее время активно развиваются методики респираторной терапии, уменьшающие потребление кислорода организмом вследствие создания положительного давления в дыхательных путях, приводящего к уменьшению работы дыхания пациента.
В то же время одной из причин того, что от 37 до 60 % пациентов с ВБП, поступивших в ОРИТ, нуждаются в искусственной вентиляции легких (ИВЛ), является неэффективное использование стандартных методик оксигенотерапии [9, 10]. При угрожающей жизни ОДН, а также в случаях несостоятельности функций нескольких органов и систем ИВЛ остается основным методом интенсивной терапии. Однако его применение может стать причиной как легочных, так и внелегочных осложнений [11].
Экспериментальное и клиническое обоснование использования неинвазивных методик оксигенотерапии (например, высокопоточной оксигенотерапии (ВПО)), минимально влияющих на структуру и функцию легких, обеспечивая при этом оптимальную оксигенацию и вентиляцию, является перспективным направлением исследований в области респираторной медицины. Основой для данной методики служит применение скорости потока до 60 л/мин с возможностью установки температуры, влажности, фракции кислорода во вдыхаемой смеси (FiO2) [12].
В отечественных рекомендациях скорость потока 30 л/мин определяется как стартовая величина при гипоксемической ОДН. Однако физиологического обоснования наиболее оптимального алгоритма выбора первичных настроек ВПО у больных с ОДН различного генеза нет [1].
Исходя из вышесказанного, целью исследования явились экспериментальное изучение механизмов воздействия ВПО и оценка ее клинической эффективности в сравнении с традиционной оксигенотерапией у пациентов с тяжелой ВБП.
Материалы и методы
Исследование одобрено независимым этическим комитетом при Военно-медицинской академии им. С.М. Кирова (Протокол № 207 от 22 мая 2018 г.). Экспериментальный этап исследования проводили на базе симуляционного центра Военно-медицинской академии им. С.М. Кирова в период с 2017 по 2018 г. Клинический этап исследования проводили в Военно-медицинской академии им. С.М. Кирова в период с 2018 по 2019 г.
Для оценки изучаемых показателей применяли аппарат ИВЛ Hamilton G5 (Hamilton Medical, Швейцария) с наличием режима HighFlow, позволяющего проводить ВПО через контур доставки газа с устройством соединения с трахеостомической канюлей OPT870 (Fisher & Paykel, Healthcare Ltd).
В качестве модели легких использовали высокореалистичный симулятор TestChest® Respiratory Flight Simulator (Organis-GmbH, Швейцария), состоящий из точной модели легких со сложной системой математического моделирования для обеспечения воспроизведения легочной механики, газообмена и гемодинамических реакций взрослого человека в норме и при различных патологических состояниях как при сохранении самостоятельного дыхания, так и при проведении ИВЛ.
В данном исследовании использовали три модели биомеханики дыхания: «здоровые легкие», «легкие со сниженной растяжимостью» и «легкие с высоким сопротивлением дыхательных путей». Все измерения проводили при комнатной температуре и влажности.
Основные характеристики моделей представлены в табл. 1.
Таблица 1. Параметры моделей легких TestChest® Respiratory Flight Simulator
Table 1. TestChest® Respiratory Flight Simulator parameters
Изменяемый параметр биомеханики дыхания модели
Варианты моделей эксперимента
Здоровые легкие
Легкие со сниженной растяжимостью
Легкие с высоким сопротивлением дыхательных путей
Растяжимость ниже нижней точки перегиба, мл/см вод. ст.
Растяжимость выше верхней точки перегиба, мл/см вод. ст.
Общая растяжимость, мл/см вод. ст.
Сопротивление дыхательных путей, условные единицы
Нижняя точка перегиба, см вод. ст.
Верхняя точка перегиба, см вод. ст.
Регистрацию показателей проводили на семи этапах исследования. На каждом этапе устанавливали величину потока и концентрацию кислорода 50 % на фоне моделирования параметров системы дыхания человека с частотой 14 уд. в мин. Для базового измерения показателей системы дыхания применяли поток 0 л/мин, для моделирования стандартной оксигенотерапии — от 5 до 15 л/мин с шагом 5 л/мин, для моделирования ВПО — от 30 до 50 л/мин с шагом 10 л/мин. При этом величина потока 30 л/мин определена в соответствии с отечественными рекомендациями по проведению неинвазивной вентиляции легких, как рекомендуемая при гипоксемической ОДН [1].
Для оценки результатов были выбраны параметры состояния дыхательной системы пациента.
В дальнейшем проводился клинический этап исследования, заключающийся в сравнительном анализе эффективности респираторной поддержки с использованием ВПО и традиционной оксигенотерапии (группы 1 и 2) у пациентов с ВБП и признаками ОДН. Количество пациентов в каждой группе составило 32 человека.
Критериями включения определены:
Критериями исключения определены:
Для объективной оценки тяжести ВБП применяли шкалу SMRT-CO (systolic blood pressure, multilobar chest radiography involvement, respiratory rate, tachycardia, confusion, oxygenation), учитывающую клинические, лабораторные и инструментальные признаки [2]. ВБП оценивали как тяжелую при сумме баллов 4 и более. Общая характеристика групп пациентов представлена в табл. 2.
Таблица 2. Антропометрические показатели, сопутствующая патология и тяжесть основного заболевания пациентов 1-й и 2-й групп
Table 2. Anthropometric indicators, concomitant pathology and the severity of the underlying disease in patients of groups 1 and 2
Показатель
Группа 1
Группа 2
(n = 32)
Значение p
Впо что это такое в медицине расшифровка
ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия; ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия; ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия
ФГБОУ ВО СГМУ Минздрава России, Архангельск, Россия
Применение высокопоточной оксигенации в терапии острого респираторного дистресс-синдрома
Журнал: Анестезиология и реаниматология. 2020;(1): 47-54
Ушаков А. А., Смёткин А. А., Фот Е. В., Кузьков В. В., Киров М. Ю. Применение высокопоточной оксигенации в терапии острого респираторного дистресс-синдрома. Анестезиология и реаниматология. 2020;(1):47-54.
Ushakov A A, Smyotkin A A, Fot E V, Kuzkov V V, Kirov M Yu. High flow oxygenation in acute respiratory distress syndrome: possibilities and perspectives. Russian Journal of Anaesthesiology and Reanimatology. 2020;(1):47-54.
https://doi.org/10.17116/anaesthesiology202001147
ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
Высокопоточная назальная оксигенация позволяет обеспечить доставку увлажненной и подогретой кислородно-воздушной смеси с фракцией вдыхаемого кислорода от 21 до 100% и величиной потока до 80 л/мин. Высокопоточная оксигенация имеет определенные преимущества перед неинвазивной вентиляцией легких. Как показывают результаты недавних исследований, высокопоточная оксигенация не менее эффективна, чем традиционная оксигенотерапия, а в ряде ситуаций более комфортна для пациента и может эффективно использоваться на различных этапах лечения острого респираторного дистресс-синдрома.
ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия; ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия; ГБУЗ АО «Первая городская клиническая больница им. Е.Е. Волосевич», 163000, Архангельск, Россия
ФГБОУ ВО «Северный государственный медицинский университет» Минздрава России, 163000, Архангельск, Россия
ФГБОУ ВО СГМУ Минздрава России, Архангельск, Россия
Кислородотерапия является средством первого ряда для лечения гипоксемической дыхательной недостаточности, однако эффективность этой методики ограничена, особенно при необходимости наращивания фракции вдыхаемого кислорода. Следует также учитывать, что при использовании стандартной маски или носовых канюль фракция вдыхаемого кислорода, как правило, не превышает 40% за счет «примешивания» окружающего воздуха. Ограничены также возможности подогрева дыхательной смеси и поддержания положительного давления в конце выдоха, что снижает клиническую эффективность метода [1]. Альтернативой в таких случаях является инвазивная искусственная вентиляция легких (ИВЛ). Данный метод сам по себе является жизнеспасающим, но при этом не лишен ряда недостатков. К наиболее частым осложнениям ИВЛ относят вентилятор-ассоциированную пневмонию и трахеобронхит, баро-, волюмо-, оксигено- и ателектотравму [2—5].
В качестве еще одного метода респираторной терапии может выступать неинвазивная вентиляция легких (НИВЛ). Данная методика хорошо зарекомендовала себя в лечении декомпенсации хронической обструктивной болезни легких (ХОБЛ), некардиогенного и кардиогенного отека легких [6—12]. К факторам, ограничивающим ее активное применение, можно отнести трудоемкость метода, а в ряде ситуаций — дискомфорт для пациента. В начале XXI века для респираторной поддержки пациентов в критическом состоянии начали рассматривать еще менее инвазивную методику — высокопоточную оксигенацию (ВПО) [6, 12, 13]. Последняя имеет ряд преимуществ перед стандартной оксигенотерапией и НИВЛ в лечении артериальной гипоксемии, не вызывает существенного дискомфорта у больного и обеспечивает величину инспираторного потока, близкую к потребностям пациента с дыхательной недостаточностью (40—60 л/мин) [14, 15].
Возможности применения ВПО в терапии острого респираторного дистресс-синдрома (ОРДС) являются в настоящее время предметом повышенного интереса со стороны врачей-анестезиологов-реаниматологов и требуют активного изучения. На данный момент нет четких алгоритмов по применению ВПО при ОРДС, не определены оптимальные показания для использования данной методики у этой категории больных, что побудило авторов к написанию обзора.
Высокопоточная оксигенация: ключевые принципы
Высокопоточная назальная оксигенация позволяет обеспечить доставку увлажненной и подогретой кислородно-воздушной смеси с фракцией вдыхаемого кислорода от 21 до 100% и величиной потока до 80 л/мин. Методика ВПО включает различные системы для эффективного увлажнения и согревания газовой смеси [13].
Принципиальными особенностями ВПО являются возможности пошаговой регуляции скорости потока и температуры, а также точность установки фракции вдыхаемого кислорода. Современные системы ВПО располагают специальными дыхательными контурами из полупроницаемого материала, не допускающего образования конденсата, а также оригинальными носовыми или трахеостомическими канюлями. При этом максимальный поток, тип увлажнения и дизайн носовых канюль варьируют в зависимости от модели устройства. На сегодняшний день оборудование для высокопоточной кислородотерапии представлено несколькими производителями [13, 14]. Кроме того, ВПО стала появляться в качестве дополнительной опции на аппаратах ИВЛ [15].
Основные эффекты высокопоточной назальной оксигенации
Основными положительными эффектами ВПО являются соответствие величины потока аппарата на вдохе потоку в дыхательных путях пациента с дыхательной недостаточностью и возможность повышения фракции кислорода на вдохе. К физиологическим эффектам ВПО относится и уменьшение мертвого пространства дыхательных путей, что обеспечивается за счет высокого потока кислородно-воздушной смеси (эффект вымывания, washout effect). Более того, высокий поток обеспечивает динамический рост давления в дыхательных путях на выдохе (эффект положительного давления в конце выдоха, ПДКВ), что способствует расправлению спавшихся альвеол и вовлечению их в газообмен [16, 17]. Повышение ПДКВ на фоне высокопоточной назальной оксигенации ограничено 2—7 см вод. ст., поэтому оно не сопровождается нарушениями гемодинамики [13, 18, 19]. Поток газовой смеси с температурой от 31 °C и выше дает возможность дополнительного согревания и увлажнения слизистой дыхательных путей, что благоприятно влияет на газообмен и переносимость пациентом процедуры. Благодаря оригинальной методике постоянного испарения влаги в контуре обеспечивается оптимальная влажность подаваемой смеси.
Таким образом, подогрев и адекватное увлажнение смеси способствуют улучшению клиренса слизистого секрета, что уменьшает бронхообструкцию и препятствует дальнейшему ателектазированию. Следует также отметить, что создание высокого потока сводит к минимуму «примешивание» окружающего воздуха, позволяя обеспечить стабильную и управляемую фракцию вдыхаемого кислорода, вплоть до 100% [20, 21]. Описанные эффекты позволяют улучшить элиминацию углекислого газа (СО2), снизить частоту дыхания и стабилизировать показатели оксигенации (рис. 1). 
Простота использования метода и «дружелюбный» интерфейс минимизируют потенциальную возможность ошибок в результате человеческого фактора. Основные противопоказания к ВПО включают нарушение сознания, высокий риск аспирации и обструкцию носовых ходов (травма, кровотечение, операция) [17, 20, 22]. Проведение ВПО может быть крайне опасным у пациентов с переломом основания черепа в связи с риском пневмоцефалии и менингита [17]. Кроме того, у пациентов с ХОБЛ при использовании ВПО с высокой фракцией кислорода возможно развитие респираторного ацидоза вследствие снижения частоты дыхательных движений и гиповентиляции [17, 22]. К специфическим, но достаточно редким проблемам проведения ВПО относят раздражение, дискомфорт и заложенность слизистой носоглотки, ощущение избыточного тепла, нарушения обоняния, дополнительный шумовой эффект и аэрофагию [17].
Определенную озабоченность вызывают вопросы инфекционной безопасности применения ВПО. В ходе ряда исследований оценена степень бактериального загрязнения окружающей среды на фоне использования высокопоточных носовых канюль по сравнению с обычной кислородной маской у пациентов с пневмонией.
Результаты показали, что использование ВПО не ассоциировалось с ростом контаминации окружающей среды грамотрицательными или иными бактериями [13, 23].
Преимущества стандартной кислородотерапии, высокопоточной назальной оксигенации и НИВЛ [22—24] суммированы в таблице. 
Высокопоточная оксигенация в лечении ОРДС
С момента первого описания ОРДС в 1967 г. прошло более полувека, однако данное состояние до сих пор является одной из ключевых проблем в отделении интенсивной терапии (ОИТ) и сопровождается высокой летальностью [25, 26]. Исход лечения ОРДС зависит от многих факторов, из них решающее значение имеют следующие: в какой стадии ОРДС начато лечение и насколько оно эффективно, какие еще органы и системы поражены, насколько устранима причина, вызвавшая ОРДС [5]. Большую роль играет и проведение респираторной поддержки, необходимой для обеспечения адекватного газообмена в легких, уменьшения работы дыхания, расправления спавшихся альвеол и поддержания нестабильных альвеол в раскрытом состоянии во время выдоха [5, 20, 25, 27].
Использование ВПО на начальных этапах лечения ОРДС
Возможность применения ВПО как стартовой терапии гипоксемической дыхательной недостаточности, в том числе ОРДС, активно обсуждается в медицинской литературе последних лет [28—30].
Однако стоит учитывать, что нарушение сознания, полиорганная недостаточность и шок являются противопоказаниями к использованию данного метода. Кроме того, одна из опасностей использования ВПО на начальных этапах лечения гипоксемической дыхательной недостаточности заключается в возможной задержке необходимой интубации трахеи, что, в свою очередь, может ухудшить результат лечения больного [29]. Наличие четких критериев для начала ИВЛ облегчает принятие такого решения.
Следует также иметь в виду, что, если в течение первого часа от начала ВПО у пациента с гипоксемической дыхательной недостаточностью не отмечено существенного клинического улучшения, риск дальнейшей неэффективности подобного лечения становится очень высоким [30]. В качестве факторов риска неэффективности ВПО при ОРДС отмечены отсутствие улучшения оксигенации, сохраняющееся тахипноэ, а также участие вспомогательной мускулатуры в акте дыхания [30]. В числе нереспираторных предикторов неудачного проведения ВПО, как правило, выделяют потребность в вазопрессорах, тахикардию, тяжесть исходного заболевания, а также полиорганную недостаточность [27—29]. Кроме того, ВПО становится неэффективной при большом объеме плеврального выпота, когда приоритетом в лечении дыхательной недостаточности становится плевральная пункция [31].
Имеющиеся на данный момент исследования относительно эффективности ВПО при гипоксемической дыхательной недостаточности противоречивы. Так, J. Frat и соавт. в своем многоцентровом исследовании, в которое включены преимущественно пациенты с пневмонией, показали, что ВПО не снижает риск интубации по сравнению с традиционной оксигенотерапией и НИВЛ (38, 47 и 50% соответственно, р=0,18) [24]. Это может объясняться ограниченными возможностями мобилизации альвеол у этой категории больных и отсутствием у них выраженных нарушений механики дыхания. Тем не менее в подгруппе пациентов с PaO2/FiO2, равном или менее 200 мм рт.ст., частота интубации трахеи и количество дней без ИВЛ к 28-м суткам исследования были статистически значимо ниже на фоне ВПО. Кроме того, ВПО сопровождалась большим комфортом, снижением выраженности дыхательной недостаточности и уменьшением тахипноэ по сравнению с НИВЛ и традиционной оксигенотерапией [24].
Анализируя результаты последних cтатей и обзоров, можно отметить, что применение ВПО у пациентов с дыхательной недостаточностью различного генеза снижает частоту интубации по сравнению со стандартной кислородотерапией и НИВЛ, не влияя при этом на длительность пребывания в ОИТ и летальность [29—32]. Так, использование ВПО снижает частоту интубации только по сравнению с традиционной оксигенотерапией, при этом степень комфорта пациентов при ВПО выше, чем при традиционной кислородотерапии и при НИВЛ [29]. Интересно отметить, что даже в тех исследованиях, в которых на фоне применения ВПО не получено статистически значимого снижения частоты интубации трахеи, авторы отмечают безопасность ВПО. Так, R. Parke и соавт. показали, что подавляющее большинство пациентов из группы ВПО хорошо переносили эту методику [22].
В настоящее время нет однозначного мнения относительно оптимального алгоритма выбора первичных настроек ВПО и последующей их коррекции у больных с дыхательной недостаточностью различного генеза. Рабочий алгоритм коррекции гипоксемии с использованием ВПО представлен на рис. 2. 
Как указано выше, аппараты для ВПО имеют простой и информативный интерфейс, при этом врач при проведении ВПО корректирует только три параметра: температуру, скорость потока и фракцию вдыхаемого кислорода (рис. 3). 
На данный момент нет четких рекомендаций по выбору температуры для согревания кислородно-воздушной смеси. В то же время показано, что применение более низкой температуры (31—34 °С) ассоциируется с большим комфортом для пациентов с ОРДС по сравнению с температурой 37 °C [33]. В любом случае подбор температуры носит строго индивидуальный характер, с учетом ощущений конкретного пациента.
Что касается устанавливаемой скорости потока, продемонстрировано, что в подгруппе пациентов с выраженной дыхательной недостаточностью больные лучше переносили максимальный поток 60 л/мин, при этом пациенты с ОРДС легкой степени не испытывали дискомфорта и при более низком потоке [33].
Таким образом, при ОРДС легкой степени тяжести допустимо начинать ВПО со скорости потока 20—30 л/мин с последующим увеличением последней в зависимости от показателей газообмена и состояния больного. В то же время у пациентов с более выраженной гипоксемией, вероятно, стоит начинать процедуру с более высоких цифр потока (50—60 л/мин) для развития максимального эффекта ПДКВ [34].
При выборе оптимальной фракции вдыхаемого кислорода у пациентов с ОРДС необходимо учитывать потенциальный вред от применения высокой концентрации кислорода, при этом следует подбирать минимальные значения, необходимые для достижения уровня SpO2 92—97% [27, 35]. Адекватной оксигенации следует добиваться прежде всего за счет увеличения скорости потока, а не фракции вдыхаемого кислорода. Подбор этих двух переменных должен строиться на принципах подбора ПДКВ и FiO2, описанных в рамках концепции респираторной поддержки у пациентов с ОРДС [5, 7, 27].
Ключевые принципы отлучения от ВПО аналогичны таковым при прекращении ИВЛ и подразумевают снижение FiO2 в условиях комплексного мониторинга оксигенации, постепенное снижение скорости потока кислородно-воздушной смеси на 5 л/мин каждые 6—8 часов; переход на традиционную кислородотерапию или спонтанное дыхание при скорости потока, равной или менее 20 л/мин, и FiO2менее 0,4 при адекватных показателях газообмена и в отсутствие признаков нарастания дыхательной недостаточности (см. рис. 2) [29].
Использование ВПО в ходе индукции анестезии у пациентов с ОРДС
В случае неэффективности стартовой консервативной терапии пациентам с ОРДС требуется обеспечение инвазивной вентиляции легких, при этом одним из критических моментов может стать сам процесс интубации трахеи с обеспечением седации и миорелаксации [36—40]. В этом плане перспективным видится направление по использованию ВПО на этапе преоксигенации. За счет поддержания высокого потока, возможности использования 100% кислорода, а также отсутствия необходимости прекращать оксигенацию во время ларингоскопии риск десатурации может быть минимизирован [41].
В настоящее время лишь в нескольких исследованиях проведено сравнение эффективности преоксигенации при помощи ВПО и лицевой маски у пациентов с гипоксемической дыхательной недостаточностью. Так, в исследовании М. Simon и соавт. у пациентов группы традиционной преоксигенации через минуту после индукции анестезии при переводе на ИВЛ у больных с гипоксемией наблюдалась более выраженная десатурация, чем у пациентов группы ВПО, у которых период ларингоскопии и интубации прошел без выраженного снижения уровня SpO2 [40].
В то же время ряд авторов уже продемонстрировали эффективность ВПО для преоксигенации у пациентов с интактными легкими. Так, А. Patel и S. Nourei показали, что преоксигенация при помощи ВПО позволяла избежать снижения уровня SpO2 менее 90%, несмотря на апноэ средней продолжительностью 17 мин [42]. Кроме того, применение ВПО во время экстренной интубации у пациентов ОИТ без признаков значимой гипоксемии (PaO2/FiO2 более 200 мм рт.ст.) ассоциируется с меньшей частотой десатурации (менее 90%), а также с меньшей частотой осложнений в ходе выполнения интубации трахеи [29].
Применение ВПО в период прекращения ИВЛ при ОРДС
Этап прекращения респираторной поддержки остается одним из ключевых аспектов ведения пациентов с ОРДС. Несмотря на улучшение состояния пациента и разрешающуюся дыхательную недостаточность, на этом этапе возможно развитие эпизодов гипоксемии и/или гиперкапнии, не менее клинически значимых, чем при манифестации ОРДС. В этих обстоятельствах нередко возникает потребность в реинтубации трахеи и продолжении инвазивной ИВЛ, особенно у пациентов высокого риска. Потребность в реинтубации остается серьезной проблемой отлучения от ИВЛ, встречающейся в 10—20% случаев ОРДС [43], и ассоциируется с ростом количества осложнений и повышением летальности (до 50% при необходимости реинтубации) [36]. В связи с этим, как показано в недавних исследованиях развития гипоксемической дыхательной недостаточности, в том числе у послеоперационных больных, необходимость поддержания адекватного газообмена после прекращения ИВЛ на фоне сохраняющейся гипергидратации легких требует дальнейшего поиска мер терапии, включая использование ВПО [30, 44].
В последнее время опубликован ряд работ, посвященных методам респираторной поддержки в постэкстубационном периоде. К таким методам относятся ВПО, НИВЛ и традиционная оксигенотерапия [34]. В недавнем рандомизированном исследовании G. Hernаndez и соавт. продемонстрировали, что применение ВПО по сравнению с традиционной оксигенотерапией способно снизить риск повторного перевода на ИВЛ у пациентов с клиникой дыхательной недостаточности в постэкстубационном периоде (4,9% по сравнению с 12,2%, р=0,004) [13].
Данное исследование включало широкий спектр пациентов с преобладанием больных хирургического профиля, с низким риском развития постэкстубационной острой дыхательной недостаточности. Более того, доля пациентов с ОРДС в этой работе невелика, что указывает на необходимость проведения дальнейших исследований. Эти же авторы оценили эффект ВПО по сравнению с НИВЛ у пациентов высокого риска в постэкстубационном периоде, показав схожее влияние обеих методик на частоту реинтубации при меньшем количестве осложнений, связанных с применением ВПО [45]. При этом одной из причин более выраженной гипоксемии у больных группы НИВЛ было раннее прекращение сеансов респираторной поддержки на фоне нарастающего дискомфорта у пациента [45].
S. Maggiore и соавт. в своем двуцентровом исследовании с участием пациентов смешанного профиля показали, что превентивное использование ВПО в раннем постэкстубационном периоде у больных с PaO2/FiO2 менее 300 мм рт.ст., находившихся на ИВЛ не менее 24 часов, сопровождается улучшением оксигенации, уменьшением дискомфорта, а также снижением частоты реинтубации по сравнению с применением кислородной маски с клапаном Вентури [46]. Следует отметить, что в эту работу включены преимущественно пациенты с пневмонией и с травмой, что указывает на необходимость проведения дальнейших исследований у больных с ОРДС.
После принятия решения о прекращении ИВЛ и экстубации целесообразно начинать ВПО с достаточно высокой скоростью потока газовой смеси (50—60 л/мин) с учетом индивидуальной переносимости. Фракция вдыхаемого кислорода также подбирается индивидуально для достижения адекватной оксигенации. При стабильном состоянии пациента показано постепенное снижение фракции вдыхаемого кислорода с последующим поэтапным снижением скорости потока кислородно-воздушной смеси (пошагово по 3—5 л/мин в течение 2—4 часов). В отсутствие признаков нарастания дыхательной недостаточности, а также при фракции вдыхаемого кислорода менее 40% и скорости потока не более 15—20 л/мин возможно прекращение ВПО [29].
Отсутствие эффекта от ВПО в раннем постэкстубационном периоде, как правило, является показанием для реинтубации и продолжения ИВЛ. Критерии повторного перевода на ИВЛ пациентов, получающих ВПО, не отличаются от стандартных. К ним относятся развитие тахипноэ, участие в акте дыхания вспомогательной мускулатуры, неспособность самостоятельно откашливать трахеальный секрет, уровень SpO2 менее 90%, а также нестабильность гемодинамики и ухудшение неврологического статуса [47].
Важным вопросом является и прекращение респираторной поддержки у пациентов с трахеостомой. Несмотря на снижение работы дыхания, риск инфекционных осложнений и невозможность в полной мере самостоятельно санировать мокроту усложняют их перевод на спонтанное дыхание.
Применение ВПО как переходного этапа между ИВЛ и спонтанным дыханием имеет определенные клинические перспективы, однако информация на эту тему ограничена и носит противоречивый характер.
Так, L. Corley и соавт., сравнивая эффекты высокопоточной и низкопоточной оксигенации у пациентов с трахеостомой и осложненным течением послеоперационного периода в кардиохирургии, отметили улучшение PaO2/FiO2 на фоне применения ВПО и связали это с возможностями более точного дозирования фракции вдыхаемого кислорода [19].
Напротив, Т. Stripoli и соавт. показали, что применение ВПО у больных с трахеостомой не имело существенных преимуществ по сравнению с традиционной кислородотерапией на этапе отлучения от респиратора [48]. Согласно данной работе, применение ВПО не сопровождалось улучшением нейрореспираторного драйва, снижением работы дыхания, а также улучшением газообмена по сравнению с пациентами контрольной группы.
Снижение преимуществ ВПО при дыхании через трахеостому может объясняться устранением одного из благоприятных эффектов методики при этом способе ее проведения — улучшения элиминации CO2 за счет вентиляции назофарингеального мертвого пространства. Ранее показано, что наличие трахеостомы само по себе позволяет снизить нейрореспираторный драйв на 30% за счет снижения сопротивления в дыхательных путях и анатомического мертвого пространства [49].
Заключение
Учитывая физиологические предпосылки, а также результаты клинических исследований, можно заключить, что высокопоточная оксигенация через назальные канюли претендует на место важного компонента респираторной поддержки пациентов с легким и умеренным острым респираторным дистресс-синдромом. Применение этой методики обосновано не только на начальных этапах ведения пациентов с острым респираторным дистресс-синдромом, но и на стадии прекращения искусственной вентиляции легких. Требуется проведение дальнейших крупных многоцентровых исследований по применению высокопоточной оксигенации.
Финансирование. Грант Президента Р.Ф. НШ—3927.2018.7.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.