Кортикальная миоклония что это симптомы
Миоклония
Пер. с англ. Н.Д. Фирсовой (2018)

В идеале устранение основной причины поможет справиться и с симптомами миоклонии. Если причина возникновения миоклонии неизвестна или не может быть устранена, то лечение будет направлено на снижение влияния миоклонии на качество жизни.
Симптомы
Люди с миоклонией часто такими словами описывают свои симптомы (рывки, толчки или судороги):
Когда обратиться к врачу
Если проявления миоклонии становятся частыми или постоянными, поговорите со своим врачом для дальнейшей оценки, правильной диагностики и лечения.
Причины
Миоклония может быть вызвана множеством причин. Врачи разделяют типы миоклонии на основании патологий, их вызвавших, что помогает подобрать лечение.
Физиологическая миоклония
Этот тип миоклонии встречается у здоровых людей и редко нуждается в лечении. Примеры:
Эссенциальная миоклония
Эссенциальная миоклония возникает сам по себе, обычно без каких-либо других симптомов и без связи с каким-либо основным заболеванием. Причина эссенциальной миоклонии часто необъяснима (идиопатическая) или, в некоторых случаях, кроется в наследственности.
Эпилептическая миоклония
Этот тип миоклонии является частью эпилептического расстройства.
Симптоматическая (вторичная) миоклония
Мышечные сокращения, возникающие в результате основного заболевания, в том числе:
Состояния нервной системы, которые приводят к вторичной миоклонии, включают:
Диагностика
Чтобы диагностировать миоклонию, врач изучит вашу историю болезни и симптомы и проведет медицинское обследование.
Чтобы определить причину миоклонии и исключить другие возможные причины вашего состояния, врач может порекомендовать несколько тестов, в том числе:
Электроэнцефалография (ЭЭГ)
Эта процедура регистрирует электрическую активность мозга и помогает определить, где в мозгу происходит миоклония. В ходе процедуры врачи прикрепляют маленькие электроды к коже головы. Вас могут попросить дышать глубоко и устойчиво, смотреть на яркий свет или слушать определенные звуки, поскольку эти действия могут выявить ненормальную электрическую активность.
Электромиография (ЭМГ)
Во время этой процедуры врачи надевают поверхностные электроды ЭМГ на несколько мышц, особенно на те, которые участвуют в непроизвольных сокращениях. Инструмент регистрирует электрическую активность мышц в покое и при сокращении, например, при сгибании руки. Эти сигналы помогают определить характер и происхождение миоклонии.
Магниторезонансная томография (МРТ)
МРТ-сканирование используется для обнаружения структурных проблем или опухолей в головном или спинном мозге, которые могут вызвать симптомы миоклонии. МРТ-сканирование использует магнитное поле и радиоволны для получения детальных изображений головного, спинного мозга и других областей организма.
Лабораторные тесты
Врач может предложить провести генетическое тестирование, чтобы помочь определить возможные причины миоклонии. Он может также проверить вашу кровь или мочу, чтобы определить:
Лечение
Лечение миоклонии наиболее эффективно тогда, когда удается найти обратимую причину, которую можно устранить – например, другое заболевание, лекарство или токсин.
Однако в большинстве случаев первопричину невозможно обнаружить или устранить, поэтому лечение направлено на ослабление симптомов миоклонии, особенно когда они приводят к инвалидности. Не существует лекарств, специально предназначенных для лечения миоклонии, но врачи позаимствовали некоторые из арсеналов для лечения других заболеваний, чтобы облегчить симптомы миоклонии. Для контроля симптомов может потребоваться более одного препарата.
Лекарственные препараты
Лекарства, которые врачи обычно назначают при миоклонии:
Другие консервативные методы лечения
Инъекции OnabotulinumtoxinA (Ботокс) могут быть полезны при лечении различных форм миоклонии, особенно когда поражена только одна область. Ботулинический токсин блокирует выброс химического вещества, которое вызывает мышечные сокращения.
Глубокая стимуляция мозга (DBS) была испытана у некоторых людей с миоклонией и другими нарушениями движения. Исследователи продолжают изучать возможности DBS в лечении миоклонии.
Хирургия
Если симптомы миоклонии вызваны опухолью или другим поражением головного или спинного мозга, может потребоваться операция. Людям с миоклонией, затрагивающей часть лица или уха, хирургия также может оказаться полезной.
Подготовка к встрече с врачом
Вероятно, сначала вы обсудите свои проблемы с вашим лечащим врачом, который затем направит вас к неврологу.
Поскольку консультации могут иметь ограничения по времени, а поговорить часто есть о чем, хорошей идеей будет тщательно подготовиться к беседе. Вот некоторая информация, которая поможет вам подготовиться.
Что вы можете сделать
Некоторые основные вопросы о миоклонии, которые стоит задать своему врачу:
В дополнение к вопросам, которые вы готовы задать своему врачу, не стесняйтесь задавать вопросы во время вашего визита в любое время, когда вы чего-то не понимаете.
Чего ожидать от врача?
Доктор, вероятно, задаст вам несколько вопросов. Если вы будете готовы ответить на них, это поможет вам сэкономить время на то, чтобы задать ему свои вопросы.
Врач может спросить:
Что такое юношеская миоклоническая эпилепсия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Агранович А. О., эпилептолога со стажем в 11 лет.
Определение болезни. Причины заболевания
Юношеской миоклонической эпилепсией (синдромом Янца) называют эпилептический синдром, который проявляется внезапными подёргиваниями в мышцах — миоклоническими приступами (от греч. «myos» — мышца, «klonos» — беспорядочное движение). Заболевание обычно развивается в подростковом возрасте.
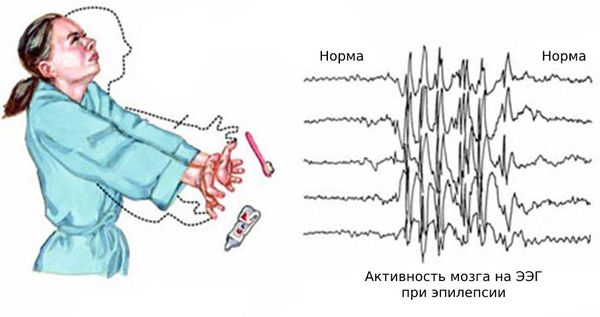
Подёргивания в первую очередь возникают в мышцах верхнего плечевого пояса и рук. Сначала пациенты не обращают на них внимания, но со временем эпизоды возникают всё чаще и ухудшают качество жизни. Например, во время приступов из рук могут выпадать предметы. В дальнейшем появляются подёргивания ног, из-за которых человек может упасть.
Нередко к этим эпизодам присоединяются генерализованные судорожные приступы — судороги возникают по всему телу и пациент теряет сознание. Также возникают абсансы — бессудорожные приступы с отключением сознания и амнезией на этот период. Как правило, частота генерализованных приступов невысокая: от одного за всю жизнь до раза в месяц. Подёргивания обычно случаются утром после пробуждения. Ярким провоцирующим фактором может стать недосыпание или вынужденное пробуждение. Также в трети случаев отмечается фотосенситивность — чувствительность к ритмическим вспышкам света.
Распространённость
Причины заболевания
Симптомы юношеской миоклонической эпилепсии
Чаще всего подёргивания возникают в верхнем плечевом поясе: мышцах рук и плеч с обоих сторон. Из-за этого пациенты нередко выпускают предметы из рук, например разбивают кружки и роняют зубные щётки. Однако возможны различные вариации миоклоний.
Приступы учащаются в утренние часы, особенно при недосыпе или вынужденном пробуждении.
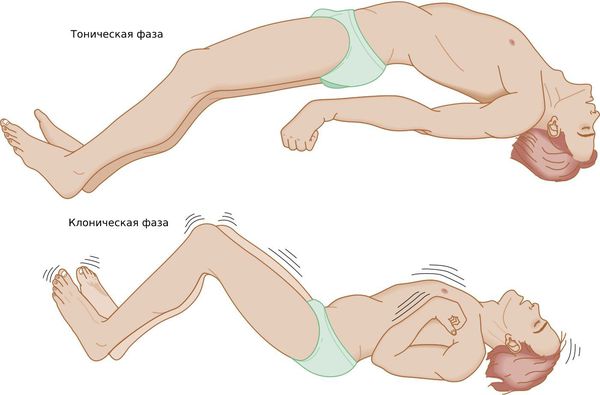
Генерализованный тонико-клонический приступ — состояние, при котором полностью отключается сознание. Приступ начинается с тонической фазы: напряжения в мышцах и специфического вскрикивания или хрипения. Руки полусогнуты и приподняты вверх или прижаты к телу. В этот момент из-за спазма дыхательной мускулатуры меняется цвет лица: оно синеет или сереет.
Далее развивается клоническая фаза, которая проявляется ритмичными подёргиваниями в конечностях. Она завершается полным мышечным расслаблением.
Патогенез юношеской миоклонической эпилепсии
Мозг человека состоит из двух основных типов клеток: нейронов и глии. Нейроны — это электрически возбудимые клетки, которые обрабатывают, хранят и передают информацию с помощью электрических и химических сигналов. Глиальные клетки играют в этом процессе вспомогательную роль.
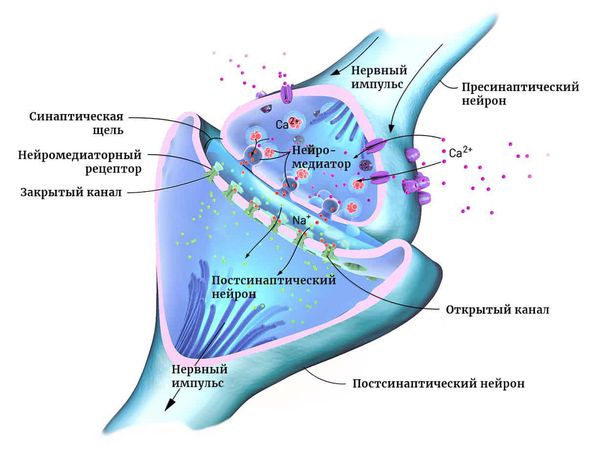
Нейроны могут соединяться друг с другом и образовывать нервные сети. В пределах одного нейрона и его отростков информация передаётся в виде электрического возбуждения. В синапсе (месте контакта между нервными клетками) оно приводит к выделению различных химических веществ — нейромедиаторов.
Нейромедиатор взаимодействует с рецепторами на мембране следующего нейрона. В результате в нём возникает электрическое возбуждение. Или не возникает — это зависит от конкретного нейромедиатора, активного в данный момент.
В нервных сетях между возбуждением и торможением работы нейронов поддерживается постоянный баланс. При сдвиге равновесия в сторону возбуждения происходит эпилептический приступ.
Классификация и стадии развития юношеской миоклонической эпилепсии
В 2017 году Международная лига борьбы с эпилепсией (ILAE) обновила классификацию заболевания, выделив четыре уровня диагностики:
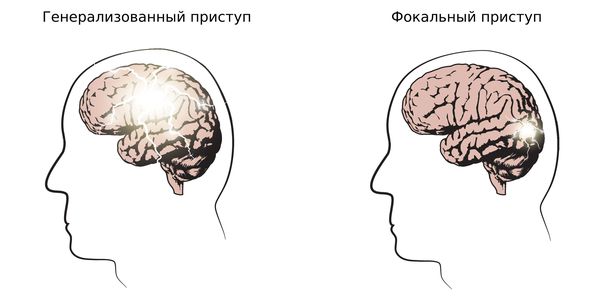
1. Определить тип приступа: фокальный (возникающий из одного очага), генерализованный и с неизвестным началом. Миоклонические, тонико-клонические приступы и абсансы относятся к генерализованным приступам.
2. Установить тип эпилепсии: фокальная, генерализованная, сочетанная (фокальная + генерализованная) и неизвестная. Юношеская миоклоническая эпилепсия относится к генерализованной эпилепсии.
4. Выявить причины заболевания: генетические, структурные, метаболические, иммунные, инфекционные и с неизвестной этиологией. Юношеская миоклоническая эпилепсия в большинстве случаев вызвана генетическими факторами.
Классификация юношеской миоклонической эпилепсии проводится в зависимости от течения заболевания. Главный критерий — это наличие миоклонических приступов. Также выделяют варианты течения с добавлением генерализованных судорожных приступов и/или абсансов.
Осложнения юношеской миоклонической эпилепсии
Пациенты часто не обращают внимания на патологические сокращения мышц, поэтому к неврологу и эпилептологу больной зачастую обращается после появления генерализованных тонико-клонических приступов. В результате противоэпилептические препараты назначают с опозданием. На фоне этого приступы могут учащаться и угрожать здоровью и жизни пациента травмами и утоплениями.
Диагностика юношеской миоклонической эпилепсии
Основной диагностический критерий заболевания — это наличие миоклонических приступов.
Сбор анамнеза
На приёме врач спрашивает о необычных внезапных состояниях:
Пациенты могут не обращать внимания на такие симптомы и считать их своей особенностью. Абсансы и генерализованные тонико-клонические приступы с потерей сознания, особенно во сне, они могут и вовсе забывать. Поэтому при сборе анамнеза важно выяснить обстоятельства приступа не только у самих пациентов, но и у родственников и очевидцев.
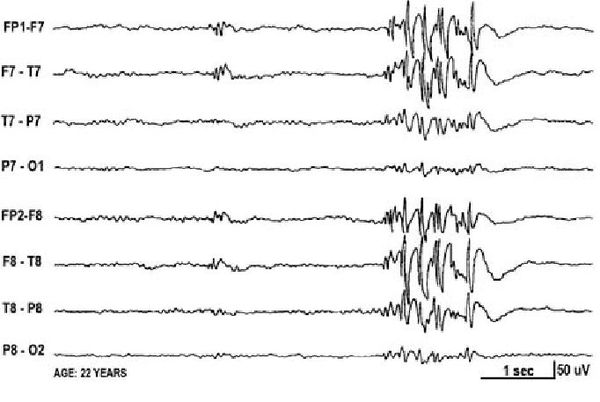
Электроэнцефалограмма (ЭЭГ)
Основным способом диагностики эпилепсии является электроэнцефалограмма — метод исследования, при котором регистрируется суммарная электрическая активность клеток коры головного мозга.
Сейчас диагноз «эпилепсия» устанавливают с помощью длительного видео-ЭЭГ мониторинга — электроэнцефалограмма записывается параллельно с одной или несколькими видеокамерами, датчиком ЭКГ и при необходимости дополнительным контролем мышечной активности, частоты и глубины дыхания.
Основной фон биоэлектрической активности при юношеской миоклонической эпилепсии, как правило, соответствует возрастной норме. Патологическая активность проявляется короткими и генерализованными разрядами полиспайков (островолновых комплексов), которые регистрируются при миоклонических вздрагиваниях и полипик-волновыми комплексами между приступами.
Эпилептическая фотосенситивность — это предрасположенность к приступам под влиянием света. Может протекать бессимптомно или проявляться эпилептическими приступами под воздействием провоцирующих факторов: видеоигр, работы за компьютером, просмотра телевизора, мигающего освещения в ночных клубах и света природного происхождения.
Интеллект и неврологический статус при заболевании находятся в норме. Выражена эмоциональная неустойчивость и признаки невротического развития личности: резкая смена настроения, вспыльчивость и повышенная тревожность
Лечение юношеской миоклонической эпилепсии
Образ жизни
Антиэпилептические препараты
Ранее лидерами в лечении юношеской миоклонической эпилепсии являлись препараты вальпроевой кислоты. Они эффективны для прекращения приступов, но вызывают много побочных эффектов:
Помимо перечисленных препаратов, могут применяться «Топирамат», «Зонисамид», «Перампанел» и «Фенобарбитал».
Прогноз. Профилактика
Эффективность АЭП в предотвращении приступов достигает 90 %. При отмене терапии часто возникают рецидивы, поэтому потребуется длительный приём препаратов, иногда пожизненный.
Качество жизни значительно ухудшается при частых миоклонических и генерализованных тонико-клонических приступах, при которых пациенты рискуют получить травмы.
Профилактика
Особое внимание стоит уделить образу и режиму жизни пациента. Самыми мощными провоцирующими факторами являются недосыпание и злоупотребление алкоголем. А учитывая, что дебют заболевания приходится на подростковый возраст, молодые люди часто нарушают эти рекомендации, особенно в студенческие годы.
Пациент, у которого выявили фотосенситивность, предрасположен к приступам под воздействием мерцающего света. Поэтому им необходимо ограничить просмотр телевизора и работу за компьютером, исключить видеоигры и избегать посещения ночных клубов.
У всех пациентов с эпилепсией имеются определённые социальные ограничения: они не могут работать в некоторых сферах, водить автомобиль и нести военную службу. Все они определяются индивидуально соответствующими комиссиями.
Кортикальная миоклония что это симптомы
Экстрапирамидные гиперкинезы относятся к числу тех расстройств, которые не столько угрожают жизни, сколько разрушают ее, значительно ограничивая функциональные возможности пациентов, приводя к их психологической и социальной изоляции. Длительное время лечение экстрапирамидных гиперкинезов вызывало лишь разочарование как самих пациентов, так и врачей. Но в последние десятилетия ситуация начала меняться. Появились более четкие критерии диагностики различных вариантов экстрапирамидных гиперкинезов, существенно расширились возможности лечения – как за счет появления новых методов, так и за счет более рационального применения ранее существовавших. И если мы до сих пор в подавляющем большинстве случаев не можем кардинально излечить гиперкинез, то по крайней мере способны существенно улучшить качество жизни многих пациентов. Ниже рассмотрены современные подходы к диагностике и лечению наиболее частых вариантов экстрапирамидных гиперкинезов.
Определение и классификация экстрапирамидных гиперкинезов
Экстрапирамидные гиперкинезы (син. – дискинезии) – непроизвольные (насильственные) избыточные движения, которые связаны с поражением базальных ганглиев и связанных с ними структур, условно объединяемых в экстрапирамидную систему [12]. Экстрапирамидные гиперкинезы следует отличать от более редких периферических гиперкинезов, связанных с поражением или дисфункцией периферических нервов (например, лицевого гемиспазма, синдрома «болезненных ног (рук) – движущихся пальцев», тетании и др.), а также от психогенных гиперкинезов, являющихся соматическим выражением того или иного психического заболевания.
К основным экстрапирамидным гиперкинезам относят тремор, дистонию, хорею, атетоз, баллизм, тики, миоклонию, акатизию [10]. Традиционно считается, что каждый гиперкинез имеет свой неповторимый двигательный рисунок, в основе которого лежит уникальный патофизиологический механизм. Отчасти это действительно так. Тем не менее опыт работы позволяет нам говорить не столько об отдельных, дискретных синдромах, сколько о едином спектре (континууме) синдромов, в котором наряду с чистыми формами широко представлены переходные или комбинированные формы, что существенно затрудняет их синдромальную диагностику и выбор правильного лечения.
Справедливо мнение, что гиперкинезы сопротивляются жесткой вербальной категоризации и их значительно проще узнать, чем описать. Ситуация усложняется еще и тем, что один и тот же гиперкинез в разных регионах тела может выглядеть по-разному. В связи с этим распознавание гиперкинезов, особенно в сложных или переходных случаях, невозможно без выделения ограниченного числа ключевых признаков. По нашему мнению, особенно важное значение имеют 3 признака: двигательный рисунок, временной рисунок, характер возникновения.
По двигательному рисунку гиперкинезы можно разделить на 3 основные группы:
По временному рисунку гиперкинезы можно разделить на 2 группы:
По характеру возникновения непроизвольные гиперкинезы можно разделить на 4 основные группы:
Таблица 1. Дифференциальная диагностика основных форм экстрапирамидных и психогенных гиперкинезов
| Гиперкинез | Произвольность движения* | Предшествующий императивный позыв | Влияние отвлечения внимания | Возможность волевого подавления | Влияние произвольного движения |
| Тремор | Непроизвольное | – | Не влияет или усиливает | – | Усиливает или ослабляет |
| Дистония | Непроизвольное | – | Не влияет или усиливает | ± | Усиливает |
| Хорея | Непроизвольное | _ | Не влияет или усиливает | ± | Вариабельно |
| Тики | Непроизвольное или произвольное | + | Ослабляет | + | Обычно ослабляет |
| Миоклония | Непроизвольное | – | Не влияет или усиливает | — | Усиливает |
| Акатизия | Произвольное | + | Ослабляет | + | Ослабляет |
| Психогенный гиперкинез | Непроизвольное | ± | Ослабляет | – | Ослабляет |
* По субъективному восприятию пациента.
Феноменологические особенности основных форм экстрапирамидных гиперкинезов в сравнении с психогенными гиперкинезами представлены в таблице 1.
Общие принципы диагностики экстрапирамидных гиперкинезов
Распознавание того или иного экстрапирамидного синдрома – лишь отправная точка сложной диагностической работы, итогом которой может быть лишь установление нозологического диагноза (см. рис. 1).
С нозологической точки зрения в рамках любого экстрапирамидного гиперкинеза могут быть выделены 3 основных формы:
Рис. 1. Три этапа диагностики экстрапирамидного синдрома.
Большинство случаев экстрапирамидных гиперкинезов имеют первичный (идиопатический) характер, однако их диагностика требует исключения других, прежде всего вторичных, форм гиперкинезов, особенно связанных с курабельными заболеваниями (такими как опухоли или эндокринопатии), а также курабельных форм мультисистемных дегенераций, в первую очередь гепатолентикулярной дегенерации (болезни Вильсона–Коновалова). Подобные случаи в клинической практике встречаются редко, но именно они должны быть исключены в первую очередь. Исключение вторичной природы гиперкинеза может потребовать дополнительного инструментального либо лабораторного исследования. Любой экстрапирамидный синдром, впервые проявившийся в возрасте до 50 лет, служит основанием для исключения гепатолентикулярной дегенерации (для этого требуется как минимум анализ крови на церулоплазмин и исследование роговицы при помощи щелевой лампы с целью обнаружения пигментного кольца Кайзера– Флейшера) [11]. Данные КТ и МРТ головного мозга особенно важны для диагностики вторичных форм, вызванных сосудистым поражением мозга, опухолью и др., однако они могут быть важным дополнительным признаком и при некоторых нейродегенеративных заболеваниях (например, при гепатолентикулярной дегенерации или болезни Гентингтона).
Наконец, в каждом случае гиперкинеза следует подумать и о возможности его психогенной природы. В прошлом большинство случаев гиперкинезов нередко рассматривались как психогенные расстройства. Этому способствовали вариабельность и динамичность проявлений экстрапирамидных гиперкинезов, их зависимость от движений, позы, эмоционального состояния пациента, нередкое присутствие у пациентов с первичными формами гиперкинезов аффективных расстройств. В настоящее время очевидно, что психогенные гиперкинезы встречаются редко, но тем важнее их своевременное выявление, позволяющее проводить целенаправленное лечение и как минимум избавляющее пациента от ненужной, а иногда и опасной для него терапии. В пользу психогенной природы гиперкинеза могут свидетельствовать: острое начало, последующее волнообразное течение с периодами длительных спонтанных ремиссий; непостоянство гиперкинеза, причудливость его рисунка, обычно не соответствующего характерным формам экстрапирамидных гиперкинезов; ослабление при отвлечении внимания, стойкая реакция на плацебо, полная резистентность к стандартной терапии; наличие других псевдоневрологических симптомов с феноменом селективной несостоятельности, выраженных аффективных расстройств с множественными соматоформными жалобами, наличие рентной ситуации (в которой больной извлекает моральную или (реже) материальную выгоду из своего заболевания) и т.д. [1].
Ниже более подробно рассмотрены подходы к диагностике и лечению 4 наиболее частых форм экстрапирамидных гиперкинезов: тремора, дистонии, хореи и тиков.
Тремор
Тремор (дрожание) – самый частый экстрапирамидный гиперкинез, характеризующийся непроизвольными ритмичными колебательными движениями части тела (чаще всего конечностей и головы) или всего тела, которые упорядочены во времени и пространстве. Феноменологически выделяют 2 основных типа тремора: тремор покоя и тремор действия (акционный тремор). Тремор покоя характерен для синдрома паркинсонизма и прежде всего – болезни Паркинсона.
Тремор действия подразделяют на постуральный, возникающий при удержании определенной позы (например, вытянутых рук), кинетический, возникающий при движении (в том числе при приближении к цели – так называемый интенционный тремор), изометрический, возникающий при изометрическом мышечном сокращении (например, при сжимании кисти в кулак). К особым формам тремора относятся ортостатический тремор, возникающий при переходе в вертикальное положение и стоянии, а также селективный кинетический тремор, возникающий только при определенных движениях (например, при письме – писчий тремор).
Основной формой первичного тремора является эссенциальный тремор (ЭТ), представляющий собой самостоятельное заболевание, преимущественно проявляющееся постурально-кинетическим тремором рук, реже – головы, голосовых связок, ног, туловища. ЭТ выявляется не менее чем у 4% лиц старше 40 лет. Более чем в половине случаев заболевание носит семейный характер. Анализ семейных случаев указывает на аутосомно-доминантный тип наследования, однако установить генетический дефект удалось лишь в отдельных случаях [4]. Не исключено, что спорадические случаи, как правило, проявляющиеся в более позднем возрасте (часто после 60 лет), носят мультифакторный характер и связаны как с генетическим дефектом, так и с воздействием неидентифицированных внешних факторов.
ЭТ начинается исподволь, обычно с постурального дрожания в руках, которое может быть как симметричным, так и асимметричным. Со временем амплитуда и распространенность тремора нарастают. Резко выраженный постуральный тремор может сохраняться и в покое. Помимо косметического дефекта тремор может вызывать нарушение функции верхних конечностей: больным все труднее принимать пищу, писать, играть на музыкальных инструментах, выполнять другие тонкие действия.
Другие неврологические проявления обычно отсутствуют, но примерно у трети больных выявляются минимальные проявления мозжечковой атаксии (например, нарушения тандемной ходьбы), минимальная гипомимия, иногда миоклония и фокальная дистония. У больных с ЭТ чаще, чем в среднем по популяции, наблюдаются артериальная гипертензия, нейросенсорная тугоухость, когнитивные нарушения.
Как особые варианты ЭТ рассматривают первичный ортостатический тремор, возникающий в ногах при стоянии, изолированный тремор головы, а также тремор, появляющийся при письме (писчий тремор). Последний занимает промежуточное положение между тремором и дистонией. Изолированный тремор головы, возникающий на фоне ее дистонической позы, как правило, представляет собой дистонический тремор, являясь вариантом фокальной дистонии (см. ниже).
ЭТ необходимо также дифференцировать с усиленным физиологическим тремором (возникающим при волнении, утомлении, под действием холода и некоторых лекарственных средств, при абстинентном синдроме, тиреотоксикозе, гипогликемии, интоксикациях), мозжечковым (преимущественно интенционным) тремором, тремором Холмса (асимметричным крупноразмашистым дрожанием, представляющим собой комбинацию постурального и кинетического тремора с тремором покоя и возникающим при очаговых поражениях среднего мозга или таламуса), тремором при полиневропатиях [3].
До сих пор в клинической практике возникают большие сложности в дифференциальной диагностике ЭТ с болезнью Паркинсона. Для последней, в отличие от ЭТ, характерны присутствие других симптомов паркинсонизма (прежде всего выраженной гипокинезии), более быстрое прогрессирование, выраженная асимметрия проявлений, преобладание тремора покоя, отсутствие тремора головы, иная последовательность вовлечения конечностей (рука – ипсилатеральная нога – контралатеральные конечности, при ЭТ: рука – контралатеральная рука – ноги), лечебный эффект противопаркинсонических средств.
К сожалению, в настоящее время возможностей предупредить или хотя бы замедлить прогрессирование заболевания не существует. Тем не менее значительная часть пациентов с ЭТ не нуждается ни в каком ином лечении, кроме рациональной психотерапии, заключающейся в разъяснении доброкачественной природы заболевания. Если тремор существенно нарушает функцию рук, его можно уменьшить почти у 2/3 больных с помощью средств первого ряда – бета-блокаторов (пропранолол, 60–360 мг/сут.) и примидона (гексамидин, 125–500 мг/сут.). Выбор препарата производят исходя из риска побочного действия, сопутствующих заболеваний и индивидуальных особенностей пациентов. У молодых больных, а также при артериальной гипертензии чаще применяют бета-блокаторы, у пожилых пациентов, особенно чувствительных к побочному действию пропранолола на сердечно-сосудистую систему, более целесообразен прием примидона, который к тому же в большинстве случаев достаточно принимать всего 1 раз в сутки – перед сном [5]. Чтобы улучшить переносимость примидона, его терапевтическая доза подбирается путем медленного титрования. После достижения эффективной дозы побочные действия наблюдаются редко. В резистентных случаях возможна комбинация 2 препаратов первого ряда либо их комбинация с препаратами второго ряда, к которым относятся клоназепам и алпразолам (особенно эффективны при кинетическом треморе и треморе головы), антагонисты кальция (нимодипин), габапентин, топирамат и теофиллин. После подбора эффективного средства или их комбинации обычно необходим их длительный прием в течение многих лет. При треморе головы и голосовых связок единственный метод, дающий гарантированный эффект, – регулярные инъекции ботулотоксина. В наиболее резистентных случаях прибегают к клозапину или проводят стереотаксическое нейрохирургическое вмешательство на таламусе.
Дистония
Дистония – синдром, характеризующийся медленными (тоническими) или повторяющимися быстрыми (клонико-тоническими) движениями, вызывающими вращение (отсюда термин «торсионная дистония» – от лат. torsio – вращение, скручивание), сгибание или разгибание туловища и конечностей с формированием патологических поз. В отличие от более быстрого и хаотичного хореического гиперкинеза (см. ниже), рисунок дистонического гиперкинеза более стереотипен и упорядочен [1, 2]. Дистонические феномены многообразны и включают преходящие дистонические спазмы, которые иногда бывают столь быстрыми, что напоминают миоклонию (при «клонической» форме дистонии) или относительно ритмичный дистонический тремор, обычно усиливающийся при попытке больного преодолеть дистоническую позу.
Характерная особенность дистонического гиперкинеза – возникновение или усиление при произвольных движениях. Дистоническая поза первоначально имеет преходящий характер, возникая лишь при определенном движении, но постепенно становится постоянной, сохраняясь и в покое. Эта эволюция дистонии весьма характерна наряду с другими проявлениями динамичности гиперкинеза, такими как улучшение после сна, влияние корригирующих жестов и изменений позы (дистония часто усиливается в вертикальном положении и уменьшается в горизонтальном), наличие парадоксальной кинезии (уменьшение гиперкинеза при изменении привычного двигательного стереотипа), колебания симптоматики день ото дня, влияние эмоционального состояния. Признаки динамичности гиперкинеза, включая возможность кратковременной произвольной коррекции патологической позы, позволяют отличить дистонию от заболеваний скелетно-мышечной системы, вызывающих более фиксированные изменения позы (псевдодистонии).
По распространенности гиперкинеза выделяют:
Почти 90% случаев составляет первичная (идиопатическая) дистония, которая проявляется только дистоническим гиперкинезом и имеет наследственный характер, но бывает представлена как семейными, так и спорадическими случаями. При раннем начале (до 15 лет) дистония обычно имеет четко наследственный характер, часто начинается с одной ноги, а затем генерализуется, вовлекая туловище. При более позднем начале (после 21 года) дистония чаще представлена спорадическими случаями, первично вовлекает мышцы верхней части тела, а в последующем чаще остается фокальной. В классическом варианте она наследуется по аутосомно-доминантному типу и связана с мутацией в локусе DYT1 на 9-й хромосоме, кодирующем белок торсин А. Реже встречаются другие варианты генерализованной дистонии с наследованием по аутосомно-рецессивному или рецессивному, сцепленному с Х-хромосомой типу [4].
Фокальные формы встречаются примерно в 10 раз чаще, чем генерализованные. К числу частых фокальных вариантов относятся краниальная дистония, включающая блефароспазм и оромандибулярную (орофациальную) дистонию, и цервикальная дистония. Сочетание орофациальной дистонии с гиперкинезом других мышц лица, в том числе с блефароспазмом и дистонией мышц шеи (сегментарная краниоцервикальная дистония), обозна чают как синдром Мейжа.
В некоторых семейных случаях сегментарной краниоцервикальной дистонии, при которой наблюдается сочетание спастической кривошеи с блефароспазмом и орофациальной дистонией, выявлен генетический дефект (ген DYT6 на 8-й хромосоме). В семейных случаях чисто цервикальной дистонии выявлен патологический ген DYT7 на 18-й хромосоме. Однако причина большинства случаев цервикальной дистонии остается неясной (идиопатическая цервикальная дистония) [4].
В последние годы выделена группа заболеваний, условно обозначаемых как «дистония-плюс», при которых дистонический гиперкинез сопровождается другими экстрапирамидными расстройствами, в частности симптомами паркинсонизма (дистония/дистония-паркинсонизм, чувствительная к L-ДОФА, или ДОФА-зависимая дистония, или болезнь Сегавы) или миоклонией (миоклоническая дистония). Вторичная (симптоматическая) дистония составляет не более 5–10% случаев дистонии. Чаще всего она возникает после очагового повреждения базальных ганглиев или таламуса (например, при инсульте), развиваясь спустя несколько месяцев, иногда на фоне регресса гемипареза («отставленная» дистония). Дистония конечности изредка возникает на фоне тяжелой рефлекторной симпатической дистрофии, возникшей после периферической травмы. Важнейшей причиной вторичной дистонии служит воздействие лекарственных средств, прежде всего нейролептиков, метоклопрамида, препаратов леводопы.
Наиболее курабельны ДОФА-зависимые формы дистонии (например, болезнь Сегавы), при которых эффективны малые дозы препаратов леводопы (суточную дозу – от 0,25 до 1,5 таблеток Накома или Мадопара 250 – назначают в 1 или 2 приема). Поскольку ДОФА-зависимую дистонию не всегда удается дифференцировать клинически, препараты леводопы целесообразно испробовать во всех случаях генерализованной дистонии, развившейся в детском и юношеском возрасте.
В целом при генерализованной дистонии можно рекомендовать следующую последовательность назначения препаратов: 1) препараты леводопы (в детском и юношеском возрасте); 2) холинолитики (обычно в высокой дозе – например, до 10 мг акинетона в сутки); 3) баклофен; 4) клоназепам и другие бензодиазепины); 5) карбамазепин (финлепсин); 6) препараты, истощающие запасы дофамина в пресинаптических депо (резерпин, тетрабеназин); 7) нейролептики – блокаторы дофаминовых рецепторов (галоперидол, рисперидон, тиапридал, фторфеназин); 8) комбинация из перечисленных средств (например, холинолитика с клоназепамом и баклофеном).
При генерализованных и сегментарных вариантах первичной дистонии, не чувствительной к леводопе, наиболее гарантированный эффект обеспечивает глубинная стимуляция медиального сегмента бледного шара. Условием эффективности вмешательства является его своевременность – до развития стойких деформаций и контрактур.
Наиболее эффективный метод лечения фокальных дистоний – инъекции ботулотоксина (ботокса или диспорта) в мышцы, вовлеченные в гиперкинез. Ботулотоксин вызывает частичный парез этих мышц и тем самым у подавляющего большинства больных устраняет гиперкинез на 3–6 мес., после чего инъекцию приходится повторять [7]. Возможности фармакотерапии ограниченны. При цервикальной дистонии эффекта иногда удается добиться с помощью клоназепама, баклофена или нейролептиков. При блефароспазме более эффективны клоназепам и холинолитики, при оромандибулярной дистонии – баклофен и холинолитики, при писчем спазме – холинолитики. В части случаев некоторого улучшения, скорее субъективного характера, можно добиться путем воздействия на мышцы, вовлеченные в гиперкинез, при помощи физиотерапевтических процедур, метода биологической обратной связи или гимнастики. В резистентных случаях прибегают к периферической денервации мышц.
Хорея
Хорея характеризуется непрерывным потоком быстрых, хаотичных, нерегулярных по времени и амплитуде мультифокальных движений. Гиперкинез чаще всего вовлекает дистальные отделы конечностей, мимические мышцы, иногда мышцы глотки, гортани, туловища. Насильственные движения напоминают гримасничание, кривляния, нарочитые ужимки, танцевальные движения (греч. choreia – пляска) [8].
К наиболее частым формам хореи относится болезнь Гентингтона (БГ) – наследственное заболевание, передающееся по аутосомно-доминантному типу, связанное с прогрессирующей дегенерацией нейронов подкорковых ядер и коры и проявляющееся главным образом сочетанием хореи с деменцией [4]. Тем не менее хорея – не единственное, а в ряде случаев и не основное проявление заболевания, поэтому термин «болезнь Гентингтона» предпочтительнее, чем термин «хорея Гентингтона». Генетический дефект при БГ выявлен на 4-й хромосоме и заключается в увеличении количества повторов («экспансии») одного из тринуклеотидных фрагментов в зоне ДНК, кодирующей белок гентингтин. В конечном итоге это предопределяет особую уязвимость и преждевременную гибель определенных популяций нейронов полосатого тела, прежде всего хвостатого ядра.
БГ обычно проявляется на 4–5-м десятилетии жизни и в последующем неуклонно прогрессирует. Хорея обычно начинается с дистальных отделов конечностей, затем постепенно генерализуется и нарушает произвольные движения. Больные не могут долго держать высунутым язык или сжимать кисть в кулак, походка становится неустойчивой, «танцующей», иногда замедленной, напряженной. Со временем непроизвольные движения все отчетливее приобретают дистонический характер, присоединяются гипокинезия и ригидность, оживление рефлексов, грубая постуральная неустойчивость, приводящая к частым падениям. Уже на ранней стадии часто наблюдается выраженная дизартрия с замедленной аритмичной речью; дисфагия появляется на более поздней стадии и бывает причиной аспирации, ведущей к асфиксии или пневмонии. Психические расстройства многообразны и бывают представлены нарастающим когнитивным дефицитом, депрессией с нередкими суицидальными попытками, навязчивыми и фобическими расстройствами, психотическими нарушениями [12].
Малая хорея, являющаяся осложнением ревматизма и в прошлом составляющая значительную часть случаев вторичной хореи, в последние годы возникает исключительно редко. В связи с этим при возникновении хореи в детском или юношеском возрасте важно исключать иные причины синдрома: сосудистую хорею, системную красную волчанку, антифосфолипидный синдром и др. У пожилых хорея чаще бывает вызвана полицитемией, заболеваниями печени, последствиями инсульта.
При умеренном гиперкинезе с нейролептиками могут конкурировать средства, блокирующие глутаматергические рецепторы (например, амантадин или мемантин), некоторые антиконвульсанты (например, топирамат), а также симпатолитики (например, резерпин), истощающие запасы катехоламинов (в том числе дофамина) в депо пресинаптических терминалей. В некоторых случаях возможна комбинация лечебных средств, в частности нейролептика с антиглутаматергическими средствами, антиконвульсантами и симпатолитиками. Согласно некоторым данным, длительный прием коэнзима Q10 и мемантина может несколько замедлять прогрессирование БГ. Важно с помощью нейролептиков и антидепрессантов корригировать сопутствующие психические расстройства, прежде всего депрессию, вспышки агрессии и неконтролируемого поведения [10].
При малой хорее средством выбора являются препараты вальпроевой кислоты и карбамазепины; только в том случае, если с их помощью не удается контролировать гиперкинез, назначают нейролептики в минимальной эффективной дозе. Кроме того, во избежание повторяющихся приступов ревматической лихорадки и развития порока сердца показана длительная пенициллинотерапия [12].
Тики представляют собой повторяющиеся отрывистые неритмичные движения, которые одномоментно вовлекают отдельные мышцы, группу мышц или часть тела. Тики возникают спонтанно на фоне нормальной двигательной активности и напоминают фрагменты целенаправленных движений.
В отличие от многих других гиперкинезов, больной может волевым усилием на определенное время (30–60 с) подавить тики, но обычно – ценой быстро возрастающего внутреннего напряжения, которое неизбежно прорывается, вызывая кратковременную тикозную «бурю». Тикам может предшествовать ощущение непреодолимой, императивной потребности совершить движение, создающее иллюзию произвольности тика. Как правило, тики стереотипны и возникают в строго определенных у данного больного частях тела. Каждый больной имеет свой индивидуальный «репертуар» тиков, который меняется со временем. В отличие от других экстрапирамидных гиперкинезов, тики сохраняются во сне [6].
Выделяют моторные, вокальные (фонические) и сенсорные тики; каждые из них делятся на простые и сложные. К простым моторным тикам относят моргание, зажмуривание, подергивание головой, пожимание плечами, втягивание живота и др., к сложным моторным тикам – подпрыгивание, биение себя в грудь, эхопраксию (повторение жестов), копропраксию (воспроизведение неприличных жестов) и др. Простые моторные тики могут быть быстрыми, внезапными (клоническими) или более медленными и стойкими (дистоническими); например, к клоническим тикам относят моргание, а к дистоническим – зажмуривание (блефароспазм), окулогирные кризы, дистонические подергивания в области шеи, плеча, брюшных мышц. Простые вокальные тики включают покашливание, фырканье, похрюкивание, свист; сложные вокальные – эхолалию (повторение чужих слов), копролалию (произнесение непристойных слов), палилалию (повторение произнесенных самим больным слов или звуков). Сенсорные тики представляют собой кратковременные весьма неприятные ощущения, императивно вынуждающие больного совершить движение. Они могут ощущаться в определенной части тела (например, в плече, кисти, животе или горле) и вынуждать больного совершать движение именно в этом регионе. По распространенности тики могут быть локальными (чаще в области лица, шеи, плечевого пояса), множественными или генерализованными.
Чаще всего тики имеют первичный характер, т.е. не связаны с какимлибо иным заболеванием, не сопровождаются другими двигательными синдромами, начинаются в детском и подростковом возрасте и связаны с нарушением созревания связей между базальными ганглиями, лимбической системой и лобной корой. Мальчики страдают в 2–4 раза чаще девочек [12].
Первичные тики условно подразделяют на: 1) транзиторные моторные и/или вокальные тики (продолжающиеся менее 1 года); 2) хронические моторные или вокальные тики (сохраняющиеся без длительных ремиссий более 1 года); 3) синдром Туретта (СТ), представляющий собой сочетание хронических моторных и вокальных тиков (не обязательно в одно и то же время). Есть основания полагать, что хронические моторные и вокальные тики и СТ, а возможно, и транзиторные тики могут быть проявлением одного и того же генетического дефекта, наследующегося по аутосомно-доминантному типу. Они встречаются у членов одной семьи и, следовательно, могут быть проявлением одного и того же генетического дефекта. В то же время различия в выраженности гиперкинеза даже у однояйцовых близнецов указывают на важную роль внешних факторов, в частности, действующих в перинатальном периоде [6]. СТ выявляется у 3% школьников.
Для СТ характерно волнообразное течение с периодами усиления и ослаб ления гиперкинеза, иногда с длительными спонтанными ремиссиями. Как правило, тики у конкретных больных возникают в строго определенных частях тела. Обычно тики максимально выражены в подростковом (предпубертатном) возрасте, а затем уменьшаются в юношеском и молодом возрасте. С наступлением зрелого возраста примерно в трети случаев тики исчезают, у трети больных они значительно уменьшаются, а у оставшейся трети сохраняются в течение всей жизни, хотя и в этом случае редко приводят к инвалидизации. С возрастом уменьшается не только интенсивность тиков, но и их дезадаптирующее влияние. У большинства взрослых больных тики обычно не усиливаются, возможно лишь их кратковременное ухудшение в период стрессовых ситуаций.
Более чем у половины больных с СТ выявляются сопутствующие психические расстройства (синдром навязчивых состояний, или обсессивнокомпульсивный синдром, и синдром дефицита внимания с гиперактивностью), роль которых в социальной дезадаптации больного бывает подчас значительно выше, чем роль гиперкинеза.
Причинами реже встречающихся вторичных тиков могут быть: повреждение головного мозга в перинатальном периоде, прием лекарственных препаратов (антиконвульсантов, нейролептиков, психостимуляторов и др.), черепно-мозговая травма, энцефалиты, сосудистые заболевания мозга, отрав ление угарным газом и т.д. При вторичных тиках гиперкинез обычно бывает менее динамичным (реже меняет локализацию, частоту, интенсивность), в меньшей степени выражены императивные позывы к движению и способность к подавлению гиперкинеза, могут присутствовать сопутствующие неврологические синдромы или такие психопатологические синдромы, как задержка психомоторного развития и умственная отсталость.
Тиком иногда ошибочно называют доброкачественную миокимию век – преходящие подергивания круговой мышцы глаз, возникающие у вполне здоровых людей при переутомлении, волнении, повышенном употреблении кофе или курении и не требующие лечения.
Во многих случаях при тиках медикаментозного лечения не требуется, достаточно успокоить больного и его родственников, рассказав о природе заболевания и указав на его доброкачественность. Важно упомянуть, что больному не угрожают снижение интеллекта, тяжелое психическое или неврологическое заболевание, и в подавляющем большинстве случаев больные прекрасно адаптируются в жизни [12].
При резистентности к указанной терапии прибегают к применению более высоких доз высокопотенциальных нейролептиков, комбинации двух нейролептиков с разным механизмом действия (например, рисперидона и тиаприда), комбинации нейролептика с антиконвульсантами (например, клоназепамом или топираматом) либо с баклофеном. При тяжелых болезненных дистонических тиках, вовлекающих мышцы лица и шеи, возможно лечение ботулотоксином, который инъецируют в мышцы, вовлеченные в тик. Показан положительный эффект инъекций ботулотоксина в голосовые связки при вокальных тиках, в том числе при копролалии.
Для лечения сопутствующего синдрома нарушенного внимания и гиперактивности применяют ноотропные средства (пирацетам, пиридитол, глиатилин и др.), агонисты пресинаптических альфа-2-адренорецепторов – клонидин и гуанфацин, малые дозы психостимуляторов, селегилин, трициклические антидепрессанты. Для лечения синдрома навязчивых состояний используют антидепрессанты, ингибирующие обратный захват серотонина (кломипрамин, сертралин, флувоксамин и др.).
В лечении больных с тиками важное место занимают методы психотерапии. Они не способствуют уменьшению тиков, но, изменяя в благоприятную сторону отношение больных к тикам и корригируя сопутствующие психические нарушения (прежде всего синдром навязчивых состояний), улучшают социальную адаптацию больных. Обучение методам релаксации позволяет больным снимать накапливающееся внутреннее напряжение. Разработаны специальные методики, тренирующие возможности больного произвольно контролировать тики (например, путем совершения конкурирующего движения при появлении ощущения, предваряющего тик).