Кортикальная атрофия что это такое и как лечить
Атрофия головного мозга на МРТ
Магнитно-резонансная томография признана одним из наиболее информативных нейровизуализационных методов исследования. В ходе процедуры получают детальные послойные снимки головного мозга, позволяющие оценить соответствие органа нормам.
МРТ актуальна при диагностике посттравматических состояний, воспалительных, опухолевых, нейродегенеративных изменений. Одно из самых тяжелых нарушений, выявляемых с помощью томографии — атрофия головного мозга. Это хроническое прогрессирующее заболевание, сопровождающееся гибелью нейронов, уменьшением объема и плотности структур головного мозга.
Атрофия лобных и височных долей на МР-сканах
В основе патологии лежат органические изменения в нервной ткани. Прогрессирование атрофии ведет к снижению функциональных возможностей ЦНС. Фактически это означает постепенное угасание работы (инволюцию) мозга вплоть до остановки жизненно важных процессов. Прогнозы неблагоприятные, так как изменения необратимы. Перспективы зависят от этиологии, формы, скорости прогрессирования болезни и качества оказываемой медицинской помощи.
Посредством МР-томографии можно выявить и определить локализацию указанных процессов на ранних этапах развития.
Признаки атрофии головного мозга
Патология может быть первичной и вторичной. Классификация обусловлена причинами развития заболевания. При первичной атрофии выявляют аномалии головного мозга и генетические нарушения. Отклонения могут манифестировать в любом возрасте, часто быстро прогрессируют, сложно поддаются коррекции.
Левосторонняя инволюция ткани головного мозга
Вторичная атрофия связана с воздействием внешних и внутренних неблагоприятных факторов. Инволюция нервной ткани может быть следствием черепно-мозговых травм, патологий сосудов, метаболических нарушений, вредных привычек, воздействия радиации и т.д. В данном случае устранение причины может способствовать замедлению развития заболевания. Правильная медикаментозная терапия способна обеспечить стабильное удовлетворительное состояние и качество жизни пациента на долгие годы.
Клинические проявления атрофии включают расстройства высшей нервной деятельности, нарушения синхронизации функций различных частей организма.
Симптомами заболевания могут быть:
проблемы со скелетной мускулатурой (от снижения тонуса до полной утраты способности двигаться);
снижение слуха и зрения вплоть до полной утраты;
речевые нарушения (от обеднения словарного запаса до невозможности изъясняться);
снижение или утрата обоняния;
изменение чувствительности разных частей тела;
нарушение координации движений;
потеря пространственной ориентации;
изменение поведения (от раздражительности до паранойи);
эмоциональная нестабильность (от чрезмерного возбуждения до полной аутизации).
Проблема диагностики атрофии головного мозга заключается в отсутствии или слабом проявлении симптомов на ранних этапах развития заболевания. Выделяют следующие стадии патологии:
Первая. Органические изменения в мозге минимальны, но уже присутствует слабая неврологическая симптоматика. Отмечают снижение способности к концентрации внимания, расстройство памяти, эмоциональную лабильность.
Вторая. Появляются нарушения слуха, зрения, речи. Существенно меняется поведение человека, возможны нелогичные поступки, которые сам больной не может объяснить или сразу забывает.
Как выглядит атрофия головного мозга на МРТ?
Диффузная атрофия головного мозга с вентрикуломегалией
Явление дифференцируют с истинной гидроцефалией. Главный МРТ-признак атрофии головного мозга — пропорциональное расширение внутренних и наружных ликворных церебральных пространств, что указывает на уменьшение объема структур органа. Выраженность изменений оценивают с помощью церебро-вентрикулярного индекса (ЦВИ Эванса). Учитывают и другие отклонения в ткани головного мозга.
Симптомы патологии на МРТ-снимках:
увеличение ЦВИ Эванса;
расширение субарахноидальных борозд и щелей;
снижение плотности мозговой ткани;
дистрофия белого вещества;
уменьшение долей мозга в размерах.
В зависимости от локализации патологических изменений и степени вовлеченности структур атрофия может быть:
кортикальной (главный признак — инволюция коры на уровне лобных и височных долей);
мультисистемной или диффузной (очаги обнаруживаются сразу на нескольких участках);
генерализованной (изменения происходят во всех отделах органа).
Атрофия коры головного мозга
Болезнь Альцгеймера

ОСОБЕННОСТИ ДИАГНОСТИКИ И ТЕРАПИИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА В НАШЕЙ КЛИНИКЕ
Наш ортодоксальный научный взгляд на проблему диагностики и лечения болезни Альцгеймера
Инновационная диагностика и персонализироанная молекулярнона-целенная терапия болезни Альцгеймера проводимая в нашей клинике
Всех пациентов с БА осматривает профессор д.м.н. Брюховецкий Андрей Степанович
Этому контингенту больных в нашей клинике по показаниям проводится специфическое нейроиммунологическое диагностическое обследование:
Наши клеточные препараты используются для лечения нейродегенеративных болезней только после курса молекулярнонацеленной лекарственной терапии, направ-ленной на восстановление проницаемости гематоэнцефа-лического барьера, блокирования цитотоксических цитокинов моноклональными антителами и специализированной имму-носупрессивной терапии :
Полагают, что основное значение в возникновении болезни Альцгеймера имеет генетическая предрасположенность
Дефекты митохондриальной ДНК найдены примерно у 50% больных (502500, ген MTND1, митохондриальное наследование). Раннее начало связано с дефектами генов АРР, PSEN1, PSEN2.
Болезнь можно рассматривать как семейство заболеваний, имеющих различное происхождение, но общий патогенез: все известные генные дефекты модифицируют процессинг белка—предшественника амилоида (гипотеза «амилоидной цепи»), что ведёт к появлению нейротоксичных форм белков.
При болезни Альцгеймера в ткани мозга образуются многочисленные бляшки — отложения амилоидного белка, вызывающие дегенерацию нейронов и их отростков.
Симптомы болезни Альцгеймера
При развитии болезни Альцгеймера наблюдаются следующие диагностирующие симптомы :
Методы исследования для постановки диагноза болезни Альцгеймера:
Лечение болезни Альцгеймера
Специфического лечения болезни Альцгеймера на данный момент нет. Следует применять минимальное количество лекарственных средств вследствие плохой переносимости:
Лечение начинают с минимальных доз, постепенно повышая до эффективных
Болезнь Пика

Причины заболевания. Причина заболевания точно не установлена, предполагают, что причина заболевания в нарушении обмена тау-протеина (особый белок центральной нервной системы) в головном мозге. Наследственная предрасположенность: иногда встречаются случаи заболевания в семье.
Симптомы болезни Пика
Диагностика
• МРТ (магнитно-резонансная томография) головного мозга: метод, позволяющий послойно изучить головной мозг. При болезни Пика отмечается атрофия (истончение) коры головного мозга в лобных и височных долях.
Лечение болезни Пика
Лечение, способное замедлить прогрессирование заболевания, отсутствует.
При тяжелых нарушениях психики и поведения может потребоваться психиатрическая помощь, а также помещение больного в хоспис (медицинское учреждение, в котором больные люди с потенциально неблагоприятным прогнозом заболевания получают должный уход и помощь).
Осложнения и последствия
Для получения информации о записи на прием к специалистам просим обращаться по телефонам:
8 499 324-93-39; 8 499 324-44-97, +7 906 749-98-00
или по электронной почте Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript. / Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Кортикальная атрофия что это такое и как лечить
Кортикобазальная дегенерация (КБД) – спорадическое дегенеративное заболевание ЦНС, вовлекающее преимущественно лобно-теменную кору и черную субстанцию, реже – стриатум, вентролатеральный таламус, ядра среднего мозга, зубчатые ядра мозжечка, нижние оливы [5, 10, 28].
Заболевание относится к числу редких, однако в последние годы оно диагностируется все чаще, и число описанных в литературе случаев приближается к 100. КБД входит в группу нейродегенеративных заболеваний, характеризующихся сочетанием паркинсонизма с другими неврологическими расстройствами, атипичными для болезни Паркинсона («паркинсонизмплюс»), однако на ранней стадии КБД могут возникать затруднения в дифференциальной диагностике с болезнью Паркинсона.
Приводим описание случая клинически диагностированной КБД.
Больной К., 67 лет. Около 2 лет назад заметил постепенно нарастающую неловкость в правой руке. Затем присоединились дрожание в этой же руке, общая замедленность движений, аспонтанность, пошатывание при ходьбе. Был поставлен диагноз болезни Паркинсона, назначены Наком (3 таблетки в сутки) и циклодол (6 мг/сут.). Вначале на фоне лечения состояние больного улучшилось, однако в дальнейшем оно продолжало ухудшаться и увеличение дозы Накома до 6 таблеток в сутки не дало эффекта.
При осмотре легкий парез взора вверх, умеренная дизартрия, рефлексы орального автоматизма, умеренная олигобрадикинезия, мышечная ригидность (с феноменом «зубчатого колеса»), более выраженная в правой руке и аксиальной мускулатуре, оживление сухожильных рефлексов, более отчетливое справа. Особое внимание обращают на себя своеобразные двигательные нарушения в правой руке. Она находится в дистонической флексорно-аддукторной позе (плечо приведено, а предплечье, кисть и пальцы согнуты), ее движения крайне замедленны и ограничены по амплитуде, иногда в ней отмечаются непроизвольные движения, не похожие на обычные гиперкинезы: правая кисть периодически сжимается и разжимается, что напоминает стереотипии, а вся рука изредка медленно приподнимается. В мышцах этой руки наблюдаются неритмичные миоклонические подергивания, которые усиливаются при движении. В обеих руках отмечается умеренный постуральный и интенционный тремор, более выраженный справа.
При движениях более сохранной левой руки в правой руке иногда отмечаются синкинетические зеркальные движения. Значительные затруднения больной испытывает при вставании, поворотах в постели. Наблюдаются умеренные дисбазические проявления в виде замедления инициации ходьбы, затруднений при поворотах, уменьшения длины шага, шаркающей походки, пошатывания при ходьбе. Справа выявляется ахейрокинез, однако флексорной позы нет. В позе Ромберга больной относительно устойчив, но реактивные постуральные рефлексы нарушены и при подталкивании в грудь больной теряет равновесие. Справа расстройства сложных видов глубокой чувствительности (астереогноз, аграфестезия, нарушение чувства дискриминации и локализации) на фоне умеренного нарушения вибрационной чувствительности и суставно-мышечного чувства. Кардиоваскулярные пробы не выявили признаков вегетативной недостаточности.
При нейропсихологическом исследовании на фоне выраженных нейродинамических нарушений, проявлявшихся замедленностью, аспонтанностью, снижением работоспособности, быстрой истощаемостью, флуктуациями внимания, трудностью вхождения в задание и удержания его условий, выявлена динамическая афазия с выраженным снижением речевой активности, обеднением структуры речевого высказывания и единичными парафазиями. При исследовании праксиса в левой руке обнаружены признаки динамической апраксии (дезавтоматизация двигательных навыков, нарушение временно́й организации двигательных актов, трудность заучивания и удержания двигательных программ, грубое нарушение реципрокной координации, застывания, двигательные персеверации) и пространственной апраксии (с нарушением конструктивного праксиса и праксиса позы), менее выраженные признаки регуляторной и кинестетической апраксии. Нарушений гнозиса не выявлено. При исследовании памяти обнаружены умеренные модально-неспецифические дефекты, связанные с нарушением активности, прочности и избирательности запоминания. В тестах на интеллект выявлено его легкое снижение, главным образом вследствие нарушения произвольной регуляции и концентрации внимания, импульсивности. В Висконсинском тесте сортировки карточек отмечено низкое количество выполненных категорий при значительном увеличении числа персеверативных ответов и ошибок, что указывало на выраженные регуляторные нарушения. Общая оценка когнитивных функций по данным Краткого исследования психического статуса (Mini-Mental State Examination) относительно высокая – 25/30 баллов. Таким образом, констатирована дисфункция лобной и теменной коры, преимущественно слева, при заинтересованности глубинных отделов мозга и относительной сохранности мнестических и интеллектуальных процессов.
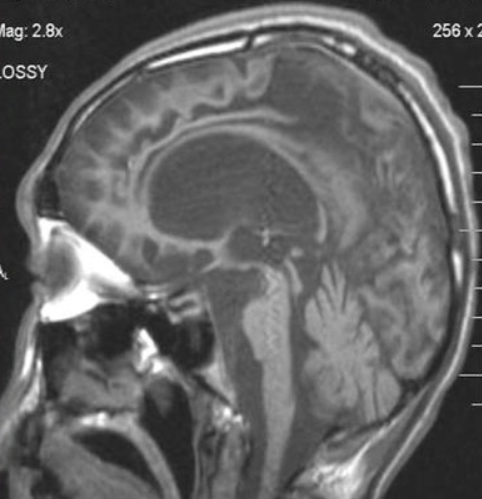
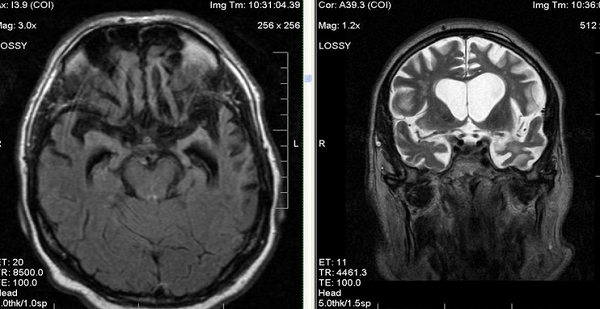
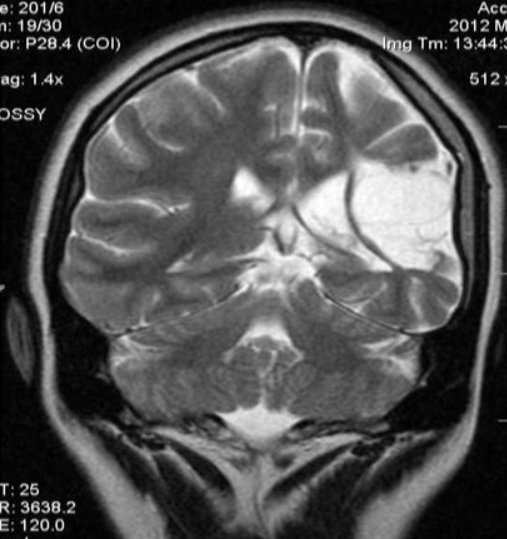
МРТ головы выявила умеренную двустороннюю церебральную атрофию преимущественно в лобно-теменной области с преобладанием слева, проявлявшуюся расширением корковых борозд и боковых желудочков. Очагов измененной интенсивности сигнала, смещения срединных структур не было.
Таким образом, неуклонно прогредиентное течение с асимметричным вовлечением коры и подкорковых структур, проявлявшимся своеобразным набором неврологических и нейропсихологических симптомов, включая леводопа-резистентный паркинсонизм, фокальную дистонию, миоклонию, постуральный и интенционный тремор, лобную дисбазию и умеренную постуральную неустойчивость, феномен «чужой» руки, апраксию и нарушение сложных видов глубокой чувствительности, в отсутствие клинических или нейровизуализационных признаков, характерных для других заболеваний, привело нас к выводу о наличии у больного КБД.
В последующем отмечено дальнейшее прогрессирование заболевания с нарастанием акинетико-ригидного синдрома, нарушений ходьбы, постуральных расстройств, усугублением когнитивного дефекта. Применение парлодела (15 мг/сут.) и Мидантана (300 мг/сут.) оказалось неэффективным. На фоне лечения клоназепамом несколько уменьшились миоклонии и интенционный тремор. Через 5 лет от начала больной оказался прикованным к постели и абсолютно зависимым от постороннего ухода.
Обсуждение
Впервые КБД была описана в 1968 г. J.Rebeiz и соавт. [25] как кортикодентатонигральная дегенерация. Нозологическая самостоятельность КБД определяется особенностями ее патоморфологии [14, 25]. Макроскопически при КБД выявляются асимметричная атрофия вещества мозга, более выраженная в лобной и теменной коре (особенно в области, окружающей роландову и сильвиеву борозды), депигментация черной субстанции. При микроскопическом исследовании наряду с уменьшением численности нейронов и глиозом в лобной и теменной коре обнаруживаются ахроматические баллонообразные клетки, представляющие собой «визитную карточку» КБД [10]. Баллонообразные клетки выявляются также в базальных ганглиях, структурах среднего мозга, зубчатом ядре мозжечка. Кроме того, в коре и подкорковых структурах обнаруживаются характерные внутриклеточные включения, содержащие тау-протеин. Тау-протеин при КБД накапливается не только в нейронах, но и в глиальных клетках: в астроцитах (формируя специфичные для КБД «астроцитарные» бляшки) и олигодендроцитах [6, 14]. При гистохимических исследованиях выявляется резкое уменьшение содержания дофамина в стриатуме [9, 29].
Заболевание обычно начинается во второй половине жизни (чаще после 60 лет) [26]. Мужчины и женщины поражаются с одинаковой частотой. Первыми проявлениями КБД обычно бывают неловкость в одной из конечностей (чаще всего в руке), а также онемение, сопровождающееся нарушением сложных видов чувствительности (астереогнозом, аграфестезией, нарушением дискриминационного чувства) [10]. Симптоматика постепенно распространяется сначала на ипсилатеральную, а затем на контралатеральную руку или ногу. Присоединяются олигобрадикинезия, ригидность, пирамидные знаки, тремор, миоклония и другие проявления поражения подкорковых и корковых структур. Неврологические нарушения могут возникать в любой последовательности и любой комбинации, что определяет значительную вариабельность клинической картины [15, 23, 26].
Наиболее частым признаком служит паркинсонизм, отмечаемый почти у 100% больных; в большинстве случаев паркинсонизм проявляется асимметричным акинетико-ригидным синдромом. Из других экстрапирамидных расстройств чаще встречается мышечная дистония (53–83%), которая бывает фокальной или сегментарной и обычно вовлекает конечности и/или аксиальную мускулатуру. Изредка отмечают блефароспазм и оромандибулярную дистонию [27]. Весьма характерна для КБД своеобразная дистоническая поза руки с приведением плеча, сгибанием предплечья, кисти и пальцев (некоторые пальцы могут оставаться разогнутыми). Иногда пальцы буквально впиваются в ладонь, и больные вынуждены брать в руку клубок ниток, чтобы не поранить руку ногтями [27]. У части больных отмечены хорея и атетоз [15, 23].
Миоклония наблюдается у 45% больных, чаще в наиболее пораженной конечности [4, 10, 15]. Миоклонические подергивания, как правило, усиливаются при движении (кинетическая, или интенционная, миоклония), их можно также вызвать путем механической или электрической стимуляции (рефлекторная миоклония). Электрофизиологические исследования показывают, что миоклония носит корковый характер и связана с растормаживанием транскортикального рефлекса в результате нарушения интракортикального или кортикоталамического торможения, вызванного селективной дегенерацией ГАМКергических нейронов или астроцитарной патологией [4].
Тремор наблюдается у 33% больных, чаще он имеет постуральный характер, реже – интенционный; изредка встречаются тремор покоя и ортостатический тремор (возникающий в ногах при переходе в вертикальное положение). У 90% больных выявляются надъядерные глазодвигательные расстройства в виде затруднения инициации и ограничения амплитуды горизонтальных и/или вертикальных саккадических и следящих движений, но явный парез взора (чаще вертикального) встречается лишь у 20% больных и обычно на поздней стадии заболевания. Иногда отмечаются форсированное отведение глазных яблок, а также апраксия открывания глаз, в основе которой лежит нарушение нормальных реципрокных соотношений между круговой мышцей глаза и мышцей, поднимающей верхнее веко, в результате чего больной периодически не может произвольно открыть глаза. У части больных выявляются лобные знаки: хватательный рефлекс и паратония.
Походка нарушается почти в 100% случаев. Если первые проявления болезни отмечались в ноге, то уже в течение первого года развиваются выраженные нарушения ходьбы по типу лобной дисбазии (апраксии ходьбы) и постуральная неустойчивость с частыми падениями (преимущественно кзади). Если же первой была вовлечена рука, то нарушения ходьбы возникают в среднем через 3 года [27]. Пирамидные нарушения встречаются часто – более чем у 70% больных, но обычно бывают умеренными и ограничиваются оживлением рефлексов и патологическими кистевыми и стопными знаками. У небольшой части больных встречается мозжечковая атаксия. У 70% больных отмечена дизартрия, которая нередко имеет сложный характер и иногда прогрессирует вплоть до анартрии. Дисфагия относится к числу редких проявлений и обычно встречается на поздней стадии [10, 15, 23, 28].
Нарушение высших мозговых функций – характерное проявление КБД, встречающееся более чем в 90% случаев [15]. Наиболее характерный для КБД тип расстройств – апраксия (84% случаев) [27]. Нередко она развивается уже на ранней стадии заболевания. Апраксия почти всегда присутствует в тех случаях, когда заболевание преимущественно поражает левое (доминантное) полушарие, а симптоматика, соответственно, начинается с правой руки. Апраксия при КБД чаще бывает двусторонней, но легче всего ее выявить в той руке, в которой менее выражена экстрапирамидная или пирамидная симптоматика [17].
Согласно современным представлениям, в нижнетеменной коре доминантного полушария по мере заучивания движения формируется его пространственно-временна́я (визуально-кинестетическая) программа (идея, или концепция, движения), находящаяся в определенном взаимодействии со схемой тела и схемой внешнего пространства. Однако для того чтобы эта программа, «записанная» с помощью трехмерного пространственного кода, претворилась в моторный акт, она должна быть преобразована в конкретный временно-пространственный план, в соответствии с которым должны активироваться нейроны первичной моторной коры. По-видимому, это происходит в дополнительной моторной коре при определенном участии фронтостриатоталамофронтального моторного круга. При поражении теменной доли больные не в состоянии не только выполнить заученное движение, но и отличить успешное движение от неуспешного (у них отсутствует образ правильного движения, и они обычно не знают, что делать), тогда как больные с поражением лобной коры или теменно-лобных связей, будучи не в состоянии выполнить то или иное движение (не знают, как делать), тем не менее способны оценить успешность своего движения [9, 11]. Реже при КБД выявляются признаки идеаторной апраксии, характеризующейся нарушением смысловой структуры действий, что проявляется прежде всего нарушением сложных, многозвеньевых действий. Признаки идеаторной апраксии, как правило, присоединяются позже в связи с дальнейшим прогрессированием апраксического дефекта. В то же время уже на ранней стадии КБД могут присутствовать признаки кинетической (конечностнокинетической) апраксии, для которой характерно нарушение микроструктуры действия, т.е. сцепления его отдельных фрагментов, в результате чего движение становится «скандированным» [1], нарушается его кинематическая мелодика [2], тогда как макроструктура действия, т.е. принципиальная последовательность его звеньев, остается относительно сохранной [2, 9].
В представленном случае мы квалифицировали имеющийся у больного апраксический дефект в соответствии с классификацией А.Р.Лурия, который выделил 4 основных типа апраксии: пространственную, характеризующуюся нарушением образа действия; кинетическую (динамическую), проявляющуюся нарушением его двигательной «временно́й развертки»; кинетическую, в основе которой лежит нарушение обратной связи и возможности сличения реального действия с идеальным; регуляторную, проявляющуюся нарушением программирования действий, системными персеверациями и эхопраксией [2]. У представленного больного апраксический дефект проявлялся главным образом кинетической и пространственной апраксией с элементами нарушения кинестетического и регуляторного праксиса.
Анализируя характер апраксического дефекта у данного больного в контексте всего комплекса нейропсихологических и неврологических расстройств, можно полагать, что апраксия при КБД связана с дисфункцией различных звеньев системы праксиса, однако ведущим механизмом является дисфункция премоторной и дополнительной моторной коры, которая может быть обусловлена не только ее первичным поражением, но и разобщением нижнетеменной и дополнительной моторной коры. Последнее объясняет наличие признаков пространственной апраксии при сохранной способности оценивать правильность действия. Обнаруженный нами у больного дефицит регуляторных когнитивных функций служит доводом в пользу того, что важную роль в развитии апраксии может играть также поражение фронтостриарных кругов, обеспечивающих переключение и адаптацию двигательных программ в необычных ситуациях, требующих концентрации внимания и мотивационного подкрепления [16].
Апраксия при КБД может выявляться не только в руках. При вовлечении вентролатеральной премоторной коры, оперкулярной области и прилегающей к ней передней части перивентрикулярного белого вещества могут возникать особые формы апраксии: оральная апраксия, апраксия взора, речевая апраксия, туловищная (аксиальная) апраксия, апраксия ходьбы [5, 15, 18].
Афазия отмечается приблизительно у 20% больных с КБД и возникает при поражении доминантного полушария [5, 15]. Описаны различные варианты речевых нарушений, которые могут быть связаны с поражением как корковых, так и подкорковых структур, однако чаще всего выявляются так называемые передние варианты афазии со снижением речевой активности и нарушением синтагматической структуры речи [18]. КБД может служить одной из причин синдрома первичной прогрессирующей афазии, протекающей по типу транскортикальной моторной (динамической – по классификации А.Р.Лурия) афазии [19]. При поражении недоминантного полушария у больных отмечаются зрительно-пространственные нарушения и синдром игнорирования половины пространства – односторонняя пространственная агнозия [24].
Довольно часто встречаются когнитивные расстройства подкорковолобного типа с нарушением регуляторных («исполнительных») функций (т.е. расстройство планирования, инициации, поэтапной реализации, завершения целенаправленных мыслительных и поведенческих актов [5]), выявляемым, в частности, в Висконсинском тесте сортировки карточек [12], психомоторных функций (с нарушением организации серийных движений, реципрокной координации), нарушением внимания [10, 23]. В то же время память может оставаться относительно сохранной либо нарушаться вторично вследствие нейродинамических и регуляторных расстройств (в этом случае запоминание можно улучшить с помощью организации мнестического процесса, в частности с помощью семантического кодирования) [6].
Снижение интеллекта с развитием деменции обычно развивается лишь на поздней стадии заболевания, на фоне уже развившегося грубого двигательного дефекта [23]. На поздней стадии заболевания деменция отмечена у 45% больных [15]. В то же время описаны патоморфологически подтвержденные случаи, когда деменция была начальным и доминирующим проявлением заболевания [14]. У части больных отмечается обсессивнокомпульсивный синдром, связанный с поражением латерального орбитофронтального круга, объединяющего орбитофронтальную кору с вентромедиальной частью хвостатого ядра [24].
Одно из характерных проявлений КБД – феномен «чужой» конечности, встречающийся приблизительно у половины больных с КБД. Обычно он становится заметным через 1 год от начала заболевания [5, 7, 15]. Симптом «чужой» (автономной) конечности – сложный сенсомоторный феномен, характеризующийся одновременно ощущением отчуждения конечности и ее непроизвольной (автономной) двигательной активностью при неспособности участвовать в произвольных действиях [7]. Иногда больные персонифицируют свою «чужую» конечность, не подчиняющуюся владельцу, наделяя ее своей собственной волей. Чаще всего феномен «чужой» конечности отмечается в руке («чужая» рука). Отчуждение руки проявляется, в частности, тем, что при выключении зрительного контроля (например, при заведении рук за спину) больной не в состоянии отличить больную руку от руки исследователя. Спектр возможной автономной активности «чужой» руки весьма широк: от простых движений (например, поднимание руки вверх, т.е. «левитация», или ее сгибание) до довольно сложных (хватательных или ощупывающих движений, навязчивых манипуляций с предметами, а иногда и аутоагрессивных действий). Нередко движения в руке возникают синкинетически – одновременно с движениями непораженной или менее пораженной контралатеральной конечности, при этом они часто имитируют их (зеркальные движения). У больных обычно грубо нарушается бимануальная координация. Иногда «чужая» рука вмешивается в движения здоровой руки («интермануальный конфликт»).
Феномен «чужой» конечности наблюдается не только при КБД, но и при фокальных поражениях дополнительной моторной коры, передней поясной извилины, медиальной части префронтальной коры доминантного полушария, вызванных инфарктом, разрывом аневризмы передней соединительной артерии, черепно-мозговой травмой и др. [5, 7]. Помимо «лобного» варианта «чужой» конечности, описан и так называемый каллозальный вариант, обусловленный поражением передней части мозолистого тела, где проходят пути, связывающие левую премоторную область с правой; в этом случае обычно вовлекается недоминантная рука, отмечается выраженный интермануальный конфликт и отсутствуют лобные знаки. Однако чаще всего феномен развивается при одновременном поражении дополнительной моторной коры и мозолистого тела. Феномен «чужой» конечности необходимо дифференцировать с лобными знаками, атетозом, псевдоатетозом, возникающим при поражении глубокой чувствительности, дистонией, гемибаллизмом и гемиатаксией, при которых не возникает ощущения отчуждения конечности, а также с синдромом игнорирования контралатерального пространства (вследствие поражения теменной доли) или зрительной атаксии (вследствие поражения затылочной доли), для которых чаще всего бывает характерна непроизвольная двигательная активность. Изредка при поражении теменно-затылочной области и таламуса даже при сохранности мозолистого тела все же возникает своеобразный вариант «чужой» руки, в основе которого лежит одновременное нарушение зрительного и кинестетического контроля за рукой [7, 10, 30]. По всей видимости, «чужая» конечность – самостоятельный синдром, однако его генез в целом и, в частности, происхождение ощущения отчуждения конечности остаются неясными. Неизвестно, в каком соотношении находится «чужая» рука с нарушением праксиса и сложных видов глубокой чувствительности. R.Leiguarda и соавт. [17] обнаружили феномен «чужой» руки только у больных с КБД, имевших апраксию. Возможно, что ощущение отчуждения и непроизвольная (расторможенная) двигательная активность частично связаны с «выключением» руки из программ действий, однако это требует доказательств.
Неврологические проявления КБД неуклонно прогрессируют. В течение нескольких лет симптоматика может выявляться только в одной руке, однако в последующем неврологические расстройства постепенно генерализуются, обрастают когнитивными нарушениями и в конце концов приковывают больного к постели [23]. В среднем это происходит за 5 лет. Умирают больные через 5–10 лет от начала заболевания, чаще всего от бронхопневмонии.
КТ или МРТ при КБД могут не выявлять патологию, но чаще у больных обнаруживается диффузная церебральная атрофия, которая нередко имеет асимметричный характер и преимущественно вовлекает лобную и теменную доли на стороне, контралатеральной симптоматике. Иногда отмечают также снижение интенсивности сигнала от скорлупы и бледного шара на Т2-взвешенных изображениях, связанное, очевидно, с отложением железа [23, 26]. Позитронно-эмиссионная томография (ПЭТ) при КБД выявляет асимметричный гипометаболизм в заднелатеральной лобной, нижнетеменной области, латеральных отделах височной коры, стриатуме, гиппокампе и таламусе, а также снижение захвата 18 F-ДОФА в стриатуме (как в скорлупе, так и в хвостатом ядре). Данная картина существенно отличается как от болезни Паркинсона, при которой гипометаболизм обычно не выявляется ни в хвостатом ядре, ни в коре (если же он присутствует в последней, то обычно в теменно-височной области, как при болезни Альцгеймера), так и от прогрессирующего надъядерного паралича (ПНП), при котором гипометаболизм выявляется в лобных областях [8, 21].
По мнению W.Oertel и N.Quinn [22], для постановки диагноза КБД необходимо наличие не менее 3 из следующих 6 признаков: 1) акинетикоригидного синдрома, не реагирующего на L-ДОФА; 2) феномена «чужой» конечности; 3) апраксии или нарушения сложных видов глубокой чувствительности; 4) фокальной дистонии в конечности; 5) грубого постурального или интенционного тремора; 6) миоклонии.
Сложность диагностики КБД заключается в том, что существует определенное клиническое и/или патоморфологическое сходство КБД с некоторыми другими дегенеративными заболеваниями ЦНС, особенно с теми из них, которые вызывают асимметричную или фокальную дегенерацию коры и базальных ганглиев. По своим морфологическим характеристикам КБД особенно близка к группе фокальных корковых дегенераций, прежде всего к болезни Пика [14]. Клинический синдром, напоминающий КБД, встречается при болезни Альцгеймера, болезни диффузных телец Леви, болезни Галлервордена–Шпатца, болезни Пика и особенно часто при ПНП [19, 24, 28]. Сходство клинической картины в этих случаях объясняется тем, что морфологически различные дегенеративные процессы могут поражать одни и те же мозговые структуры. В связи с отсутствием патогномоничных клинических и патоморфологических признаков некоторые авторы высказывают сомнение в нозологической самостоятельности КБД, а само заболевание рассматривают как клинический синдром, в виде которого могут проявляться различные нейродегенеративные заболевания [28].
На ранней стадии дифференциальный диагноз приходится проводить с болезнью Паркинсона, для которой также характерна асимметричность проявлений. Однако малая эффективность препаратов L-ДОФА при КБД, отсутствие тремора покоя и особенно появление атипичных для болезни Паркинсона подкорковых и фокальных корковых нарушений позволяют отвергнуть этот диагноз. На более продвинутой стадии могут возникать трудности в дифференциации с хроническим сосудистым поражением мозга, болезнью Крейтцфельдта–Якоба, мультисистемной атрофией и др. В тех случаях, когда выраженные когнитивные и поведенческие нарушения присутствуют уже на ранней стадии заболевания, необходимо подумать о болезни Пика или болезни Альцгеймера с «синдромом КБД». В первом случае внимание будут привлекать поведенческие и когнитивные нарушения лобного типа, выраженные речевые нарушения по типу динамической афазии, во втором – нарушения памяти, счета, речи (по типу акустико-мнестической и семантической афазии). Значительные трудности могут возникать при дифференциальной диагностике КБД и ПНП, поскольку при КБД могут отмечаться паралич вертикального взора и выраженные постуральные нарушения, тогда как при ПНП – асимметричный акинетико-ригидный синдром, апраксия и феномен «чужой» руки [27]. Правильная диагностика возможна при оценке всего комплекса синдромов, их соотношения и времени наступления. При ПНП обычно отсутствуют фокальные корковые нарушения и миоклонии, а выраженный паралич вертикального взора (особенно вниз), грубая постуральная неустойчивость, тяжелая двусторонняя акинезия и аксиальная ригидность развиваются сравнительно рано. Асимметричное начало с развитием ригидности или дистонии в одной из конечностей при ПНП наблюдается исключительно редко.
Важное дифференциально-диагностическое значение имеет МРТ, позволяющая прежде всего исключить сосудистое поражение или объемный процесс. Следует отметить, что у пожилых пациентов (а КБД – это болезнь пожилого возраста) МРТ нередко выявляет очаги измененной интенсивности сигнала в базальных ганглиях и/или очаговые или диффузные изменения перивентрикулярного белого вещества, о морфологическом субстрате которых бывает сложно судить. В связи с этим для того, чтобы избежать гипердиагностики сосудистого процесса, необходимо соотносить размер и локализацию таких очагов с характером и выраженностью клинических проявлений. Значение МРТ в дифференциальной диагностике нейродегенеративных заболеваний менее определенно. Пока можно лишь полагать, что это зависит прежде всего от возможности МРТ выявлять характерное для каждого заболевания распределение церебральной атрофии, например: преобладание атрофии лобных долей и полюса височной доли в случае болезни Пика, выраженную атрофию медиальных отделов височных долей (и прежде всего гиппокампа) при болезни Альцгеймера, атрофию среднего мозга при ПНП. Иногда имеет значение и изменение интенсивности сигнала от подкорковых структур мозга (например, при болезни Галлервордена–Шпатца). Следует подчеркнуть, что достоверная диагностика КБД, как, впрочем, и других нейродегенеративных заболеваний, возможна лишь при аутопсии.
Терапевтические возможности при КБД весьма ограниченны. Попытка лечения высокими дозами метилпреднизолона, которая основывалась на предположении об аутоиммунном генезе КБД и выявлении у части больных воспалительных изменений в цереброспинальной жидкости (легкое повышение цитоза и содержания белка), оказалась безуспешной [29]. У части больных выявляется умеренный, хотя и не стойкий, эффект препаратов L-ДОФА, что соответствует результатам исследований нейромедиаторного обмена, показывающим, что у ряда больных выявляется пресинаптический дефицит дофамина, связанный, вероятно, с дисфункцией нигростриарных путей. Чаще же препараты L-ДОФА оказываются неэффективными, что, по всей видимости, отражает доминирующую роль стриарной дегенерации (и, соответственно, постсинаптических нарушений) в генезе паркинсонизма. Определенный эффект можно иногда получить и с помощью агонистов дофаминовых рецепторов. Выраженность миоклонии, интенционного тремора можно уменьшить с помощью клоназепама. Постуральный тремор можно облегчить с помощью бета-адреноблокаторов. Баклофен, холинолитики, антиконвульсанты обычно неэффективны [11]. Попытки лекарственной терапии нередко лишь ухудшают состояние больных, способствуя нарастанию когнитивного дефекта, нарушений ходьбы, заторможенности и спутанности. При фокальных дистониях эффективны инъекции ботулотоксина [11]. Важное значение имеет лечебная гимнастика, которая предотвращает контрактуры, облегчает болезненную дистонию и позволяет некоторое время поддерживать активность больного.
Литература
* Неврологический журнал. – 1997. – №6. – С. 17–23.