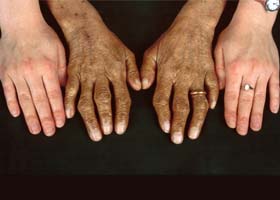
гемохроматоз что это такое фото
Гемохроматоз — причины, симптомы и лечение
Являясь одним из наиболее важных микроэлементов, железо содержится в целом ряде пищевых продуктов. Его основными источниками служат красное мясо, яблоки, специально обогащённый хлеб и крупы. Железо содержится в составе молекулы гемоглобина (присоединившей железо протопорфирин-IX). В составе красных кровяных телец – эритроцитов, доставляет из лёгких кислород по всему телу. Организм здорового человека содержит от 3 до 4 грамм железа. Однако при гемохроматозе этот показатель возрастает до 20-60 г.
Такое обусловленное генетической наследственностью заболевание, как гемохроматоз, проявляется в накоплении железа в органах и тканях, вызываемом нарушением его обмена. Местами чрезмерной концентрации этого поступающего из пищи элемента становятся различные органы и ткани организма: печень и поджелудочная железа, селезёнка и миокарда, эндокринные железы и кожа. Переизбыток накопленного железа нередко провоцирует развитие цирроза печени, сердечной недостаточности, сахарного диабета, артрита и ряда других заболеваний.
Учёные американского гринвиллского Института расстройств желез, расположенного в Южной Каролине, подсчитали, что в США около 150 тысяч диагностированных больных гемохроматозом и около миллиона человек имеют предрасположенность к этому заболеванию. То есть вероятность его развития составляет треть процента. Помимо первичного (классического) гемохроматоза, различают и вторичный. Он связан с многократным переливанием крови, повторными кризами мегалобластной и гемолитической анемий, просчётами в лечении препаратами железа.
Симптомами гемохроматоза могут стать артрит, суставные боли, усиленная пигментация кожи. Кроме того, так как в организме человека до 90% железа поглощаются печенью, проявления заболевания могут варьировать в довольно широких пределах. В оказывающих медицинские услуги учреждениях диагностика гемохроматоза довольно проста. Так как это заболевание, как правило, наследственное, она обеспечивается сочетанием тщательно собранного семейного анамнеза и лабораторной диагностики.
Клиническими симптомами служат быстрая утомляемость и слабость, выраженное похудание, сахарный диабет, снижение давления, болезненность и отёчность суставов, сердечная недостаточность, грифельно-серый с коричневым оттенком цвет кожи, гиперпигментация сетчатки и слизистых оболочек. При лечении гемохроматоза применяется богатая белком диета с ограниченным количеством содержащих железо продуктов (яиц, мёда, рыбы, мяса, яблок и т.д.). Алкоголь категорически противопоказан.
Рекомендуются флеботомия или венесекция – кровопускания, способствующие удалению железа из организма и уменьшающие пигментацию и размер печени, улучшающие общее состояние. Медикаментозное лечение строится на связывающих железо и способствующих его выведению препаратах дефероксамин и Б-десфераль. Прогнозируется лечение заболевания в зависимости от длительности его течения до момента диагностики.
Гемохроматоз что это такое фото
Синонимы: бронзовый диабет, цирроз печени пигментный, синдром Труазье—Ано—Шоффара, синдром Реклингхаузена—Аппельбаума.
Определение. Заболевание, вызванное наследственным дефектом обмена железа и сопровождающееся развитием пигментного цирроза печени, пигментации кожи, сахарного диабета и сердечной недостаточности.
Историческая справка. Болезнь впервые описал в 1865 г. французский терапевт, профессор Арман Труссо в сообщении о пациенте с диабетом, циррозом печени и бронзовой пигментацией кожи. Однако он не связывал наличие данного заболевания с накоплением железа в паренхиматозных органах. В 1871 г. французский патолог Charles Troisier (1844-1919) и в 1882 г. французские врачи Victor Hanot (1844-1896) и Anatole Chauffard (1855—1932) описали данное заболевание как сочетание сахарного диабета с гиперпигментацией кожи и циррозом печени при избытке железа. В 1889 г. термин «гемохроматоз» предложен впервые Фридрихом фон Реклингхаузеном (1833—1910), а в 1900 г. — Лео Аппельбаумом.
Этиология и патогенез. Гемохроматоз относится к группе болезней «накопления», заключается в генетически обусловленном нарушении метаболизма железа и начинается задолго до проявления симптомов. Избыточное накопление железа в виде ферритина и гемосидерина происходит в паренхиматозных органах (чаще в печени, поджелудочной железе, реже в селезенке, сердце и других органах) с последующим их фиброзом и функциональной недостаточностью. Молекулярный механизм, лежащий в основе токсического действия железа,— это генерация свободных радикалов и перекисное окисление липидов. В коже и мышцах откладывается также железосодержащий пигмент — липофусцин.
Итог этого явления — вторичная воспалительно-склеротическая реакция тканей. Под влиянием избыточного содержания железа в коже, по-видимому, за счет усиления тирозин-тирозиназной активности, происходит усиление меланогенеза. На основании генетических и биохимических различий выделяют четыре типа гемохроматоза. Типы 1, 2 и 3 наследуются аутосомно-рецессивно, а тип 4 — аутосомно-доминантно.
Тип 1 является классическим и сопровождается перенасыщением трансферрина, повышением концентрации ферритина и содержания железа в ткани печени; генные локусы — 6р21.3, 1q21.
Тип 2 считается ювенильным и характеризуется значительным отложением железа во внутренних органах, ранним началом и быстрым прогрессирующим течением; генные локусы — 19р13, 1q21.
Тип 3 характеризуется высоким содержанием железа во внутренних органах, нормальными насыщением трансферрина и концентрацией ферритина в крови; локус гена — 7р22. Тип 4 сопровождается значительными изменениями биохимических показателей при минимальных отложениях гемосидерина во внутренних органах; локус гена — 2р32.
Также выделяют приобретенную (вторичную) форму гемохроматоза, которая развивается в результате избыточного поступления в организм железа. Среди вторичных гемохроматозов выделяют четыре вида. Первый (посттрансфузионный) развивается в результате частых повторных гемотрансфузий при лечении хронических анемий. Второй (алиментарный) регистрируется в африканском племени банту, а также у лиц, употребляющих в больших количествах железосодержащие тонизирующие напитки и алкоголь.
Третий (метаболический) возникает при нарушениях метаболизма железа при промежуточной талассемии, циррозе печени (после операции портокавального анастомоза), гепатитах В и С, неалкогольном стеатогепатозе, кожной порфирии, раковых заболеваниях, при закупорке протока поджелудочной железы. Четвертый (смешанный) отмечается при большой талассемии и некоторых видах дизэритропоэтической анемии.
Частота. Наследственный гемохроматоз является одним из самых распространенных аутосомно-рецессивных заболеваний в Европе, Америке, Австралии с частотой гетерозигот 10—16%, развивающихся в среднем в 3—7 случаях на 1000 носителей гена наследственного гемохроматоза.
Возраст и пол. Эта болезнь в 95% случаев поражает мужчин, обычно в возрасте 40—60 лет, клинические проявления у них наиболее тяжелые и начинаются раньше, чем у женщин.
Общая характеристика. Характерна триада: поражение печени (цирроз у 92%), поджелудочной железы (сахарный диабет у 25—70%) и кожи (меланоз у 84%), однако полный симптомокомплекс наблюдается только в терминальной стадии. Примерно у 50% больных отмечают спленомегалию, артралгии, иногда нейропатии.
Поражение печени. Самый постоянный признак гемохроматоза. При пункционной биопсии обнаруживаются микронодулярный цирроз, большое количество зерен железа в печеночных и купферовских клетках, явления фиброза. Позднее присоединяется асцит, появляются «голова медузы», кровотечения из расширенных вен пищевода.
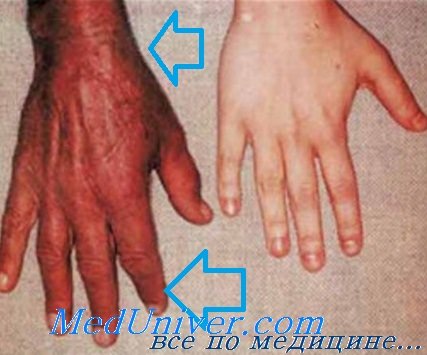
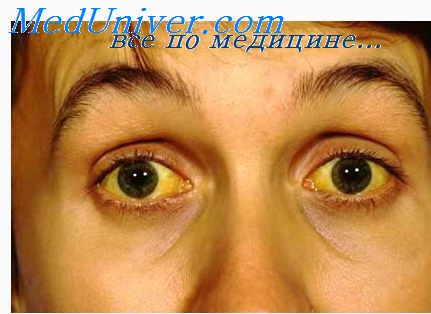
Поражения кожи. Меланоз кожи возникает на открытых участках, половых органах, в области крупных складок и старых рубцов. На пике заболевания пигментируется весь кожный покров. Пигментация варьирует от грязно-бурой до бронзовой, аспидной, иногда она может предшествовать развитию других симптомов за несколько лет. Кожа сухая, истонченная, с небольшим шелушением. В отличие от болезни Аддисона, слизистые оболочки в процесс вовлекаются редко, обнаруживается пигментация слизистых глаз, полости рта и гениталий.
По другим данным, слизистые поражаются в пятой части случаев. Также могут наблюдаться кожный зуд, атрофия кожи, ихтиозиформные изменения, алопеция, койлонихия, эритема ладоней, паукообразные гемангиомы.
Кардиальные проявления. Несмотря на то что отложения железа в сердце при наследственном гемохроматозе имеются в 90—100% случаев, клиническая симптоматика выявляется у трети больных. Поражение сердца может быть бессимптомным, однако выявляется, как правило, при углубленных исследованиях или провокационных пробах. Дисфункция миокарда обычно проявляется хронической застойной недостаточностью.
Эндокринные нарушения. Сахарный диабет может быть латентным, обычно он развивается на поздних стадиях болезни. Отмечается резистентность диабета к терапии. В результате гиперэстрогенемии у мужчин может развиться оволосение лобка по женскому типу, гипогонадизм, гинекомастия, снижение либидо.
Гистология кожи. Обнаруживают повышенное содержание меланина в базальном слое эпидермиса, отложение гемосидерина преимущественно вокруг сосудов, потовых желез.
Диагноз ставят на основании характерных клинических признаков, повышенной концентрации железа в сыворотке крови и определения процента насыщения трансферрина, концентрации ферритина. В классическом варианте и развернутой форме заболевание встречается не часто, но даже при наличии типичной клинической картины не редко диагностируется только на аутопсии или в случаях внезапной смерти при судебно-медицинских вскрытиях.
Течение и прогноз. Заболевание длительно протекает скрытно. Клинические признаки возникают обычно после 40 лет. Частая причина смерти — печеночная недостаточность вследствие цирроза печени, кровотечения из расширенных вен пищевода.
Лечение у терапевтов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гемохроматоз
Что такое гемохроматоз?
Гемохроматоз — это преимущественно наследственное заболевание с накоплением железа и отложением его в тканях. Болезнь еще называется бронзовым диабетом из-за отложения в коже железосодержащего пигмента гемосидерина.
Также железо накапливается в печени, сердце, поджелудочной железе, селезенке, железах эндокринной системы, что вызывает их постепенное разрушение. Чаще всего гемохроматоз врожденный, но иногда встречается вторичный гемохроматоз — у пациентов с болезнями печени, крови, нарушениями обмена веществ или при передозировке препаратов железа.
Симптомы гемохроматоза
При врожденном гемохроматозе признаки болезни появляются у взрослых людей, когда в организме уже накоплено более 20-40 г железа. Первые симптомы — это сильная утомляемость, ослабление полового влечения, потеря веса. Затем присоединяются:
В развернутой стадии болезни обнаруживают поражение внутренних органов с развитием:
Гемохроматоз может привести к смерти больного из-за развития осложнений: кровотечения из расширенных вен пищевода (при циррозе печени), диабетической комы, острого мозгового нарушения кровообращения, сепсиса, рака печени.
Причины появления гемохроматоза
Наследственное генетическое нарушение обмена железа возникает при мутации гена HFE короткого плеча 6-ой хромосомы. Этот ген отвечает за формирование сигнала о недостатке железа в организме. Если ген поврежден, то возникает ложный сигнал и начинает активно вырабатываться железосвязывающий белок, усиливается всасывание железа из пищи.
При этой болезни за год накапливается от 0,5 до 1 г железа. Вначале оно откладывается в виде белковых ферритиновых комплексов, но затем ферритина уже не хватает и железо (сильный окислитель) начинает разрушать органы. На месте такого разрушения образуется соединительная ткань вместо работающей (фиброз и цирроз).
При приобретенном гемохроматозе возникает избыток железа из-за его передозировки (переливание крови, препараты), нарушения обмена в печени.
Первичный и вторичный гемохроматоз
Первичный гемохроматоз — это самостоятельное врожденное заболевание из-за генетического дефекта. Он бывает 4 видов:
Вторичный гемохроматоз всегда возникает на фоне другой болезни:
Спровоцировать усиленное накопление железа может и низкобелковая диета, бесконтрольное применение железа в препаратах или/и добавках, частые переливания крови, неправильное лечение препаратами железа.
Факторы риска при гемохроматозе
Вероятность развития гемохроматоза выше у людей:
Диагностика
Диагноз гемохроматоза ставят на основании типичной клиники и при обнаружении отклонений в анализах крови:
Для подтверждения наследственного происхождения гемохроматоза проводится молекулярно-генетическая диагностика методом ПЦР в реальном времени. Дополнительно исследуют состояние печени (печеночные пробы, УЗИ, биопсия, МРТ), уровень глюкозы и гликированного гемоглобина, изменения миокарда (ЭКГ, ЭхоКГ).
Лечение гемохроматоза
Основные принципы терапии:
Одновременно проводится лечение пораженных органов. У пациентов с распространенным циррозом печени решается вопрос о пересадке органа.
Гемохроматоз
Общие сведения
Гемохроматоз (синдром перегрузки железом, бронзовый диабет, HFE-гемохроматоз, гемомеланоз, пигментный цирроз печени, сидерофилия) — болезнь накопления железа, обусловленная повышенным всасыванием его в кишечнике, что способствует массивному накоплению железа в различных тканях (печени, сердца, поджелудочной железы, эндокринных желез, селезёнки, коже) и их повреждению (фиброзу) с последующим развитием недостаточности.
Железо относится к одному из важнейших биохимических компонентов, принимающим участие в метаболическом обмене, но в тоже время он является потенциально токсичным микроэлементом, вызывающим окислительные повреждения нуклеиновых кислот. Соответственно процесс гомеостаза в организме человека железа жестко регулируется, подвергаясь процессу рециркуляции путем захватывания/разрушения состарившихся эритроцитов макрофагами печени/селезенки, то есть осуществляется деградация гемоглобина и, соответственно, освобождение железа, которое связывается с ферритином/трансферрином и утилизируется.
Физиологические потери железа в сутки варьируют в пределах 1-2 мг и восполняются естественным путем (употреблением железосодержащих продуктов и всасыванием эквивалентного количества в желудке). Процесс всасывания железа происходит в двенадцатиперстной кишке/начальных отделах тощей кишки и контролируется белками-регуляторами обмена железа. В то время, как избыточное поступление в кровь железа (переливании крови/парентеральное введении препаратов железа) механизма контроля не имеет.
Термин «гемохроматоз» в настоящее время используется преимущественно в контексте клинико-патологического синдрома, который может быть обусловлен как генетически-детерминированным переизбытком железа в организме, так и другими причинами.
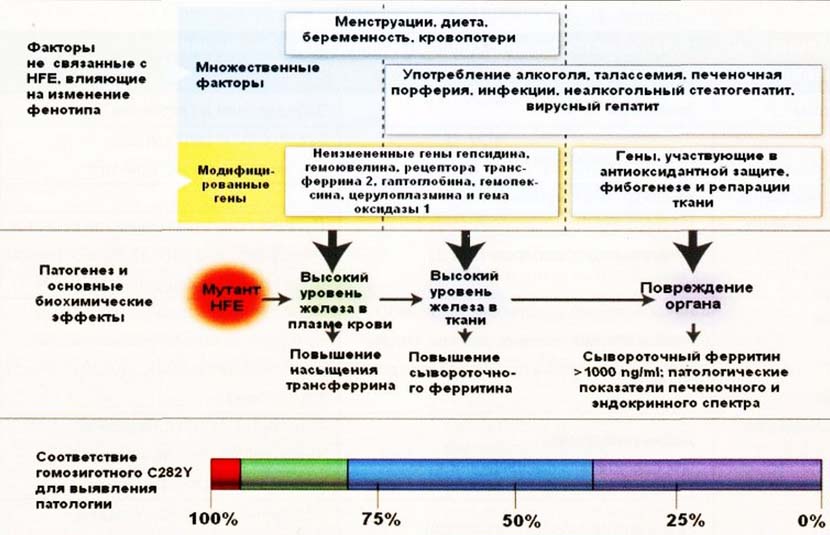
Классический, вызываемый мутацией HFE-гена (C282Y/H63D) представляет собой ступенчатый процесс, начинающийся нарушением процесса насыщения трансферрина, продолжается увеличением сывороточного ферритина и завершающийся конечной стадией — депонированием в жизненно важных органах железа с формированием фиброза/цирроза.
Распространенность наследственного гемохроматоза формы СПЖ варьирует в пределах от 1:1000 до 1:5000 человек. У лиц мужского пола гемохроматоз встречается в 5-7 раз чаще, чем у женщин. При этом у них встречаются чаще тяжелые формы заболевания, протекающие с осложнениями. Манифестирует заболевание преимущественно в возрасте 30-50 лет. Вторичный гемохроматоз встречается у лиц с болезнями печени и гемоглобинопатиями. Гемохроматоз начинает проявляться не сразу, а лишь после того, как переизбыток железа в организме достигает общего содержания железа 20-40 г. Симптомы переизбытка железа в организме манифестируют классическим симптомокомплексом: циррозом печени, пигментацией кожных покровов/слизистых оболочек, сахарным диабетом. Бронзовый диабет сопровождается высокой вероятностью развития гепатоцеллюлярной карциномы (первичного рака печени).
Следует сказать и о накоплении пигмента железа в клетках кожи (болезнь Майокки, болезнь Шамберга, Гужеро-Блюма). Однако, эти заболевания, например, болезнь Шамберга (гемосидероз кожи) имеют совершенно другой патогенез и причины развития. Характерно преимущественно токсико-аллергическое поражения капилляров или наличие эндокринной патологии различного генеза, например, если в организме имеется избыток гормонов щитовидной железы.
Заболевание связано с поражением стенок капилляров кожи, вызывающее увеличение их проницаемости, что способствует превращению железа, вышедшего из гемоглобина сосудистого русла в пигмент гемосидерин, который обуславливает появление специфических коричневого цвета пятен на коже.
Патогенез
Патогенетический механизм врождённого и приобретённого гемохроматоза совершенно различный, также как и патогенез типов в каждой из этих групп. В основе патогенеза врожденного гемохроматоза лежат мутации генов, которые ответственны за синтез белков, принимающих участие в процессе метаболизма железа. Это приводит к разбалансировке процессов поступления и выведения железа, сопровождаемой расстройством насыщения трансферрина, ростом сывороточного ферритина, что приводит к появлению в крови свободного железа.
Патологический процесс завершается накоплением железа в тканях организма и токсическим повреждением органов. Высокая реакционно-токсическая способность ионов железа вызывает оксидативный стресс и инициирует развитие процессов перекисного окисления липидов, что вызывает повреждение клеточных структур (ДНК, мембраны, органелл). Соответственно поражение кардиомиоцитов вызывает токсическую кардиомиопатию; гепатоцитов — фиброз (разрастание коллагена); клеток поджелудочной железы — сахарный диабет; гипофиза — клеток, вырабатывающих гормоны (гонадотропины), регулирующие репродуктивную функцию; клеток эпидермиса — образование пигмента меланина. Наиболее часто поражаемыми органами-мишенями являются печень, поджелудочная железа, сердце, гонады, суставы, гипофиз.
Ниже схематически показана структура патогенеза первичного HFE-ассоциированный гемохроматоза.
Классификация
Различают классический (первичный), генетически обусловленный гемохроматоз и приобретенный (вторичный) гемохроматоз.
Врожденный гемохроматоз в соответствии с типом мутации представлен несколькими типами:
Вторичный гемохроматоз представлен несколькими видами:
Причины
Причиной наследственного гемохроматоза являются мутации HFE-гена, локализованного в 6 хромосоме на ее на коротком плече. Тип передачи — аутосомно-рецессивный. Мутации вызывают нарушение процесса захвата железа клетками 12-перстной кишки, что приводит к формированию ложного сигнала о недостаточном содержании железа в организме. Это способствует увеличению процесса синтеза энтероцитами железосвязывающего белка и резкому усилению абсорбции железа в кишечнике (на фоне нормального поступлении с пищей). Чрезмерное отложение гемосидерина (железосодержащего пигмента) происходящее в различных внутренних органах, и мягких тканях, вызывает гибель функционально активных элементов с постепенным развитием фиброзно-склеротических процессов.
Причиной развития вторичного гемохроматоза является, как правило, избыточное поступления экзогенного железа в организм (частых гемотрансфузиях, потреблении железа с водой/пищей, неконтролируемом приеме препаратов железа), а также расстройства метаболизма, заболевания крови (талассемии), злокачественные новообразования, низкобелковые диеты, заболевания печени (гепатиты, цирроз).
Симптомы
Симптомы гемохроматоза от начала патологического накопления железа манифестируют не сразу, обычно, клинические признаки появляются через несколько лет. При первичном гемохроматозе клиническая картина более выражен, поскольку переизбыток железа в организме существенно выше. Гемомеланоз развивается в несколько стадий:
Клиническая манифестация приходится преимущественно на зрелый возраст, что обусловлено достижением критических значений содержания в организме общего железа (избыток железа в крови достигает значений 20-40 г). В клинической симптоматике могут преобладать те или иные синдромы, в соответствии с чем выделяют гепатопатическую, кардиопатическую и эндокринологическую формы заболевания.
Для начальной стадии характерны неспецифичные жалобы, проявляющиеся общей слабостью, повышенной утомляемостью, снижением массы тела и либидо. Пациентов могут беспокоить сухость кожных покровов и слизистых, боли в правом подреберье, выраженные артралгии, вызванные хондрокальцинозом крупных суставов. По мере развития формируется классический симптомокомплекс, который манифестирует:
Симптомы переизбытка железа в организме в позднем периоде проявляются кахексией, асцитом, портальной гипертензией, выраженным увеличение печени/селезенки. Летальный исход наступает преимущественно вследствие острой сердечной недостаточности, печеночной недостаточности, диабетической комы, кровотечения из варикозных вен пищевода, асептического перитонита и сепсиса.
Анализы и диагностика
Постановка диагноза осуществляется на основе сбора анамнеза, клинических проявлений и данных лабораторных исследований, в качестве которых используются:
При поражение внутренних органов может назначаться МРТ/КТ печени, УЗИ органов брюшной полости, ЭКГ, рентгенография суставов.
Лечение
Лечение направлено на удаление избытка железа из организма и минимизацию риска развития необратимого поражения органов и тканей.
Кровопускания
Традиционным методом лечения являются кровопускания, которое проводится пожизненно. Начальный курс составляет одну процедуру в неделю в объеме 500 мл. После достижения снижения уровня гемоглобина на 15-20 г/л, а показаний сывороточного ферритина до 20-40 нг/мл вводится этап поддерживающей терапии – кровопусканию по 500 мл крови один раз в 2-4 месяца у лиц мужского пола и каждые 3-6 месяцев для лиц женского пола. Противопоказаниями к кровопусканиям является сердечная недостаточность, анемии, болезни печени.
Хелатирующая терапия. При невозможности поведения кровопусканий назначают хелатирующее лечение, в основе назначение лекарственных средств из группы комплексонов, связывающих избыток железа в сыворотке крови/тканях и выводящие ионы железа из организма с мочой и фекалиями — дефероксамин (Десферал), деферазирокс (Эксиджад).
Однако, с учетом короткого периода полураспада этих препаратов, необходимо медленное их введение: 3-4 часовые инфузии внутривенно или 12/24 часовые инфузии подкожно через специальные помпы. Одновременно назначаются препараты для симптоматической терапии, при необходимости проводится лечение сердечной недостаточности, цирроза печени, гипогонадизма, сахарного диабета.
В основе определения эффективности лечения — динамика клинических /лабораторных данных. Как правило, состояние пациентов после курса кровопусканий начинает улучшаться: уменьшаются размеры печени, купируется симптоматика кардиомиопатии и сахарного диабета, исчезает сонливость, утомляемость, слабость.
Гемохроматоз
Что провоцирует / Причины Гемохроматоза:
Впервые заболевание было описано М. Troisier в 1871 г. как симптомокомплекс, характеризующийся сахарным диабетом, пигментацией кожи, циррозом печени, связанным с накоплением железа в организме. В 1889 г. Reclinghausen ввел термин «гемохроматоз», отражающий одну из особенностей болезни: необычную окраску кожи и внутренних органов. Было установлено, что железо вначале накапливается в паренхиматозных клетках печени, а затем может откладываться и в других органах (поджелудочной железе, сердце, суставах, гипофизе).
Патогенез (что происходит?) во время Гемохроматоза:
В норме в организме содержится около 4 г железа, из них г в составе гемоглобина, миоглобина, каталазы и других дыхатель-bix пигментов или ферментов. Запасы железа составляют 0,5 г, из них часть находятся в печени, но при гистологическом исследовании на железо обычными методами они не видны. В норме дневной рацион человека содержит около 10-20 мг железа (90 % в свободном стоянии, 10 % в соединении с гемом), из которых всасывается 1-1,5 мг.
Количество всосавшегося железа зависит от его запасов в организме: чем выше потребность, тем больше железа всасывается. Всасывание происходит главным образом в верхних отделах тонкой кишки и является активным процессом, при котором железо может переноситься далее против градиента концентрации. Однако механизмы переноса неизвестны.
При гемохроматозе всасывание железа в пищеварительном тракте увеличивается до 3,0-4,0 мг. Таким образом, в течение 1 года его избыточное количество, откладывающееся в клетках печени, поджелудочной железы, сердца и других органах и тканях, составляет примерно 1 г. В конечном итоге внутри- и внеклеточные пулы организма становятся перенасыщенными железом, что позволяет свободному железу вступать в токсические внутриклеточные реакции. Являясь сильным окислительно-восстановительным веществом, железо создает свободные гидроксильные радикалы, которые, в свою очередь, разрушают макромолекулы липидов, белков и ДНК.
Повышенное накопление железа в печени характеризуется:
Заболевание связано с так называемыми миссенс-мутациями, т. е. мутациями, вызывающими изменение смысла кодона и приводящими к остановке биосинтеза белка.
Генетическая природа ПГХ подтверждена М. Simon и соавт. в 1976 г., выявившими у представителей европейской популяции тесную ассоциацию заболевания с определенными антигенами главного комплекса гистосовместимости. Для клинической экспрессии необходимо наличие у больного двух аллелей ПГХ (гомозиготность). Присутствие одного общего с больным HLA-гаплотипа указывает на гетерозиготное носительство аллели ПГХ. У таких лиц могут обнаруживаться косвенные признаки, указывающие на повышенное содержание железа в организме, и отсутствие клинически значимых симптомов. Гетерозиготное носительство гена преобладает над гомозиготным. В случае если оба родителя являются гетерозиготами, возможен псевдодоминантный тип наследования. У гетерозигот абсорбция железа обычно несколько повышена, выявляется небольшое увеличение железа в сыворотке крови, однако опасной для жизни перегрузки микроэлементом не наблюдается. В то же время если гетерозиготы страдают другими заболеваниями, сопровождающимися нарушениями обмена железа, то возможно появление клинико-морфологических признаков патологического процесса.
Тесная связь заболевания с HLA-антигенами позволила локализовать ген, ответственный за ПГХ, расположенный на коротком плече хромосомы 6, вблизи локуса А системы HLA и связанный с аллелем A3 и гаплотипами A3 В7 или A3 В14. Данный факт послужил основанием для исследований, направленных на его идентификацию.
Наследственный гемохроматоз первоначально считался простым моногенным заболеванием. В настоящее время по генному дефекту и клинической картине выделяют 4 формы ПГХ:
Идентификация гена HFE (ассоциированного с развитием гемохрома-тоза) явилась важным моментом в понимании сущности заболевания. Ген HFE кодирует структуру протеина, состоящего из 343 аминокислот, строение которого сходно с молекулой системы МНС класса I. лиц, страдающих гемохроматозом, выявлены мутации в этом гене. Носители аллеля C282Y в гомозиготном состоянии среди этнических русских насчитывается не менее 1 на 1000 человек. О роли HFE в метаболизме железа свидетельствует взаимодействие HFE с рецептором трансферрина (TfR). Ассоциация HFE с TfR снижает сродство этого рецептора к трансферрину, связанному с железом. При мутации С282У HFE вообще не способен связываться с TfR, а при мутации H63D аффинность к TfR снижается в меньшей степени. Трехмерная структура HFE была исследована при помощи рентгеновской кристаллографии, что дало повод установить характер взаимодействия между HFE и легкой цепью 2т, а также определить локализацию мутаций, характерных для гемохроматоза.
Мутация С282У приводит к разрыву дисульфидной связи в домене, имеющем важное значение в формировании правильной пространственной структуры белка и его связывания с 2т. Наибольшее количество белка HFE вырабатывается в глубоких криптах двенадцатиперстной кишки. В норме роль белка HFE в крип-тонных клетках заключается в модуляции захвата железа, связанного с трансферрином. У здорового человека повышение уровня сывороточного железа приводит к повышению его захвата глубокими клетками крипт (процесс опосредован TfR и модулируется HFE). Мутация C282Y может нарушить TfR-опосредованный захват железа криптальными клетками и, таким образом, формировать ложный сигнал о наличии низкого содержания железа в организме.
Из-за снижения содержания внутриклеточного железа дифференцирующиеся энтероциты, мигрирующие к вершине ворсинок, начинают вырабатывать повышенное количество DMT-1, в результате чего усиливается захват железа. Основным звеном патогенеза является генетический дефект ферментных систем, регулирующих всасывание железа в кишечнике при нормальном поступлении его с пищей. Доказана генетическая связь с системой HLA-A. Исследование неравновесности сцепления с использованием этих маркеров показало связь гемохроматоза с Аз, В7, Bt4, D6 Siosh D6 S126O.
Потенциальная токсичность объясняется его способностью как металла с переменной валентностью запускать ценные свободнорадикальные реакции, приводящие к токсическому повреждению органелл и генетических структур клетки, повышенному синтезу коллагена и развитию опухолей. У гетерозигот выявляют небольшое повышение уровня железа в сыворотке крови, но не обнаруживают избыточного накопления железа или повреждения тканей.
Однако это может произойти, если гетерозиготы страдают и другими заболеваниями, сопровождающимися нарушениями обмена железа.
Вторичный гемохроматоз чаще развивается на фоне заболеваний крови, поздней кожной порфирии, частых гемотрансфузий, приема железосодержащих препаратов.
Симптомы Гемохроматоза:
Особенности клинических проявлений:
Клинические проявления заболевания развиваются после наступления зрелого возраста, когда запасы железа в организме достигают 20-40 г и более.
В развитии заболевания различают три стадии:
Начало болезни постепенное. В начальной стадии на протяжении ряда лет преобладают жалобы на выраженную слабость, утомляемость, похудение, снижение половой функции у мужчин. Часто отмечается боль в правом подреберье, суставах в связи с хондрокальцинозом крупных суставов, сухость и атрофические изменения кожи, яичек.
Развернутая стадия заболевания характеризуется классической триадой. пигментацией кожи, слизистых оболочек, циррозом печени и диабетом.
У большинства пациентов железо в первую очередь откладывается в печени. Увеличение печени наблюдается почти у всех больных. Консистенция печени плотная, поверхность гладкая, в ряде случаев отдается ее болезненность при пальпации. Спленомегалия выявляйся у 25-50 % больных. Внепеченочные знаки встречаются редко Парный диабет наблюдается у 80 % больных. Часто он инсулин-зависимый.
Наблюдаются эндокринные расстройства в виде гипофункции гипофиза, эпифиза, надпочечников, щитовидной железы (1/3 больных) половых желез. Различные виды эндокринопатий встречаются более чем у 80 % больных. Самой частой формой патологии является сахарный диабет.
Отложение железа в сердце при ПГХ наблюдается в 90-100 % случаев, однако клинические проявления поражения сердца обнаруживаются лишь у 25-35 % больных. Кардиомиопатия сопровождается увеличением размеров сердца, нарушениями ритма, постепенным развитием рефрактерной сердечной недостаточности.
Возможно сочетание гемохроматоза с артропатией, хондрокальцинозом, остеопорозом с кальциурией, нервно-психическими расстройствами, туберкулезом, поздней кожной порфирией.
Выделяют латентный (включающий больных с генетической предрасположенностью и минимальной перегрузкой железом), с выраженными клиническими проявлениями, и терминальный гемохроматоз. Чаще встречаются гепатопатическая, кардиопатическая, эндокринологическая формы: соответственно, медленно прогрессирующая, быстро-прогрессирующая и форма с молниеносным течением.
Латентная стадия ПГХ наблюдается у 30-40 % больных, что выявляется в ходе семейно-генетического обследования родственников пациентов или при популяционном скрининге. У части указанных лиц старшей возрастной группы имеются минимальная симптоматика в виде незначительной слабости, повышенной утомляемости, чувства тяжести в правом подреберье, пигментации кожных покровов на открытых участках тела, снижения либидо, незначительной гепатомегалии.
Стадия развернутых клинических проявлений характеризуется наличием астеновегетативного синдрома, абдоминальной боли, иногда довольно интенсивной, артралгий, снижением либидо и потенции у 50 % мужчин и аменореей у 40 % женщин. Кроме того, могут наблюдаться потеря массы тела, кардиалгии и сердцебиение. При объективном обследовании выявляются гепатомегалия, меланодермия, нарушение функции поджелудочной железы (инсулинзависимый сахарный диабет).
В терминальной стадии ПГХ наблюдаются признаки декомпенсации органов и систем в виде формирования портальной гипертензйй, развития печеночно-клеточной, а также право- и левожелудочковой сердечной недостаточности, диабетической комы, истощения. Причинами смерти таких больных, как правило, являются кровотечения из варикозно расширенных вен пищевода, печеночно-клеточная и сердечная недостаточность, асептический перитонит, диабетическая кома.
У таких пациентов существует предрасположенность к развитию опухолевого процесса (риск его развития у лиц старше 55 лет повышается в 13 раз по сравнению с общей популяцией).
Диагностика Гемохроматоза:
Особенности диагностики:
Диагностика основывается на множественных органных поражениях, случаях заболевания у нескольких членов одной семьи, повышенном содержании железа, экскреции железа с мочой, высокой концентрации трансферрина, ферритина в сыворотке крови. Диагноз вероятен при сочетании с сахарным диабетом, кардиомиопатией, гипогонадизмом и типичной кожной пигментацией. Лабораторными критериями служат гиперферремия, повышение индекса насыщения трансферрина (более 45 %). Резко увеличиваются уровень ферритина в сыворотке крови, экскреция железа с мочой (десфераловая проба). После внутримышечного введения 0,5 г десферала выделение железа возрастает до 10 мг/сут (при норме 1,5 мг/сут), коэффициент НТЖ (железо/ОЖСС) повышается. С внедрением в практику генетического тестирования увеличилось количество лиц с наличием гемохроматоза без клинических признаков перегрузки железом. Проводят исследование на наличие мутаций C282Y/H63D в группе риска по развитию перегрузки железом. Если пациент является гомозиготным носителем C282Y/H63D, диагноз наследственного гемохроматоза может считаться установленным.
Среди неинвазивных методов исследования депонирование микроэлемента в печени может быть определено с помощью МРТ. В основе метода лежит снижение интенсивности сигнала печени, перегруженной железом. При этом степень снижения интенсивности сигнала пропорциональна запасам железа. Метод позволяет определить избыточное отложение железа в поджелудочной железе, сердце и других органах.
При биопсии печени наблюдается обильное отложение железа, дающего положительную реакцию Перлса. При спектрофотометрическом исследовании содержание железа составляет свыше 1,5 % от сухой массы печени. Важное значение придается количественному измерению уровня железа в биоптатах печени методом атомно-абсорбционной спектрометрии с последующим исчислением печеночного индекса железа. Индекс представляет соотношение концентрации железа в печени (в мкмоль/г сухого веса) возрасту больного (в годах). При ПГХ уже на ранних стадиях этот показатель равен или превышает 1,9-2,0 и не достигает указанной величины при других состояниях, характеризующихся гемосидерозом печени.
В латентной стадии заболевания функциональные пробы печени практически не изменяются, а по данным гистологического исследования, наблюдаются гемосидероз 4-й степени, фиброз портальных трактов без выраженных признаков воспалительной инфильтрации.
На стадии развернутых клинических проявлений гистологические изменения печени обычно соответствуют пигментному септальному или мелкоузловому циррозу с массивными депозитами гемосидерина в гепатоцитах и менее значительными в макрофагах, эпителии желчных протоков.
При гистологическом исследовании в терминальной стадии заболевания выявляется картина генерализованного гемосидероза с поражением печени (по типу моно- и мультилобулярного цирроза), сердца, поджелудочной, щитовидной, слюнных и потовых желез, надпочечников, гипофиза и других органов.
Перегрузка железом наблюдается при ряде врожденных или приобретенных состояний с которыми необходимо дифференцировать ПГХ.
Классификация и причины развития состояния перегрузки железом:
Заболевание необходимо также дифференцировать с патологией крови (талассемия, сидеробластная анемия, наследственная атрансферри-немия, микроцитарная анемия, поздняя кожная порфирия), заболеваниями печени (алкогольное поражение печени, хронический вирусный гепатит, неалкогольный стеатогепатит).
Лечение Гемохроматоза:
Особенности лечения гемохроматоза:
Показана диета, богатая белками, без продуктов, содержащих железо.
Наиболее доступным способом удаления избытка железа из организма являются кровопускания. Обычно удаляется 300-500 мл крови с частотой 1-2 раза в неделю. Число кровопусканий рассчитывается в зависимости от уровня гемоглобина, гематокрита крови, ферритина, величины избытка железа. При этом учитывается, что в 500 мл крови содержится 200-250 мг железа, главным образом в составе гемоглобина эритроцитов. Кровопускания продолжают до развития у больного анемии легкой степени. Модификацией данной экстракорпоральной методики является цитаферез (ЦА) (удаление клеточной части крови с возвратом аутоплазмы в замкнутом контуре). Кроме механического удаления форменных элементов крови, ЦА обладает детоксикационным действием и способствует уменьшению выраженности дегенеративно-воспалительных процессов. Каждому больному проводится 8-10 сеансов ЦА с дальнейшим переходом на поддерживающую терапию с использованием ЦА или гемоэксфузий в количестве 2-3 сеансов в течение 3 мес.
Медикаментозное лечение основано на использовании дефероксамина (десферал, десферин) по 10 мл 10 % раствора внутримышечно или внутривенно капельно. Препарат обладает высокой специфической активностью к ионам Fe3+. При этом 500 мг десферала способны Удалить из организма 42,5 мг железа. Длительность курса составляет 20-40 дней. Одновременно проводят лечение цирроза, сахарного диабета и сердечной недостаточности. Часто наблюдаемый анемический синдром у больных ПГХ при наличии избыточного содержания железа в ткани печени ограничивает применение эфферентной терапии. В нашей клинике разработана схема применения рекомбинантного эритропоэтина на фоне ЦА. Препарат способствует повышенной утилизации железа из депо организма, за счет чего происходит снижение общих запасов микроэлемента, повышение уровня гемоглобина. Реомбинантный эритропоэтин вводится в дозе 25 мкг/кг массы тела на фоне сеансов ЦА, проводимых 2 раза в неделю в течение 10-15 нед.
Прогноз:
Прогноз определяется степенью и длительностью перегрузок.