Блуждающий нерв и сон
Блуждающий нерв и сон
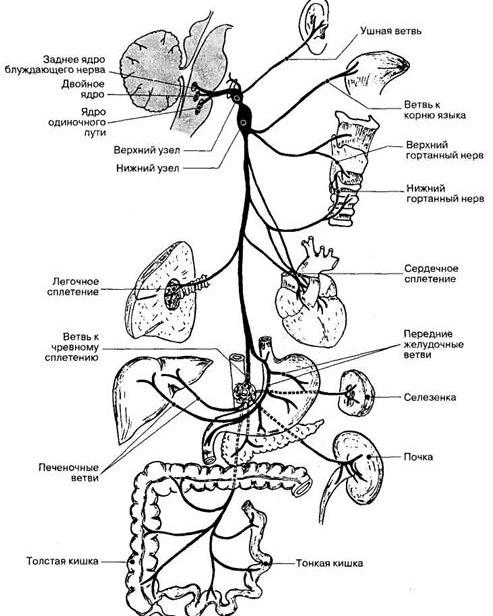
Блуждающий нерв выходит из полости черепа через яремное отверстие вместе с языкоглоточным и добавочным нервами, на шее располагается в сосудисто-нервном пучке, где соседствует с внутренней яремной веной, общей и внутренней сонными артериями, нервами каудальной группы. Проникает в грудную полость через верхнее отверстие грудной клетки, где правый блуждающий нерв лежит впереди подключичной артерии, а левый располагается на передней поверхности дуги аорты. Пройдя через заднее средостение, левый и правый блуждающие нервы образуют пищеводное сплетение, из которого формируются передний и задний стволы блуждающего нерва, которые через пищеводное отверстие диафрагмы спускаются в брюшную полость, формируя здесь ряд сплетений.
Дендриты клеток нижнего узла вместе с ветвями языкоглоточного нерва формируют глоточное сплетение (pl. pharyngeus), осуществляющее иннервацию слизистой оболочки глотки. Верхний гортанный нерв (n. laryngeus superior), пройдя позади внутренней сонной артерии, подходит к слизистой оболочке гортани выше голосовой связки, к слизистой надгортанника, частично к корню языка.
Из нижнего чувствительного узла блуждающего нерва осуществляется также иннервация бронхов, околосердечной сумки. В составе блуждающего нерва проходят чувствительные волокна для пищевода, желудочно-кишечного тракта, печени, почек.
Семиотика поражения блуждающего нерва. Синдром Арнольда
Жалобы больного при поражении блуждающего нерва самые разнообразные. Ими могут быть нарушение проглатывания жидкой пищи, попадание ее в нос, утрата звучности голоса и др.
При поражении чувствительных веточек блуждающего нерва имеет место болевой синдром. Описана невралгия верхнего гортанного нерва. В повседневной практике врача она встречается довольно редко. Причиной ее служат воспалительные процессы в гортани, струмэктомия, тонзилэктомия. Невралгия характеризуется болевыми пароксизмами в области гортани. Боли односторонние, часто возникают во время еды или глотания, иррадиируют вдоль нижней челюсти, в ухо. Болевая точка располагается на боковой поверхности шеи, чуть выше щитовидного хряща. Во время приступа боли возникает кашель, общая слабость (Гречко В.Е., 1981). Приступы кашля автор объясняет повышенной чувствительностью слизистой гортани и трахеи. При длительно существующей невралгии верхнего гортанного нерва снижается и исчезает глоточный рефлекс. Пораженная сторона гортани становится неподвижной, может появиться сужение голосовой щели.
Нам пришлось наблюдать невралгию ушной веточки (r. auricularis). Причиной развития заболевания явилось сильное охлаждение, кариозные зубы. Боль носила постоянный характер, локализовалась в верхнебоковых отделах шеи, распространялась в подчелюстную область, в ухо, особенно в область слухового прохода, заушную зону. На фоне постоянных болей возникали приступы труднопереносимых болей с преимущественной локализацией в подчелюстной зоне и в наружном слуховом проходе.
На функциональное единство висцеральных волокон блуждающего, диафрагмального нервов и задних рогов шейных сегментов указывают в своей монографии М.Б. Кроль, Е.А. Федорова, 1966. Боли, как подчеркивают авторы, носят невралгический характер, возникают внезапно, стреляющие, кратковременные, не совпадают с зонами Захарьина-Геда для конкретного органа. В момент пароксизма обнаруживается гиперестезия в месте максимальной боли. Вне приступа нарушений чувствительности не обнаруживается (в зонах Захарьина-Геда расстройства чувствительности носят стойкий характер). Приведенные данные надо иметь в виду всегда, когда мы сталкиваемся с болевым синдромом, который не укладывается в рамки обычных невралгий.
При изолированном поражении блуждающего нерва речь больного приобретает носовой оттенок, на стороне очага мягкое небо свисает, малоподвижно или неподвижно, язычок отклоняется в здоровую сторону. Небный рефлекс отсутствует. Необходимо иметь в виду, что у больных с хроническим или острым тонзиллитом, курильщиков нередко отсутствуют небные рефлексы, язычок может отклоняться. При этом он обычно гиперемирован, припухший (увеличен в размерах).
При выключении функции отдельных веточек блуждающего нерва может развиться паралич гортани. В этом случае голосовая связка на стороне очага занимает срединное положение, не сокращается при фонации и дыхании, голос становится хриплым. При процессах в области шеи может страдать верхний гортанный нерв. При этом кроме анестезии слизистой оболочки гортани нарушается функция m. cricothyreoidei, напрягающей голосовую связку. Голос становится низким, грубым.
Нижний гортанный нерв (возвратный) чаще поражается при опухолях средостения, аневризмах аорты, сонной или подключичной артерий, опухолях шеи. Вследствие паралича мышц гортани (кроме m. cricothyreoidei) у больных развивается афония. При двустороннем параличе возвратных нервов наступает резкое затруднение дыхания из-за смыкания голосовых связок в результате паралича mm. cricoarytaenoidei postici, расширяющих голосовую щель.
Раздражение блуждающего нерва и его ветвей вызывает замедление сердечной деятельности, усиление перистальтики кишечника, сужение бронхов, расширение сосудов. Волокна, замедляющие сердечную деятельность, берут начало от отдельной клеточной группы, расположенной вблизи вентрального соматического ядра блуждающего нерва, затем проходят в общем стволе X пары, заканчиваются в сердечных узлах, откуда берут начало постганглионарные волокна к сердечной мышце.
Блуждающий нерв или «зри в корень»
Блуждающий нерв – работа внутренних органов
Почему медикаментозное лечение внутренних органов нередко является безрезультатным?
Мы часто удивляемся…. Как же так? Я виду здоровый образ жизни, не пью, не курю, не злоупотребляю жирной и жареной пищей, а у меня болит живот. И вот мы идем к врачу с жалобами на боль в эпигастрии, расстройство кишечника, тяжесть в животе…
Очень часто, проблемы с желудочно-кишечным трактом не связаны с самими внутренними органами… а связаны с нарушениями в «центре управления» (нервной системе), а точнее с нарушением коммуникаций между «центром» и «исполнителями» (внутренними органами).
Человеческая нервная система условно делится на центральную нервную систему и вегетативную.
Вегетативная (дословно переводится как растительная) – обеспечивает работу внутренних органов – дыхание, пищеварение, секреторная функция желез, регулирование давления и т.д. благодаря вегетативной системе, мы не думаем, как дышать, или переваривать пищу, это происходит как-то само по себе.
Вегетативная нервная система в свою очередь, тоже делится на симпатическую и парасимпатическую системы. Эти системы противостоят друг – другу.
Симпатическая нервная система отвечает за готовность человека к охоте, атаке или уходу от погони – она стимулирует повышение давления, учащение дыхания и сердечных сокращений, подавляя при этом деятельность желудочно-кишечного тракта.
Парасимпатическая нервная система отвечает за «отдых» человека, активизирует работу желудочно-кишечного тракта и секреторную функцию желез пищеварения, успокаивая дыхание, сердцебиение и понижая давление.
Основным нервом парасимпатической нервной системы является блуждающий нерв.
Это нерв, который выходит из яремного отверстия черепа и спускается по шее в грудную и брюшную полости, отдавая свои веточки внутренним органам. К сожалению, именно этот нерв очень часто ущемляется на разных участках своего пути (на уровне яремного отверстия, апертуры грудной клетки, грудобрюшной диафрагмы).
В результате ущемление блуждающего нерва, симпатическая нервная система начинает доминировать, угнетая деятельность желудочно-кишечного тракта…
Пища плохо переваривается, нарушается перистальтика кишечника, секреция поджелудочной железы и самого желудка…. Общее самочуствие ухудшается, беспокоит тяжесть в области желудка, ощущение переполнения даже при принятии небольшого количества пищи, нередко может сопровождаться разлитой тупой болью в левом пореберье, левом боку, центральной части живота под грудиной.
В таком случае медикаментозное лечение, скорее всего, будет безрезультатным. Необходимо выявить место компрессии нерва и устранить его.
Возможно, Вам нужно пройти обследование (в Киеве), КТ или МРТ.
Блуждающий нерв и сон
Актуальность. Вегетативные расстройства (их происхождение, клинические проявления и лечение) являются одной из актуальных проблем современной медицины. Функцией вегетативной нервной системы является удержание функциональных параметров деятельности различных систем в границах гомеостаза, т. е. поддержание постоянства внутренней среды; вегетативное обеспечение психической и физической деятельности, адаптация к меняющимся внешним средовым условиям. Практически не существует таких заболеваний, в развитии и течении которых, не играла бы важную роль вегетативная система. Знание основных вегетативных синдромов помогает диагностике и повышению качества лечения болезней, с расстройствами вегетативной нервной системы. Таким образом, немаловажное место в медицине принадлежит современным методам лечения вегетативной нервной системы, т.к. пусковым фактором возникновения болезней являются те или иные нарушения в этой системе (1, 2).
Цель: раскрыть основные принципы современных методов лечения вегетативной нервной системы.
Вегетативная нервная система, которая также называется автономной (systema nervosum autonomicum), контролирует следующие функции организма, такие как питание, дыхание, циркуляция жидкостей, выделение, размножение. Она иннервирует преимущественно внутренние органы и состоит из двух основных отделов: симпатического и парасимпатического. Совместная работа обоих отделов регулируется и контролируется корой головного мозга, которая является высшим отделом центральной нервной системы. Центры вегетативной нервной системы располагаются в головном и спинном мозге (3).
Таким образом, нарушение в какой либо структуре вегетативной нервной системы приводит к нарушению функций, что приводит к возникновению болезни в той или иной системе. Зная, где располагается патологический очаг, мы можем назначить адекватное лечение, используя современные методы, для достижения наибольшего эффекта.
Нарушения в вегетативной нервной системе – это очень частая проблема, с которой приходится сталкиваться современному человеку. Это сочетание эмоционально-психических расстройств с нарушениями со стороны сердечно-сосудистой, дыхательной, пищеварительной, мочеполовой систем. Лечение ВНС – процесс сложный, требующий индивидуального подхода и постоянной коррекции. Современные способы лечения включают в себя модификацию образа жизни, изменение подхода к профессиональной деятельности, коррекцию психо-эмоциональных расстройств, применение медикаментозных средств, в соответствии с развившимися синдромами. Для реализации всего лечебного комплекса может потребоваться невропатолог, терапевт, психолог (психиатр) (4, 6, 7).
Основные принципы современных методов лечения ВНС рассмотрим на примере ВСД. Прежде всего, перед началом лечения необходимо исключить другие заболевания различных органов и систем, которые могут давать симптомы, идентичные таковым при ВСД. Только после достоверно установленного диагноза можно приступать к лечению.Современный взгляд на устранение синдрома ВСД состоит в одновременном применении комплекса медикаментозных и немедикаментозных воздействий, причем последним принадлежит ведущая роль. К методам лечения ВСД относят:
– коррекцию психо-эмоциональной сферы;
– ведение здорового образа жизни;
– модификацию трудовой деятельности;
Коррекция психо-эмоциональной сферы
«Все болезни – от нервов,» — это высказывание как нельзя более точно подходит к ВСД. В большинстве случаев «виноват» какой-то психологический фактор, его ликвидация способствует выздоровлению. При выяснении анамнеза заболевания почти всегда пациенты самостоятельно указывают, с чего «все началось».По возможности необходимо создать позитивную обстановку вокруг больного. Этому способствуют рациональный отдых, поездки на природу (в лес за грибами, на рыбалку, просто прогулки по парку и т.д.). Наличие хобби будет только содействовать нормализации психо-эмоционального состояния. Желательны занятия спортом (2, 7).
Здоровый образ жизни
В первую очередь нужно оптимизировать режим дня. Качественный и полноценный сон (отход ко сну в одно и то же время, длительность сна 7-8 часов и т. д.), прием пищи в одно и то же время, пребывание на свежем воздухе – это все маленькие, но значимые факторы для успешного процесса лечения. Отказ от вредных привычек. Умеренная физическая нагрузка оказывает положительное «тренирующее» воздействие на сердечно-сосудистую систему, способствует нормализации сосудистого тонуса, улучшает кровоток в органах и тканях (4, 6, 7).
Физиотерапевтические методы (6)
Среди немедикаментозных воздействий эта группа мер одна из наиболее эффективных. Физиотерапевтические процедуры успешно применяются не только при лечении больных с ВСД в условиях поликлиники или стационара, но и при проведении санаторно-курортного лечения. Наиболее часто используют электрофорез с разными фармакологическими средствами (кальцием, кофеином, мезатоном, эуфиллином, папаверином, магнием, бромом, новокаином), электросон, водные процедуры (душ Шарко или циркулярный, подводный душ-массаж, контрастные ванны), хлоридно-натриевые ванны, общие радоновые, сероводородные, йодобромные ванны, транскраниальную электроаналгезию, синусоидальные модулированные токи, гальванизацию, магнитотерапию, аэроионотерапию, инфракрасную лазеротерапию, УВЧ, тепловые процедуры (аппликации парафина и озокерита), грязелечение. Показаны иглорефлексотерапия и массаж. Курсовое применение физиотерапевтических методов позволяет устранить многие симптомы ВСД, иногда даже без дополнительного приема лекарственных средств внутрь.
Лекарственная терапия (7)
Фармакологический спектр применяемых препаратов огромен в связи с многообразием симптомов заболевания. Одновременное назначение большого количества препаратов может нанести вред больному, поэтому для каждого больного создается программа приема лекарств в определенной последовательности, которая корригируется в процессе лечения. Препараты, применяемые для лечения, можно разделить на следующие группы:
– успокоительные – предпочтительнее растительные средства (валериана, пустырник) и их комбинации (дормиплант, ново-пассит, нотта, фитосед, персен, седафитон, нервофлукс и др.). Возможны комбинации растительных препаратов с барбитуратами (особенно при сопутствующих нарушениях сна): барбовал, валокордин, корвалол, корвалтаб и др.;
– транквилизаторы – применяют при более выраженных расстройствах эмоциональной сферы, сопровождающихся чувством тревоги и напряжения. Среди них популярными являются гидазепам, грандаксин (тофизопам), буспирон, мебикар (адаптол), афобазол. При еще более выраженных проявлениях показаны диазепам (сибазон), феназепам;
– нейролептики – используются для снижения чувства нервозности, агрессивности, раздражительности и вспыльчивости, тревоги и страха, нормализации сосудистого тонуса и артериального давления. Применяют ридазин (сонапакс, тиорил), эглонил (сульпирид), рисперидон (нейриспин, рисполепт). И транквилизаторы, и нейролептики должны назначаться только врачом и применяться строго по показаниям в течение определенного промежутка времени;
– снотворные – нормализующее влияние на сон оказывают и растительные успокоительные средства, и транквилизаторы, и некоторые нейролептики. Среди непосредственно снотворных препаратов можно отметить золпидем (ивадал), зопиклон (соннат, сомнол), залеплон (анданте), дормикум, радедорм, донормил, мелатонин. Эту группу лекарственных средств назначают на небольшой промежуток времени (обычно 7-14 дней) при крайней необходимости;
– антидепрессанты – применяют у больных со сниженной мотивацией, астенией и депрессией. Они улучшают настроение, уменьшают тоску, косвенным образом нормализуют сон. Это такие препараты как сиднофен, коаксил, флуоксетин (прозак), сертралин (золофт, стимулотон), пароксетин (паксил), амитриптилин, людиомил, симбалта;
ноотропы – препараты, «питающие» мозг. Помогают справиться с общей слабостью, нарушением внимания и памяти, головными болями и головокружением, шумом в ушах. К этой группе относят пирацетам (ноотропил), ноофен (фенибут), глицин (глицисед), пантогам, пантокальцин. С этой же целью возможно применение нейрометаболитов: актовегина (солкосерила), церебролизина;
– препараты, улучающие кровообращение, – кавинтон (винпоцетин), оксибрал, стугерон, пентоксифиллин (трентал);
– препараты, снижающие артериальное давление (гипотензивные), – бисопролол (конкор), атенолол, метопролол, анаприлин. Из растительных средств с этой целью применяют препараты валерианы, зверобоя, боярышника, настойку пиона, душицу, мелиссу, калину и др.;
– препараты, повышающие артериальное давление, – кофеин, мезатон, большинство растительных адаптогенов (настойка лимонника, родиолы розовой, женьшеня);
– препараты, влияющие на метаболизм в сердце, применяются для уменьшения болей и неприятных ощущений в области сердца: милдронат, рибоксин, настойка боярышника. При нарушениях ритма (увеличении частоты сердечных сокращений) показаны аспаркам, панангин, конкор, барбовал, корвалдин;
– при повышении внутричерепного давления – диакарб, лазикс (фуросемид), препараты петрушки, можжевельника, крапивы, мочегонные травы;
– вегетотропные препараты – белласпон, беллатаминал. Они обладают комбинированным действием, влияют и на психо-эмоциональное состояние, и на болевой синдром, и на потливость, снимают симптомы как со стороны симпатической, так и со стороны парасимпатической нервной системы. Также в качестве вегетотропного препарата может быть использован платифиллин;
– антиоксиданты – мексидол, кратал, витрум-антиоксидант, янтарная кислота;
– витамины — показаны как поливитаминные комплексы с общеукрепляющей целью, так и изолированный прием витаминов Е, А, С, группы В (нейровитан, мильгамма, неуробекс, нейрорубин);
– адаптогены – это группа лекарственных средств, повышающих стрессоустойчивость организма. Они обладают антиастеническим действием, способны повышать артериальное давление и тонус сосудов, повышают неспецифический иммунитет: женьшень, родиола розовая, лимонник, элеутерококк, заманиха, аралия, левзея сафлоровидная. Общетонизирующим действием обладают препараты, содержащие спирулину, фенхель, тимьян, ламинарию.
Вывод. Нарушения ВНС не только являются важной частью патогенеза многих заболеваний, а сами могут играть роль « пуcкового механизма » в развитии сложных болезней. В этой связи возникает необходимость использование дополнительный методов лечения на более ранних этапах нарушений ВНС с целью профилактики возможных осложнений, приводящих к снижению качества жизни населения
Блуждающий нерв
Общие сведения, где находится блуждающий нерв
От головного мозга из черепной коробки отходит 12 пар черепных нервов. Блуждающий нерв является десятой парой, и получил своё название из-за брожения по организму и широкого распространения. Анатомия нервной системы предполагает, что у вагусного нерва сложное строение, два ствола и он самый длинный. Картинки наглядно демонстрируют, что по всей длине вагуса расположены его ядра.
Патогенез
Схема прохождения правого блуждающего нерва
Чаще всего патология возникает при полиомиелите, острой форме демиелинизирующей полинейропатии Гийена-Барре и дифтерии.
Классификация
Части тела, которые охватывает Nervus vagus:
Блуждающий нерв состоит из волокон 3-х типов:
Причины
Полноценное функционирование блуждающего нерва крайне важно, т.к. при его патологии:
К неправильной работе иннервируемых вагусом органов приводит:
Патологические изменения могут наблюдаться как в полости черепа, так и на периферической части блуждающего нерва. Внутричерепные причины:
Внечерепные, периферические причины:
Симптомы блуждающего нерва
Клиническая картина во многом зависит от причины возникновения проблемы, локализации и степени повреждения. При внечерепных поражениях охватываются все 3 типа волокон вагуса и последствия могут быть крайне тяжёлыми:
Симптомы, свидетельствующие о поражении вагуса:
Воспаление блуждающего нерва
Клиническая картина зависит от локализации зоны поражения:
Тонус
В состав вегетативной нервной системы входят симпатические волокна и уравновешивающие их работу парасимпатические нервные волокна. Здоровый тонус определяется их нормальным взаимодействием. Признаки правильной работы вегетативной нервной системы:
В результате поражения блуждающего нерва страдает вегетативная нервная система, симптомы неврастении проявляются при нарушении в работе парасимпатических волокон n.vagus:
Раздражение
При раздражении вегетативных волокон блуждающего нерва наблюдаются серьёзные нарушений в работе внутренних органов. Что делают парасимпатические волокна:
Раздражение парасимпатических волокон ведёт к усилению работы желёз внутренней секреции, стимуляции перистальтики кишечника. Чрезмерная выработка желудочного сока может привести к язвенной болезни пищеварительного тракта, а при усиленной перистальтике развивается диарейный синдром. Как результат раздражения нерва может развиться приступ удушья из-за бронхоспазма.
Блуждающий нерв и аритмия
Патологическая работа сердечно-сосудистой системы может быть связана с поражением блуждающего нерва. Возможные нарушения ритма:
Парасимпатическая нервная система активизируется в ночное время суток, что объясняет регистрацию нарушений ритма именно во время сна, ночью. Пациенты предъявляют жалобы на чувство нехватки воздуха, дискомфорт за грудиной. При поражении блуждающего нерва снижается пульс и уровень кровяного давления. При угнетении парасимпатических волокон наблюдается противоположная картина.
Гастрокардиальный синдром
Понятие включает совокупность изменений в работе сердечно-сосудистой системы, которые носят рефлекторный характер и возникают при возбуждении рецепторов желудка и пищевода, чувствительных к химическим и механическим воздействиям. Приступы развиваются в результате раздражения вагуса при повышении давления в брюшной полости, связанного с переполнением желудка.
Клиническая картина складывается из симптомов, которые напоминают сердечный приступ. Диагностический поиск направлен на исключение заболеваний сердечно-сосудистой системы и выявление заболеваний пищеварительного тракта, которые могут быть причиной синдрома Ремхельда. Терапия заключается в применении седативных средств, спазмолитиков и включает сеансы психотерапии.
Анализы и диагностика
Залогом успешного лечения является своевременное обращение к врачу, выставление правильного диагноза и подбор адекватной терапии. Первичный осмотр проводится неврологом. Основные моменты, на которые стоит обратить внимание при осмотре:
С помощью стаканы воды проводится оценка глотательной функции: при поражении вагуса появляется кашель во время глотания. Дополнительные, но обязательные методы обследования:
Лечение блуждающего нерва
Позитивный результат лечения достигается при определении истинной причины патологии и устранении её. В некоторых случаях положительная динамика наблюдается после плазмофереза – процедуры по очищению крови. Хороший эффект достигается и после электростимуляции нерва – процедура по направлению динамического тока в область болевых ощущений – в блуждающий нерв.
Блуждающий нерв и сон
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБУН «Институт физиологии им. И.П. Павлова» РАН, Санкт-Петербург, Россия
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБУН «Институт физиологии им. И.П. Павлова» РАН, Санкт-Петербург, Россия
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Периферическая нейростимуляция в терапии головных болей
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(10): 79-88
Соколов А. Ю., Любашина О. А., Ваганова Ю. С., Амелин А. В. Периферическая нейростимуляция в терапии головных болей. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(10):79-88.
Sokolov A Yu, Lyubashina O A, Vaganova Yu S, Amelin A V. Peripheral neurostimulation in headache treatment. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2019;119(10):79-88.
https://doi.org/10.17116/jnevro201911910179
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБУН «Институт физиологии им. И.П. Павлова» РАН, Санкт-Петербург, Россия
По приблизительным оценкам не менее трети населения развитых стран в разной степени страдает от тех или иных форм первичных головных болей (ГБ), фармакотерапия которых не всегда эффективна и имеет ряд ограничений. Немедикаментозное лечение ГБ может быть альтернативой назначению фармакологических средств и единственно возможным вариантом оказания помощи пациенту при развитии у него лекарственно-резистентной цефалгии. В обзоре рассмотрены различные методы электрической нейромодуляции, использующиеся в терапии первичных ГБ. Приведена информация об этапах внедрения в клиническую практику имплантируемых и неинвазивных устройств, позволяющих осуществлять электростимуляцию периферических нервов и крылонебного узла, а также выполнять транскраниальное магнитное воздействие. Описаны способы применения доступных на мировом рынке портативных электротехнических устройств и обсуждены механизмы антицефалгического действия нейромодулирующей терапии. Особое внимание уделено методам электростимуляции блуждающего и затылочных нервов.
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБУН «Институт физиологии им. И.П. Павлова» РАН, Санкт-Петербург, Россия
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБУН «Институт физиологии им. И.П. Павлова» РАН, Санкт-Петербург, Россия
Институт фармакологии им. А.В. Вальдмана ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия; ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Лечение первичных головных болей (ГБ), к числу которых, согласно международной классификации ГБ [1], относятся мигрень, ГБ напряжения (ГБН) и группа тригеминальных автономных цефалгий, заключается прежде всего в назначении различных лекарственных препаратов, способных либо купировать болевой приступ, либо предотвратить его появление. К сожалению, такая стратегия не всегда эффективна, и ей на помощь приходят немедикаментозные методы терапии цефалгий.
Несмотря на то что официальной классификации методов нелекарственной коррекции ГБ не существует, с определенным упрощением их можно разделить на инвазивные и неинвазивные. К числу последних наряду с рекомендациями по модификации образа жизни пациента относятся когнитивно-поведенческая терапия, методика биологической обратной связи, различные релаксационные техники, а также массаж и мануальная терапия [2—6]. Инвазивная тактика подразумевает использование акупунктуры [7—9] или хирургического подхода, в рамках которого проводят пластику триггерных точек, декомпрессию ветвей периферических нервов, радиочастотную абляцию крылонебного ганглия и т. д. [10—12].
Особую нишу в нефармакологическом лечении ГБ занимают различные способы электрической нейромодуляции, к которым в последние годы стабильно возрастает интерес профильных специалистов [13, 14]. К инвазивным методикам относятся электростимуляции гипоталамуса или вентральной области покрышки (англ.: Deep Brain Stimulation, DBS), крылонебного ганглия, затылочных нервов и верхних сегментов шейного отдела спинного мозга [14—16]. К неинвазивным техникам относятся стимуляции блуждающего и надглазничного/надблокового нервов [16—18], чрескожная электростимуляция области сосцевидного отростка (англ.: Percutaneous Mastoid Electrical Stimulation, PMES) [19], мишенью которой считается фастигиальное ядро мозжечка, термоэлектрическая калорическая стимуляция наружного слухового прохода (англ.: Caloric Vestibular Stimulation, CVS) [20], так называемая безболезненная отдаленная электростимуляция (англ.: Non-painful remote electrical stimulation), при которой электроды накладывают «отдаленно от головы» — на верхнюю часть плеча [21], а также два вида транскраниальной стимуляции — электрическая и магнитная, действие которых направлено на определенные зоны коры [22, 23].
Способы нейромодуляции и технические устройства, разрешенные к применению для лечения ГБ
На сегодняшний день четыре из указанных выше процедур одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и/или Европейским медицинским агентством именно для лечения цефалгий, причем три из них являются неинвазивными.
Неинвазивный нейростимулятор Cefaly
FDA разрешило использование чрескожного стимулятора надглазничного и надблокового нервов Cefaly (производство «Cefaly Technology», Бельгия, [24, 25]) для профилактики мигрени 12.03.14, а для купирования атаки этого заболевания — 15.09.17; сама методика нередко именуется «external trigeminal nerve stimulation» (eTNS) [17]. Приказом Росздравнадзора от 23.09.16 нейростимулятор Cefaly допущен к обращению на территории Российской Федерации с номером регистрационного удостоверения РЗН 2016/4743.
В настоящее время на американском рынке доступно три разновидности устройства: Cefaly PREVENT (для предотвращения мигрени), Cefaly ACUTE (для купирования приступа) и Cefaly DUAL (оба показания) [25], которые почти не различаются по внешнему виду. Нейростимулятор представляет собой небольшое портативное устройство ромбовидной формы, которое фиксируется посередине лба и контактирует с кожей посредством пленочного самоклеющегося многоразового электрода; управление осуществляется с помощью единственной кнопки, расположенной центрально. В линейке продукции Cefaly Technology это вторая так называемая магнитная модель (крепится к гибкому накожному электроду с помощью двух магнитов); оригинальная версия стимулятор — Cefaly1 — имела симметричные дужки для расположения на голове и по внешнему виду напоминала «очки для циклопа». В европейских странах производитель Cefaly предлагает использовать его не только для профилактики различных форм мигрени, но и для лечения ГБН, кроме того, в продаже имеется аксессуар Cefaly Kit Arnold, представляющий собой надеваемый на голову эластичный ремень из токопроводящего материала, позволяющий осуществлять стимуляцию затылочных нервов при окципитальной невралгии [24]. Основанием для получения разрешений к применению Cefaly для превентивной и абортивной терапий мигрени послужили позитивные результаты соответствующих клинических исследований [17, 18]; активное постмаркетинговое изучение антицефалгической эффективности Cefaly продолжается в проектах различного дизайна [26, 27]. На основании данных нейровизуализирующих и нейрофизиологических исследований, проведенных у лиц с мигренью, механизм терапевтического действия eTNS связывают с изменением метаболизма в различных кортикальных областях, в частности в передней поясной извилине, что, впрочем, едва ли объясняет обезболивающий эффект процедуры [17].
Неинвазивный магнитный стимулятор Spring TMS/sTMS mini
В мае 2014 г. автономный транскраниальный магнитный стимулятор Spring TMS (производство «eNeura Inc.», США [28]) получил одобрение надзорного ведомства США для купирования приступа мигрени с аурой, а с июня 2017 г. в США и странах Евросоюза устройство разрешено и для предотвращения приступов мигрени. Поскольку Spring TMS представлял собой довольно громоздкое изделие, вскоре после выхода на рынок он был снят с производства, уступив место более элегантному и удобному в использовании устройству под названием sTMS mini, внешне напоминающему подголовник автомобильного кресла или миниатюрную ортопедическую подушку [28]. Для проведения процедуры пациент должен прижать устройство к затылку и нажать на кнопку подачи электромагнитного импульса. И хотя итоги недавнего систематического обзора свидетельствуют в целом об умеренной эффективности транскраниальной магнитной стимуляции [29], возможности этого метода — прежде всего как средства профилактической терапии мигрени — продолжают активно изучаться [30, 31]. В отличие от eTNS, влияние которой на нейрональную активность оценивалось только на людях, механизм действия транскраниальной магнитной стимуляции изучался на специфических моделях ГБ у животных. Было показано, что у крыс и кошек данная процедура подавляет возникновение и распространение кортикальной депрессии [32], роль которой как возможного триггера атак мигрени, равно как и нейрофизиологического коррелята мигренозной ауры, является предметом оживленных дискуссий [33]. Кроме этого, у крыс транскраниальная магнитная стимуляция подавляла возбудимость нейронов вентрального заднемедиального ядра (ВЗМЯ) таламуса, имеющих крайне важное значение в нейробиологии мигрени [33], причем это угнетение было налоксон-обратимым, что свидетельствует о вовлечении опиоидергической системы в реализацию антимигренозного эффекта изучаемого метода лечения [32].
Неинвазивный нейростимулятор gammaCore/gammaCore Sapphire
Неинвазивный электрический стимулятор блуждающего нерва gammaCore (производство «electroCore, Inc.», США [34]) разрешен в США по трем показаниям. Так, 18.04.17 FDA допустило gammaCore к применению в абортивной терапии атак эпизодической кластерной ГБ, являющейся самой распространенной формой тригеминальной автономной цефалгии [35], 29.01.18 указанная организация одобрила использование устройства для купирования приступов мигрени, а 28.11.18 — для профилактики кластерной ГБ у взрослых пациентов в качестве средства дополнительного лечения. В 2018 г. на смену базовой модели gammaCore пришло изделие gammaCore Sapphire, имеющее более строгий дизайн и внешне напоминающее электрошокер размером с ладонь. Для выполнения процедуры необходимо прижать устройство двумя металлическими контактами к переднебоковой поверхности шеи в проекции ствола блуждающего нерва и включить необходимый режим стимуляции [34]. Кроме США, gammaCore Sapphire свободно продается в Европе, Латинской Америке, Канаде, Индии и Новой Зеландии.
Имплантируемый нейростимулятор Pulsante SPG
Имплантируемый электростимулятор крылонебного ганглия Pulsante SPG (производство «Autonomic Technologies, Inc.», США [36]) c февраля 2012 г. одобрен в Европе для контроля кластерной ГБ [14, 37, 38]. Pulsante SPG представляет собой автономную систему, состоящую из миниатюрного имплантируемого стимулятора и внешнего программируемого контроллера. Для установки стимулятора, состоящего из генератора электрических импульсов, крепежного элемента и короткого электрода, выполняется несложное хирургическое вмешательство, в ходе которого через внутриротовой доступ устойства вводится в крылонебную ямку и фиксируется винтами к верхнечелюстной кости. Управление стимуляцией осуществляется посредством контроллера, напоминающего плоскую телефонную трубку; пациент прикладывает устройство к щеке в проекции установленного стимулятора и включает требуемый режим для его активации [37, 38]. Частое использование Pulsante SPG «по требованию», т. е. для купирования приступов кластерной ГБ, что является официально зарегистрированным показанием, сопровождается, как правило, уменьшением интенсивности и частоты атак; также обсуждается возможность применения изделия и для лечения мигрени. Механизм антицефалгического действия электростимуляции крылонебного ганглия связывают с вмешательством в тригемино-автономный рефлекс, активация которого рассматривается как компонент патогенеза тригеминальных автономных цефалгий, хотя эта гипотеза экспериментально не подтверждена [37, 38]. Интересно, что для достижения лечебного эффекта критически важны параметры стимуляции, например частота тока; было показано, что низкочастотная стимуляция может оказать противоположное действие, т. е. спровоцировать приступ ГБ [39].
Учитывая бурное развитие технологий и большое количество текущих клинических исследований, в ближайшие годы можно ожидать появления на рынке новых девайсов, например имплантируемых (StimRelieve Halo Migraine System, производство «StimRelieve, LLC», США) и неинвазивных (OSTNS Neurostimulator и Relivion, производство «Neurolief Ltd», Израиль) мультитаргетных стимуляторов перикраниальных периферических нервов, а также разрешения к применению и расширения показаний к назначению уже известных устройств [13, 14, 16].
Далее более подробно будут рассмотрены этапы внедрения в клиническую практику и нейрофизиологические механизмы действия при цефалгиях двух, пожалуй, наиболее известных и универсальных процедур из числа неинвазивных и инвазивных методик — электрической стимуляции блуждающего и затылочных нервов.
Электрическая стимуляция блуждающего нерва
На протяжении почти 20 лет электрическая стимуляция блуждающего нерва — она же вагусная нейростимуляция (ВНС) — является признанным методом лечения рефрактерных к фармакотерапии эпилепсии [40] и депрессии [41]. Вместе с тем в последние годы ВНС рассматривается клиницистами и как эффективный способ немедикаментозного лечения фармакорезистентных первичных ГБ [13, 14].
В нескольких пилотных исследованиях начала 2000-х годов было показано, что не менее чем у половины пациентов стимуляция вагуса сопровождается уменьшением частоты и интенсивности приступов ГБ при хронической мигрени, кластерной ГБ или хронической ежедневной ГБ, являющихся у исследуемых лиц не только сопутствующими депрессии или эпилепсии состояниями [42, 43], но и основными заболеваниями [44]. Кроме этого, включение ВНС в схему лечения позволяло уменьшить дозу и количество потребляемых фармакологических препаратов профилактического ряда [42, 44]. Было замечено что, помимо самостоятельной эффективности, ВНС способна потенцировать превентивное антицефалгическое действие гипоталамической стимуляции, используемой для лечения фармакоустойчивой хронической кластерной ГБ [45]. Описывались случаи, когда электрическая и даже механическая — пальцевое надавливание на переднюю поверхность шеи — стимуляции блуждающего нерва сопровождались прерыванием приступа ГБ [46, 47].
Широкое внедрение методики ВНС существенно сдерживалось тем, что первые вагусные стимуляторы были довольно сложными имплантируемыми устройствами (например, изделия от компании «Cyberonics, Inc.», США), для установки которых, равно как и для последующей замены источника питания, требовалось хирургическое вмешательство. Эта непростая процедура была сопряжена с очевидными операционными рисками и могла приводить к развитию таких побочных эффектов, как парез голосовых связок, брадикардия и асистолия, парестезии и болевые ощущения, кашель, одышка, фарингит и инфекционные осложнения [48].
С появлением в начале 2010-х годов более безопасных неинвазивных устройств, позволяющих чрескожно стимулировать либо шейный отдел (gammaCore [23]), либо ушную ветвь блуждающего нерва (NEMOS, производство «Cerbomed», Германия [49]) возобновился интерес к ВНС, что способствовало проведению дальнейших изысканий.
Сначала в открытых клинических исследованиях были продемонстрированы эффективность и хорошая переносимость неинвазивной ВНС (нВНС) при купировании приступов эпизодической мигрени [50], а также мигрени с частыми приступами и хронической мигрени; использование устройства также помогло сократить чрезмерное потребление анальгетиков [51]. В проспективном обсервационном когортном исследовании нВНС зарекомендовала себя как безопасная процедура, сопровождающаяся снижением частоты, интенсивности и продолжительности мигренозных атак, что ассоциировалось еще и с облегчением симптоматики связанных с ними слабости, депрессии и нарушений сна [52]. В открытом исследовании нВНС оказалась эффективной в профилактике менструальной мигрени [53].
Результаты первого проспективного, рандомизированного многоцентрового двойного слепого контролируемого исследования нВНС как средства профилактики хронической мигрени были опубликованы в 2016 г. В пилотном проекте EVENT удалось выявить, что постоянное применение нВНС уменьшает количество дней с ГБ при хронической мигрени по сравнению с исходными показателями, хотя значимых различий с контрольной группой обнаружено не было. Авторы отмечают хорошую переносимость и безопасность метода и предсказуемо указывают на необходимость проведения более масштабного исследования с аналогичным дизайном [54].
В том же году были представлены итоги еще двух рандомизированных контролируемых исследований нВНС, но уже при лечении кластерной ГБ. В первом проекте PREVA была доказана эффективность процедуры в превентивной терапии хронической кластерной цефалгии [55]. Во второй работе — ACT1 — использование нВНС позволяло купировать приступы эпизодической кластерной ГБ у значимо большего по сравнению с контролем числа пациентов [56]. Именно результаты исследований PREVA и АСТ1 вместе с данными схожего по дизайну проекта АСТ2 [57] послужили основанием для разрешения надзорными ведомствами США и Европы использования стимулятора gammaCore в профилактике и абортивном лечении кластерной ГБ соответственно.
Как уже упоминалось, в январе 2018 г. FDA одобрило применение gammaCore для купирования приступов эпизодической мигрени как с аурой, так и без; решение было принято на основании результатов двойного слепого, рандомизированного контролируемого исследования PRESTO [58].
Уместно будет добавить, что нВНС может с успехом применяться у пациентов с мигренью разных возрастных категорий [59], лиц с индометацин-чувствительными тригеминальными вегетативными цефалгиями [60] и добавление процедуры к стандартным схемам лечения хронической кластерной ГБ является экономически целесообразным [61].
Несмотря на то что во всех указанных работах использован стимулятор шейного отдела блуждающего нерва gammaCore, есть данные моноцентрового, рандомизированного, двойного слепого, контролируемого исследования о том, что перкутанная электростимуляция ушной ветви блуждающего нерва с помощью прибора NEMOS (ныне выпускается под брендом VITOS, производство «tVNS Technologies GmbH», Германия [49]) также является эффективным и безопасным воздействием при профилактическом лечении хронической мигрени [62].
Антиноцицептивный эффект ВНС был неоднократно показан как в скрининговых поведенческих тестах на животных [63], так и в условиях экспериментально индуцированной боли у людей [64]. Предполагается, что обезболивающее действие ВНС реализуется посредством различных механизмов при участии множества нейроанатомических структур ЦНС (центральное серое вещество среднего мозга, ядра шва, голубое пятно и т. д.), ответственных за ноцицептивный процессинг [64], в том числе и в системе тройничного нерва, играющего ключевую роль в патогенезе цефалгий [33, 35]. В частности, в нейрофизиологических и иммуногистохимических исследованиях ВНС приводила к преимущественному угнетению Fos-реактивности и/или спайковых ответов нейронов спинального ядра тройничного нерва (СЯТН) [63, 65] и ВЗМЯ таламуса [66] при болевой стимуляции их рецептивных полей, что может свидетельствовать о торможении ноцицептивной трансмиссии в тригеминоталамическом пути на сегментарном и супраспинальном уровнях.
Однако нейробиологические механизмы собственно антицефалгического действия ВНС долгое время оставались неясными. Предпринимаемые попытки объяснения клинической эффективности ВНС при первичных ГБ носили преимущественно умозрительный характер и основывались на приведенных выше фактах неспецифического антиноцицептивного действия ВНС и рассуждениях о возможном вовлечении различных больмодулирующих структур мозга, имеющих связи с ядром одиночного тракта и СЯТН, с последующим изменением тонкого баланса их взаимоотношений [44, 64]. Совершенно очевидно, что малая доказательная база подобных представлений и умозаключений являлась прямым следствием дефицита экспериментальных работ по изучению эффектов ВНС на моделях головной боли у животных.
Результаты первого исследования такого рода, выполненного авторами настоящего обзора, были опубликованы в 2012 г. [67]. Мы провели серию острых опытов на электрофизиологической модели тригеминодуроваскулярной ноцицепции у крыс, суть которой заключается во внеклеточной микроэлектродной регистрации спайковой активности нейронов тригеминоталамокортикального пути; такая методика единодушно признается мировым научным сообществом как наиболее информативный способ исследования релятивных мигрени процессов в экспериментах на животных [68]. Было показано, что непрерывная электростимуляция центрального отрезка блуждающего нерва оказывает преимущественно подавляющее влияние на фоновую активность и вызванные электрическим раздражением твердой мозговой оболочки ответы конвергентных нейронов СЯТН. Наблюдаемый эффект зависел от режима, продолжительности и частоты вагальной стимуляции: прекондиционирующая ВНС с частотой 30 Гц в течение 200 мс однозначно уступала постоянной стимуляции с той же силой тока, но частотой 10 Гц. Таким образом, впервые на нейрофизиологической модели ГБ удалось продемонстрировать главным образом антиноцицептивное действие ВНС, реализуемое через угнетение возбудимости тройничных сенсорных нейронов второго порядка [67].
Активное внедрение в практику лечения ГБ неинвазивного стимулятора шейного отдела блуждающего нерва gammaCore способствовало поддержанию интереса к изучению механизмов антицефалгического действия ВНС, и после 2012 г. были опубликованы результаты нескольких исследований, которые могут считаться профильными с этой точки зрения. Так, у предварительно сенситизированных дуральной аппликацией провоспалительных медиаторов крыс нВНС снижала выраженность периорбитальной аллодинии и уменьшала внеклеточное содержание глутамата в каудальной порции СЯТН, повышенное после внутрибрюшинного введения нитроглицерина [69]. Также в опытах на крысах было показано, что ВНС с использованием как имплантируемых, так и чрескожных электродов с равной эффективностью ингибирует распространение кортикальной депрессии [70]. Кроме этого, нВНС подавляла поведенческую реакцию на механическую стимуляцию кожи морды и снижала экспрессию ассоциированных с нейрональной возбудимостью протеинов в клетках тройничного ганглия и СЯТН у крыс, предварительно сенситизированных инъекцией в трапециевидную мышцу полного адъюванта Фрейнда, после обонятельной провокации запахом ароматического масла [71]. У здоровых нВНС сопровождалась существенным уменьшением слезоотделения, вызванным раздражением слизистой носа, что свидетельствует о торможении тригеминовегетативного рефлекса, играющего заметную роль в патогенезе ГБ, особенно тригеминальных автономных цефалгий [35]; авторы рассуждают о возможном вовлечении ядра одиночного тракта и гипоталамуса в реализацию подавляющего эффекта ВНС [72]. Все эти данные могут объяснять нейрофизиологические механизмы реализации терапевтического потенциала ВНС в клинической практике при лечении ГБ.
Примечательно, что спустя 5 лет после публикации первых итогов работы по изучению эффектов ВНС на электрофизиологической модели мигрени [67] аналогичные результаты были воспроизведены зарубежными учеными [73], что актуализирует ранее изложенную информацию и подтверждает правильность сделанных наблюдений и выводов.
Электрическая стимуляция затылочных нервов
Учитывая накопленные к настоящему времени данные, справедливо утверждать, что на роль фаворита среди инвазивных методик антицефалгической электронейростимуляции с точки зрения соотношения универсальности, эффективности и безопасности вполне может претендовать электрическая стимуляция затылочных нервов (ЭСЗН) [14, 74, 75]. Действительно, результаты клинических наблюдений и исследований разного дизайна свидетельствуют об успешном применении ЭСЗН для лечения таких хронических заболеваний, как гемикрания континуа [76], тригеминальные автономные цефалгии SUNCT и SUNA [77], пароксизмальная гемикрания [78], кластерная ГБ [79] и мигрень [80, 81]. Также описаны случаи эффективности ЭСЗН в терапии гипнической ГБ [82], ГБ у пациентов с мальформацией Киари [83], лекарственно-индуцированной ГБ [84], хронической ГБН [85] и цервикогенной цефалгии [86]. При общей оценке упомянутых работ, как правило, более чем у половины подвергнутых процедуре ЭСЗН пациентов отмечены значимое уменьшение частоты и/или интенсивности приступов ГБ, улучшение качества жизни и сокращение потребления препаратов абортивного и/или превентивного рядов.
Несмотря на то что опубликованный в 2015 г. метаанализ контролируемых исследований ЭСЗН при хронической мигрени не выявил убедительных доказательств эффективности метода [87], интерес к его использованию не ослабевал, что неудивительно, поскольку объем существующих данных оправдывал дальнейшее изучение ЭСЗН при условии тщательной селекции пациентов, учета всех возможных исходов, подбора оптимальных параметров стимуляции, наличия адекватной статистической мощности и улучшения хирургической подготовки [88].
Действительно, после 2015 г. качество исследований возросло [80, 81], а более обширный метаанализ 2018 г. выявил в целом успешность применения ЭСЗН при лекарственно-резистентных ГБ как минимум по двум контрольным точкам, хотя и с низким уровнем доказательности из-за риска системных ошибок. Авторы обзора указывают на малое количество рандомизированных контролируемых исследований, недостаточный размер выборок, гетерогенность оцениваемых исходов и делают вывод о необходимости дальнейшего проведения работ в этой области [75].
Электростимулятор затылочных нервов (например, производства компании «Medtronic», Ирландия [89]) представляет собой высокотехнологичную систему, состоящую из имплантируемого устройства в виде небольшого плоского блока, совмещающего в себе программируемый генератор импульсов и источник питания, с длинными, тонкими и гибкими проволочными электродами, а также внешнего пульта дистанционного радиоуправления. Во время хирургической операции через разрез на задней поверхности шеи электроды вводят под кожу моно- или билатерально и располагают почти перпендикулярно восходящим ветвям большого и малого затылочных нервов. Современные модели электродов нередко снабжены специальными концевыми «якорями» (типа AnkerStim у «Medtronic»), «цепляющимися» за фасцию и препятствующими их смещению. После вживления, как правило, электроды временно соединяют с наружным источником тока и в течение нескольких дней проводят предварительную оценку эффективности метода; решение об установке инкорпорируемого блока принимается на основании положительных результатов такого тестирования, т. е. уменьшения интенсивности ГБ у конкретного пациента. Внутренний импульсный генератор может имплантироваться в различные участки тела, например в подключичную, подмышечную, поясничную и подвздошную области. При выборе места расположения устройства исходят не только из косметических соображений, но учитывают и возможность натяжения электродов при движениях человека (что нежелательно, поскольку может вести к их миграции), а также принимают во внимание особенности телосложения и предпочтения самого пациента [90].
Перспективным представляется использование способа комбинированной стимуляции затылочного и надглазничного нервов с помощью имплантируемых электродов [91]. Кроме того, в апреле 2017 г. были опубликованы весьма оптимистичные результаты первого рандомизированного контролируемого исследования эффективности и безопасности чрескожной — с неимплантируемыми электродами — ЭСЗН в профилактике мигрени [92]. На основании полученных данных можно прогнозировать дальнейшее развитие и распространение метода ЭСЗН уже без хирургической подготовки, что позволит избежать характерных для инвазивного способа осложнений (миграция электродов, инфицирование раны, а также локальная боль, связанная с нахождением имплантатов в тканях) [90].
Несмотря на успех ЭСЗН в лечении цефалгий, механизм ее терапевтического действия долгое время оставался неясным. Попытки его объяснения сводились к преимущественно общим и обтекаемым рассуждениям на тему индуцированного ЭСЗН-подавления активности А-дельта- и С-афферентов тройничного нерва, равно как и вовлечения сегментарных и супраспинальных нейроанатомических образований, участвующих в ноцицептивном процессинге при ГБ [74, 77, 84]. В большинстве своем эти умозаключения были основаны на данных единичных нейровизуализирующих исследований [93], а также на адаптации теории «воротного контроля» боли [94] к особенностям тригеминоцервикальной конвергенции [95, 96].
Первые экспериментальные исследования эффектов ЭСЗН на моделях ГБ у животных появились в конце 90-х — начале 2000-х годов. Было показано, что электростимуляция большого затылочного нерва повышает метаболическую активность в каудальной порции СЯТН и задних рогах шейных сегментов спинного мозга у кошек [97], а также усиливает чувствительность нейронов тригемино-цервикального комплекса для менингеальных входов у крыс [95]. Однако эти работы скорее позволяли трактовать патогенез цервикогенной ГБ и подтверждали существование единого морфофункционального континуума между тройничным каудальным ядром и задними рогами верхних шейных сегментов спинного мозга [96], чем объясняли эффективность ЭСЗН при цефалгиях. Кроме этого, использованные в указанных экспериментах параметры стимуляции нерва, как и сам протокол ее назначения, не соответствовали таковым для применения в реальной клинической практике [74, 77].
Во второй декаде ХХI века были проведены исследования, результаты которых в большей мере способствуют пониманию причин эффективности ЭСЗН при Г.Б. Так, на модели хронической мигрени у крыс, предварительно сенситизированных с помощью эпидуральной инфузии провоспалительных медиаторов [98], равно как и у животных со спонтанной тройничной аллодинией [99], ЭСЗН повышала пороги чувствительности к механическому раздражению кожи головы и конечностей в поведенческих тестах. Эти данные демонстрируют антиаллодинический эффект ЭСЗН, что может свидетельствовать об угнетении процессов центральной сенситизации, но не отвечают на вопрос, почему это происходит.
Вероятный нейрофизиологический механизм действия ЭСЗН при цефалгиях был впервые выявлен в серии опытов с различными электростимуляционными сетами (напряжение 1—6 В с частотой 50—100 Гц) на вышеописанной модели тригеминоваскулярной ноцицепции у крыс. Тот же авторский коллектив, которому принадлежит первенство демонстрации в эксперименте эффектов ВНС, показал, что высокочастотная надпороговая стимуляция большого затылочного нерва при сопоставимых с используемыми в клинике параметрах сопровождается подавлением фоновой активности конвергентных нейронов СЯТН и их ответов на электрораздражение твердой мозговой оболочки [100]. Этот угнетающий эффект имел прямо пропорциональную зависимость от значений амплитуды ЭСЗН и был максимальным при напряжении 6 В, что в целом коррелирует с клиническими данными о большей эффективности надпороговой стимуляции [101]. По сравнению с эффектами ВНС изменение частоты спонтанных и вызванных спайков под действием ЭСЗН носило схожий, хотя и более выраженный и однонаправленный характер, что позволяет говорить о возможной сопоставимости ЭСЗН и ВНС как методов лечения ГБ в плане наличия общего механизма действия.
Очевидно, что возможность влияния ЭСЗН на активность тригеминоваскулярных нейронов СЯТН предопределяется конвергенцией афферентов тройничного и большого затылочного нервов на указанных клетках [95, 96]. Известно, что тригеминоцервикальные конвергентные механизмы могут быть как ингибиторными, так и возбуждающими и приводить соответственно либо к угнетению, либо к индукции или потенцированию боли [102]. В описанной выше экспериментальной работе, вероятно, благодаря оптимально подобранным параметрам тока и протоколу назначения ЭСЗН был выявлен только тормозной тип тригеминоцервикального взаимодействия, развитие которого можно объяснить с позиции «теории воротного контроля» [94]. Согласно этой гипотезе, электростимуляция толстых А-бета-волокон затылочного нерва может сопровождаться подавлением ноцицептивного входа по тонким А-дельта-тройничным афферентам, что будет приводить к угнетению ответов клеток СЯТН. Таким образом, допустимо с определенной уверенностью говорить о том, что антицефалгическое действие ЭСЗН может быть связано с подавлением ноцицептивного процессинга на уровне тригеминоцервикального комплекса.
В вышедшей в апреле 2017 г. в журнале «Neurosurgery» статье приводятся данные исследования зарубежных коллег, которое можно считать логическим продолжением изучения влияния ЭСЗН на активность клеток тригеминоталамического пути [103]. Авторы показали, что у предварительно сенситизированных крыс (хроническая инфузия провоспалительных медиаторов через эпидуральный катетер) ЭСЗН угнетала ответы нейронов ВЗМЯ таламуса на механическую стимуляцию кожи морды и передних конечностей, т. е. выявили уже на супрасегментарном уровне эффект ЭСЗН, аналогичный полученному нами при изучении реакции клеток СЯТН.
Заключение
В области немедикаментозного лечения ГБ складывается несколько парадоксальная ситуация: бурное внедрение нейромодулирующих методов в клиническую практику заметно опережает понимание механизмов их антицефалгического действия. Из-за недостаточного количества экспериментальных исследований, посвященных этому вопросу, внятных объяснений терапевтической эффективности электронейростимуляции при ГБ в настоящее время мало, и если таковые появляются [32, 67, 69, 70, 73, 100], это сразу же усиливает позиции конкретного способа нейромодуляции на фронте борьбы с ГБ.
На сегодняшний день электрическая стимуляция периферических нервов с использованием как неинвазивных, так и имплантируемых устройств представляется эффективным, безопасным и экономически оправданным способом терапии различных форм ГБ, позволяющим существенно улучшить качество жизни пациентов и сократить потребление ими лекарственных препаратов [104, 105]. Необходимо дальнейшее изучение различных стимуляционных методик в экспериментальных и клинических исследованиях и их внедрение в схемы лечения цефалгий.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.