венозно лимфатическая недостаточность что значит
phlebolog.pro
флеболог Дробязго С.В.
г. Москва, Большой Головин переулок, 4. Клиника КСТ
запись на прием: +7 495 607 0557
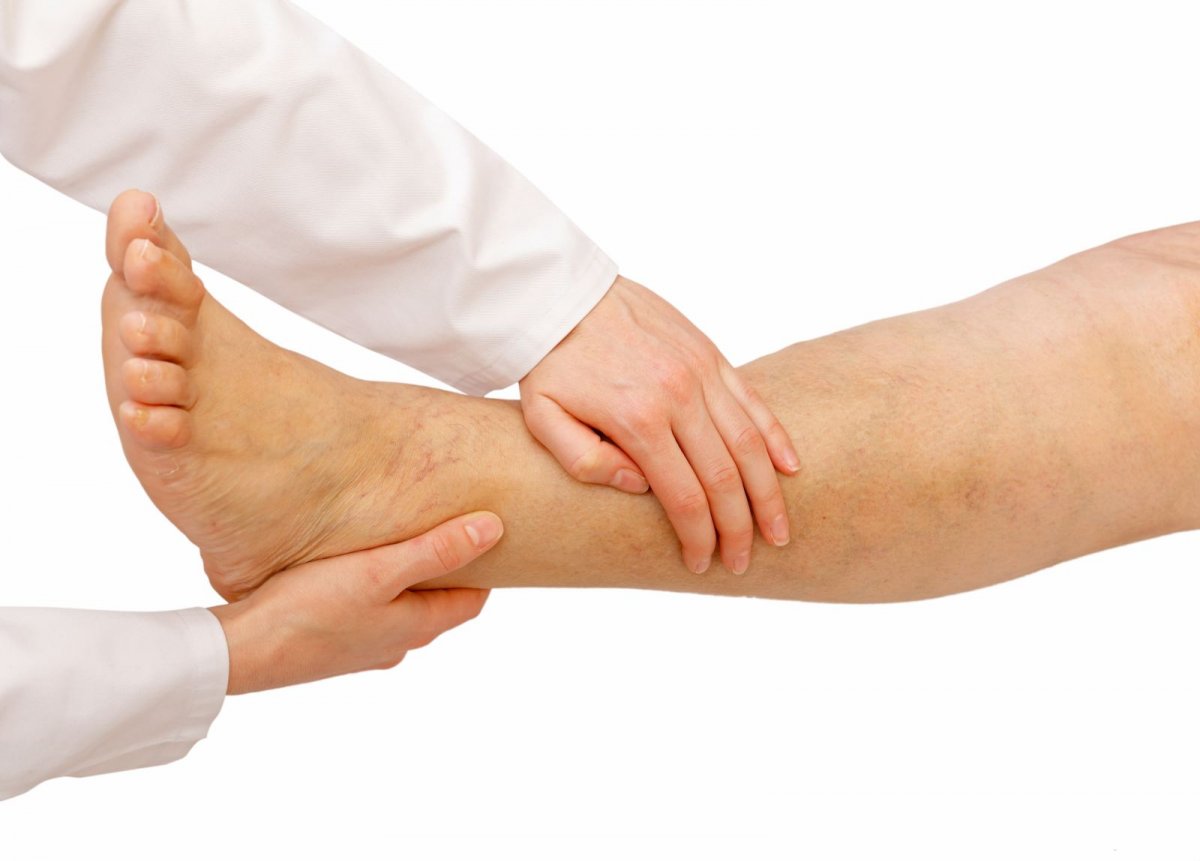
Почему отекают ноги, венозная и лимфатическая недостаточность
H. Partsch, B.B. Lee
Phlebology 2014, Vol. 29(10) 645–647
Венозная и лимфатическая системы тесно взаимодействуют через систему капилляров на тканевом уровне, транспортируя венозную кровь и лимфу из тканей. Сейчас очевидно, что обе системы взаимозависимые, однако этим фактом мягко пренебрегали многие десятилетия.
Тесная взаимосвязь лимфатической и венозной систем формируется еще на этапе эмбрионального развития, и впоследствии приводит тесному анатомическому взаимодействию. В результате, этот тандем поддерживает физиологическую дренажную функцию, несмотря на совершенно разные реодинамические условия.
Уникальная взаимосвязь, о которой идет речь, играет важную роль в патофизиологии любого вида отека. Перечисленные выше теоретические положения имеют и практическое значение, касающееся как дифференциальной диагностики, так и лечения.
Проведенные недавно фундаментальные исследования показали, что отток тканевой жидкости осуществляется в основном за счет лимфатического дренажа, а не за счет реабсорбции в венозных капиллярах, как считалось ранее [2]. Это означает, что лимфатические сосуды играют основную роль при любом виде отека. «Хронический отек», который держится более трех месяцев, и с которым сталкивается любой практикующий флеболог, может быть определен как лимфедема, независимо от его первоначальной причины.
Отек развивается когда компенсаторных возможностей лимфатической системы по транспортировке жидкости недостаточно чтобы справиться с повышенной фильтрацией жидкости в ткани. Экстравазация жидкости может быть связана с пониженным онкотическим давлением, повышенной проницаемостью капиллярной мембраны и, что наиболее важно для флебологов, с увеличением венозного давления [3].
Отек, связанный с пониженным осмотическим давлением плазмы (гипоальбуминемия) может быть вызван различными причинами: недостаточным питанием, болезнями кишечника (синдром мальабсорбции), печеночной недостаточностью или нефротическим синдромом.
В результате травмы или воспаления повышается проницаемость капилляров, жидкость и плазма проходит через эндотелиальный барьер в ткани. Некоторые лекарственные препараты, например, блокаторы кальциевых каналов, также могут увеличивать отек, влияя на проницаемость.
Тем не менее, наиболее частой причиной хронического отека является повышенное давление в капиллярах из-за высокого венозного давления. Это именно та ситуация когда флебологи вступают в игру. Капиллярное давление может повышаться вследствие венозной обструкции и/или венозного рефлюкса, при длительном вынужденном статическом положении, при правожелудочковой сердечной недостаточности.
Живя в эру, когда ожирение приобрело характер эпидемии, клиницисты все чаще сталкиваются с новой проблемой, характеризующейся часто чудовищным двусторонним отеком, липодерматосклерозом с папилломатозным фиброзом кожи. Нередко такое состояние описывают как «вторичная лимфедема на фоне ожирения” или «слоновость”, «еlephantiasis nostras verrucosa”.
Подобное уникальное состояние вызвано венозной обструкцией как выше так и ниже паховой складки, когда в сидячем положении под тяжестью жирового фартука сдавливаются вены [6, 7]. Такая форма лимфедемы может быть устранена методами бариатрической хирургии и восстановлением мобильности пациента [8].
Флеболимфедема, таким образом, представляет собой сочетание хронической венозной недостаточности (ХВН) и лимфатической недостаточности (ХЛН) различного происхождения. Клинические проявления весьма вариабельны и зависят от степени и этиологии ЗВН и ХЛН. Тем не менее, в большинстве случаев, флеболимфедема развивается вторично на фоне ХВН после тромбоза глубоких вен (ТГВ) и ХЛН, развивающейся в результате постоянного местного повреждения тканей (например, при трофической язве).
Raju и соавторами [11] описано 11 пациентов с «венозной лимфедемой” из-за стеноза подвздошой вены, у которых лимфедема была ликвидирована после стентирования этих вен. Однако, при радионуклидной сцинтиграфии у таких пациентов определяется нормальный лимфатический клиренс. В других работах было продемонстрировано органическое поражение лимфатических путей у пациентов с трофическими язвами [12], а отделяемое из язв было идентифицировано как лимфатическая жидкость [13].
Лимфатическая система вовлечена в патологический процесс не только при трофических изменениях кожи, то так же у пациентов с тромбозом глубоких вен (ТГВ) и посттромбофлебитическим синдромом (ПТФС) [13, 14]. Субфасциальный лимфатический дренаж нарушен у большинства пациентов с ТГВ и ПТФС, в то время как префасциальный лимфодренаж усилен, за исключением пациентов у которых были повторные эпизоды воспаления подкожной клетчатки. Вовлечение лимфатической системы в этих ситуациях указывает на ее роль в удалении фибриновых наложений со стенок вен. Фибрин как раз таки и поддерживает хроническое воспаление, приводящее к ремоделированию, характерному для ПТФС [15].
Объективная оценка лимфатической системы затруднена при отсутствии первичного поражения лимфатических сосудов. Стандартная лимфосцинтиграфия после под- или внутри-кожного введения радионуклида, как правило, показывает нормальный клиренс или усиление лифодренажной функции, что влечет за собой неверный вывод об отсутствии лимфатической недостаточности. Патологические сцинтиграфические признаки нарушения лимфодренажа появляются только при глубоком повреждении всей лимфатической транспортной системы.
Тем не менее, признаки лимфатической микроангиопатии, как правило, можно обнаружить на локальном отечном участке кожи используя водорастворимый контраст (непрямая рентгенлимфография) или при помощи метода флюоресцентной микроангиграфии [13].
Локальная экстравазация контраста в начальных лимфатических капиллярах является типичной особенностью, в то время как крупные лимфатические коллекторы остаются интактными и могут даже контрастироваться ускоренно. Этот феномен хорошо продемонстрирован при липодерматосклерозе (CEAP C4b) и был назван «локализованной (вторичной) лимфедемой”. Такой лимфоотек хорошо устраняется компрессионной терапией [13].
Структурные изменения при отеке, выявляемые визуализационными методами исследования, такими как УЗИ, КТ, МРТ не специфичны и редко помогают разграничить различные формы хронического отека [16].
В нескольких исследованиях было продемонстрировано потенциальное влияние лимфедемы на венозный дренаж. BB Lee с соавторами указывает, что лимфатический застой постепенно нарушает и венозный возврат, что в свою очередь усугубляет лимфедему [17].
Дисфункция лимфатической сети в медии венозной стенки может приводить к воспалительной аккумуляции липидов и дальнейшему повреждению адвентиции [18].
Компрессия не эластичным материалом, традиционно используемая в лимфологии, находит все более широкое признание и среди флебологов. С тех пор как были получены данные о клинических и гемодинамических преимуществах не эластической компрессии, при правильном ее использовании [18]. С другой стороны, убедительных доказательств валяния мануального лимфодренажного массажа (МЛД) на скорость заживления трофических язв получено не было, поэтому данный метод не рекомендуется в последних руководствах [19]. С учетом механизма действия этих двух терапевтических опций, логично предположить, что компрессия за счет бандажа или чулка будет препятствовать отеку все время пока конечность находится в компрессии, в то время как МЛД, проводимая специалистом, будет работать лишь непродолжительное время, пока производится массаж. МЛД используется для смягчения рубцово-измененных границ трофической язвы и высоко ценится пациентами. Однако, мануальный лимфодренажный массаж эффективен лишь в тех случаях, когда «парализованные» лимфатические сосуды изменены «обратимо» а не повреждены окончательно. Эта дорогостоящая и очень персонал-зависимая процедура никогда не заменит компрессионную терапию [19].
Другим практическим аспектом комплексного взаимодействия венозной и лимфатической систем является нарушение лимфооттока после травм [20] или хирургических операций на венах [21]. Кроме того, существует много интересных данных о взаимосвязи венозной и лимфатической систем при различных генетических мальформациях, что было отражено в текущих клинических рекомендациях.
Например, первичная флеболимфедема при синдроме Клиппель-Треноне представляет собой комбинацию хронической венозной недостаточности (ХВН) в результате венозной мальформации, а так же лимфатической недостаточности в результате мальформации лимфатических путей. Наиболее частой причиной ХВН при венозных мальформациях является рефлюкс/гипертензия краевых вен из-за дисплазии глубоких вен (агенезия или гипоплазия подвздошной, бедренной вены) или дефектов, нарушающих венозный отток, таких как извитость, стеноз, эктазия, аневризма. Хроническая лимфатическая недостаточность при первичной лимфедеме связана с трункулярными мальформациями (аплазия, гипо- или гиперплазия) [18].
В заключение, следует сказать, что многочисленные флебологи и лимфологи должны объединиться и стать одной большой семьей, чтобы вместе обмениваться опытом и лучше понимать друг друга.
Что такое хроническая венозная недостаточность? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьян А. Г., флеболога со стажем в 31 год.
Определение болезни. Причины заболевания
Хроническая венозная недостаточность (ХВН) — патология, возникающая вследствие нарушений венозного оттока крови в нижних конечностях. Она является одной из самых часто встречаемых болезней, относящаяся к сосудистой системе.
ХВН затрагивает больше женскую половину населения, нежели мужскую. [1] [2] У четверти жителей развитых стран мира можно выявить данное состояние.
Зачастую ХВН путают с варикозным расширением вен нижних конечностей, что является заблуждением. ХВН может существовать и без видимых проявлений расширения вен.
Наследственность, избыточный вес, гиподинамия, ранее перенесённые заболевания сосудистой системы (тромбофлебит или же тромбоз), нарушения гормонального фона и повышенное внутрибрюшное давление, могут являться причинами нарушения оттока крови в нижних конечностях.
У женщин развитие заболевания чаще начинается в период беременности и родов. Во время беременности уровень прогестерона и эстрогена значительно возрастает. Они ослабляют стенки вен. Кроме гормональных изменений, прогрессирование ХВН может быть связано со смещением венозных сосудов в малом тазу, а также с увеличивающейся маткой. Ухудшение состояния венозных стенок может быть связано с изменением давления в венах, при схватках во время родов. Высокий эстрогеновый фон, напряжение стенок вен во время родов являются основными виновниками возникновения заболевания. [7]
Частые и продолжительные статические нагрузки, подъём тяжестей приводят к началу заболевания и его прогрессированию. Пациенты считают нормальным клинические проявления ХВН, связывают их с утомлением и недостаточной физической активностью. К сожалению, больные несвоевременно обращаются к специалистам при первых симптомах заболевания. Наиболее часто ХВН подвержены спортсмены, люди с избыточной массой тела, беременные женщины.
Недооценка серьезности недуга приводит, как правило, к тяжёлым последствиям: расширение вен, их воспаление, тромбообразование, образование трофических язв на нижних конечностях (частые осложнения ХВН). [2]
Симптомы хронической венозной недостаточности
Клинические признаки ХВН многообразны и не зависят от прогрессирования заболевания.
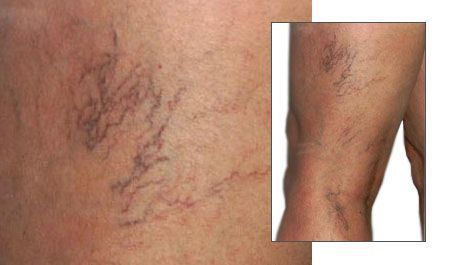
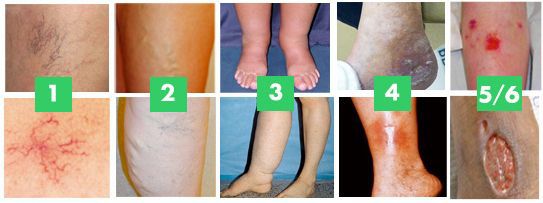
Начальная стадия проявляется одним или сразу комплексом симптомов. Поводом для обращения к специалисту может стать лишь косметический дефект «звездочки» (телеангиэктазии — ТАЭ), а также появление дискомфорта, тяжести в ногах, усиливающейся при длительном пребывании на ногах. Значительно реже могут встречаться спазмы мышц и раздражения кожных покровов, которые могут проявляться в разной степени. Варикозно-расширенных вен может и не быть, но, как правило, при обследовании выявляются признаки поражения внутрикожных вен. [5]
В основном проявление и протекание ХВН сводятся к следующим жалобам:
По мере развития беременности у женщин начинает возрастать степень встречаемости названых признаков. Их появление сокращается в течение недели после рождения ребенка. [7]
Нередко люди с ХВН жалуются на ощущение тепла в ногах, появление зуда, жжения и чувства тяжести. Чаще всего интенсивность симптоматики ХВН усиливается ко второй половине дня или в связи с повышением температуры воздуха.
Возникновение болей в нижних конечностях обусловлено нарушением работы клапанов, приводящего к переходу тока крови из глубоких вен в поверхностные. Вследствие повышения давления в поверхностных венах происходит постепенное нарастание боли, возникает отёчность, сухость и гиперпигментация кожи. [6] Выраженные трофические нарушения могут вызвать открытие язв.
Значительный объём циркулирующей крови (ОЦК) начинает задерживать в нижних конечностях, что приводит к головокружениям, обморокам и сердечной недостаточности. Так как уменьшается ОЦК, людям с выраженным ХВН плохо удаётся справиться с физическими и умственными нагрузками.
При болезненности вен и покраснении над ними кожи в период протекания симптоматики ХВН существует риск, что они могут предшествовать тромбообразованию вен в нижних конечностях.
Патогенез хронической венозной недостаточности
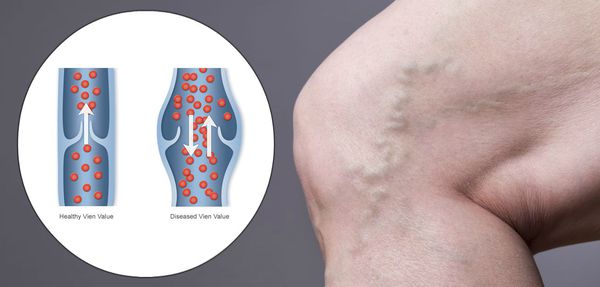
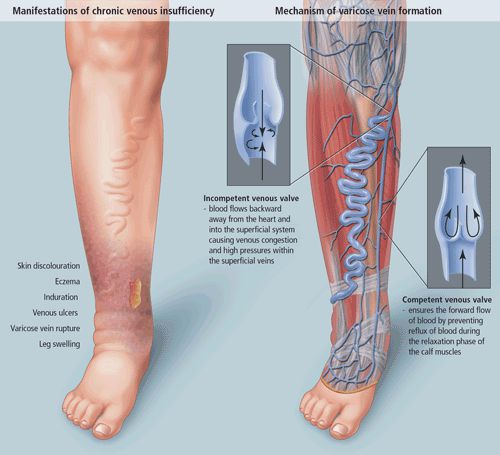
Патогенез ХВН очень специфичен. У здорового человека отток крови происходит через глубокие вены голени. Благодаря совместной работе постоянно сокращающейся и расслабляющейся скелетной мускулатуры и клапанного аппарата кровь направляется к сердцу, где она насыщается кислородом. В процессе этой работы гладкая скелетная мускулатура усиливает давление на вены, а клапанная система, которая состоит из смыкающихся створок, не позволяет крови поддастся силе тяжести.
Из-за длительно существующих факторов риска возникает венозная гипертензия, происходит расширение и выпячивание стенки вен. Створки клапанов расходятся и не могут препятствовать патологическому оттоку крови. Увеличенный объём крови сильнее давит на стенку вены, поэтому вена расширяется. Если не начать лечение, вена продолжит расширяться. Стенки сосудов начнут стремительно терять свою эластичность, их проницаемость увеличится. Через стенки в окружающие ткани будут выходить элементы крови, плазма. Таким образом возникает отёк тканей, что еще больше обедняет их кислородом. В тканях накапливаются свободные радикалы, медиаторы воспаления, запускается механизм активации лейкоцитов. Это нарушает питание и обмен веществ тканей. Конечным итогом становится образование «венозных» трофических язв, что существенно снижает качество жизни пациента. [4] [6]
Классификация и стадии развития хронической венозной недостаточности
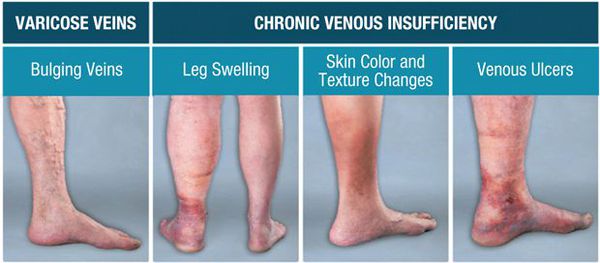
По клиническим признакам выделяют следующие стадии ХВН:
Тромбофлебит можно вылечить только путём хирургического вмешательства. [3] [5]
Осложнения хронической венозной недостаточности
К осложнениям ХВН можно отнести кровотечение из расширенной вены, тромбофлебит и венозную язву. Все эти осложнения возникают на поздних стадиях ХВН при длительном течении заболевания.
Кровотечение из расширенной вены может наступить после травматизации или начаться самопроизвольно. Причиной является нарушение целостности изъязвленных кожных покровов над веной. Как правило, эти вены располагаются в области щиколотки. Эта зона отличается очень высоким давлением в венах, особенно в вертикальном положении тела. Венозная кровь имеет низкую свертываемость, поэтому данные кровотечения при поздней диагностике бывают очень обильными. Неотложная помощь заключается в немедленном переводе больного в горизонтальное положение, конечности придают возвышенное положение и накладывают давящие повязки, если есть возможность выполняется эластичное бинтование. Флебологи могут прошить кровоточащий сосуд или склеить его специальными препаратами. [6]
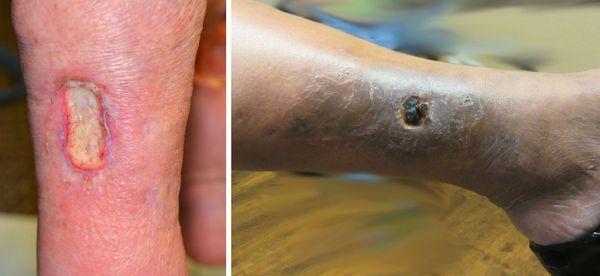
Трофическая язва развивается в нижней трети голени, в зоне максимальных нарушений кожи. Сначала там появляются коричневые пятна — пигментация. Затем в центре возникают белесоватые уплотнения, напоминающие натёк парафина. Это рассматривается как предъязвенное состояние. Даже малейшая травма этого участка может привести к возникновению дефекта кожи.
Возникший дефект кожи начинает прогрессивно увеличиваться, вокруг начинается воспаление кожи. Происходит инфицирование язвы. Она начинает мокнуть, тем самым зона воспаления увеличивается. При сохранении причин, вызвавших образование язвы, она возникает вновь и вновь. Поэтому оптимальная тактика лечения — первоочередное устранение причин, вызвавших язву, и профилактику её рецидива. Консервативное лечение заключается в адекватной эластической компрессии, подборе компрессионного трикотажа для пациентов с трофическими язвами, использовании специальных раневых покрытий для различных стадий воспаления трофической язвы. [3]
Диагностика хронической венозной недостаточности
Важно знать, что в лечении любого заболевания главным является выявление его на ранних сроках, тем самым можно предотвратить возможные осложнения, минимизировать затраты и значительно сократить время лечения.
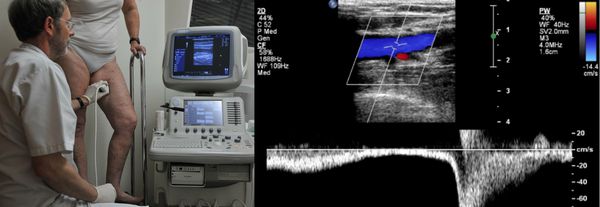
Проведение диагностики ХВН на ранних стадиях способствует ускорению лечения. При диагностике важно определить стадию заболевания. После общего клинического осмотра врач проводит дуплексное ангиосканирование вен нижних конечностей, чтобы определить тактику лечения. Дуплексное ангиосканирование поможет оценить состояние исследуемых сосудов, увидеть места их сужений или расширений, а также выявить тромбообразования.
Для самостоятельной диагностики ХВН достаточно просто посмотреть на свои ноги. Такие симптомы, как отёчность, боли и судороги, а также появление на ногах сосудистых сеток и вен, являются «тревожным звонком» для похода к флебологу.
Одним из самых доступных методов диагностики данного заболевания является УЗИ, главным преимуществом которого является многоразовость применения без рисков для здоровья, безболезненность, а также возможность выявить нарушения в текущей работе венозного аппарата. [3]
Для получения лучшего результата обследование рекомендуется проводить во второй половине дня. Поскольку именно после дневной нагрузки на ноги можно провести более точную оценку состояния клапанов, диаметра вен и степени поражённости стенок. На тактику лечения влияет наличие тромба в просвете вен, который приводит к нарушению тока крови и несёт наибольшую угрозу для жизни пациента.
Лечение хронической венозной недостаточности
Способов лечения ХВН достаточно много. В специализированных клиниках основное место занимаю малоинвазивные методы лечения, то есть оперативные вмешательства с минимальным повреждением кожного покрова.
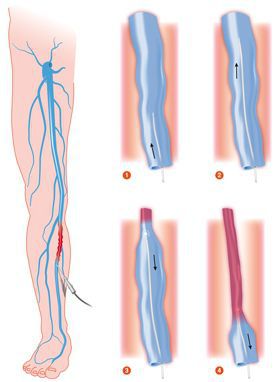
Эндовазальная лазерная коагуляция (ЭВЛК)
В развитых странах помощь с использованием лазерной техники получают до 40% пациентов, страдающих данным заболеванием. При ранней диагностике лечение занимает немного времени и не оставляет следов.Во многих клиниках используется флебологический водяной лазер с длиной волны до 1500 нм, поддерживающий радиальные световоды. Данная технология позволяется закрыть вены любого диаметра через небольшой прокол кожи.
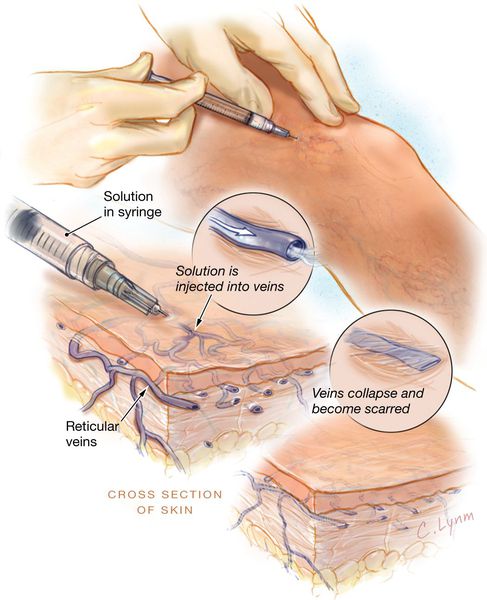
Склеротерапия
Метод склеротерапии основывается на введении склерозанта в просвет поражённого сосуда. Благодаря этому веществу вена заращивается и в дальнейшем исчезает полностью. При более глубоком расположении варикозных вен, применяется методика эхо-склеротерапии. Для более точного внутривенного введения лекарства, процедуру выполняют под контролем УЗИ. С помощью данной методики происходит замещение соединительной тканью, которая исчезает в течение нескольких месяцев. Склеротерапия используется также для устранения наружных косметических проявлений варикоза.
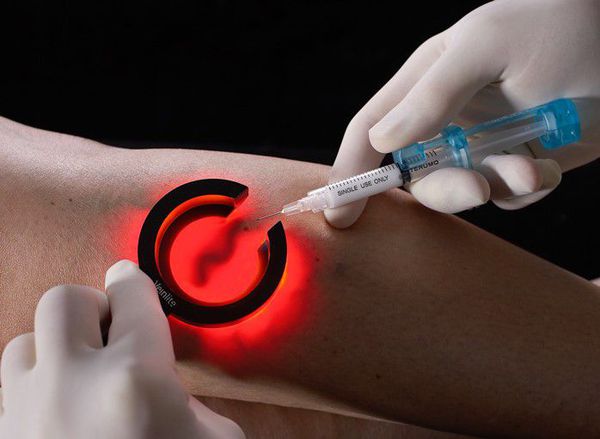
Методика диодной люминесцентной склеротерапии заключается в подсвечивании люминесцентной лампой телеангиоэктазий (до 0,4 мм) или ретикулярных вен (до 2 мм), в просвет которых вводится специальный раствор.
Перспективным направлением в эстетической флебологии является сочетанное применение диодного лазера и склеротерапии — лазерной криотерапии (ClaCS). Данный метод позволяет устранить ретикулярные вены и телеангиоэктазии без особых неприятных ощущений.
Консервативная терапия ХВН заключается в:
Пациенту не стоит волноваться о выборе метода лечения, так как флеболог подберёт индивидуальный вариант терапии в зависимости от возраста и вида деятельности пациента, от формы его заболевания и наличия патологий. Обычно при обращении в крупные флебологические центры специалисты для лечения одного пациента одновременно применяют множество методов. Например, для наиболее эффективного и результативного лечения ХВН выполняют лазерную операцию в сочетании с инъекционными способами лечения вен. [4]
Прогноз. Профилактика
Существуют несколько методов, способствующих снижению риска развития патологии и остановке прогрессирования ХВН.
Наибольший положительный эффект даёт увеличение физической активности. Ежедневные пешие прогулки (желательно 2-3 км), спортивная ходьба, бег, плавание, езда на велосипеде повышают венозное давление. Если для вашей работы характерны длительные ортостатические нагрузки, то старайтесь в течение рабочего дня делать 10-15 минутные перерывы, во время которых разминать мышцы ног или же принимать горизонтальное положение, при этом ноги должны быть приподняты.
При ХВН принятие горячих ванн, посещение бани и сауны строго противопоказано, поскольку вызывает увеличение вен, их переполнение и нарушает отток крови.
Снизить риск усиления симптомов ХВН позволяет сокращение времени пребывания на солнце и в солярии, из-за которых снижается мышечный и венозный тонус.
В остановке прогрессирования ХВН немаловажную роль играет постоянный мониторинг массы тела, ведь чем больше вес человека, тем большей нагрузке поддаются сосуды ног. Из рациона питания следует максимально исключить жиры, соль и сахар, все острое и пряное. Употребление пикантных и солёных блюд вызывает задержку жидкости в организме, отложение жира и увеличение веса. Необходимо употреблять как можно больше грубой клетчатки и пищевых волокон.
Женщинам рекомендуется как можно реже ходить в обуви на высоком каблуке (выше 4 см). Из-за высокого каблука мышцы нижних конечностей поддаются непрерывному напряжению, тем самым увеличивая нагрузку на вены. Чтобы восстановить естественный отток крови, ногам нужно давать отдых в течение нескольких минут, снимая обувь каждые 2-3 часа. Помните, что выбирая свободную, устойчивую и удобную обувь, можно избежать возникновения проблем с сосудами.
Людям, входящим в группу риска развития данной патологии, следует носить исключительно свободную одежду и носки без тугой резинки. Для людей, имеющих склонность к ХВН, рекомендуется носить компрессионный трикотаж, подобранный с помощью консультации специалистов-флебологов. [5] [6]
Хроническая ЛИМФОВЕНОЗНАЯ НЕДОСТАТОЧНОСТЬ нижних конечностей и лимфосцинтиграфия
Отеки нижних конечностей наблюдаются при посттромбофлебитическом синдроме у 80-100% больных в зависимости от формы заболевания. Согласно классификации В. С. Савельева, различают отечную, отечно-варикозную, варикозно-трофическую или трофическу
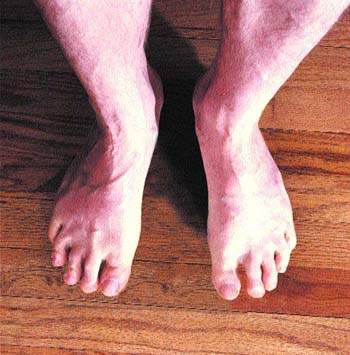 |
Отеки нижних конечностей наблюдаются при посттромбофлебитическом синдроме у 80-100% больных в зависимости от формы заболевания. Согласно классификации В. С. Савельева, различают отечную, отечно-варикозную, варикозно-трофическую или трофическую формы заболевания. Главное внимание при изучении отеков у больных с посттромбофлебитическим синдромом уделялось венозной гипертензии нижних конечностей. С этой позиции рассматривались клапанная недостаточность вен [3], диффузия воды и протеинов в тканях на микроциркуляторном уровне [1, 8], венозная гипертензионная микроангиопатия [14].
Нарушения лимфооттока в нижних конечностях при тромбофлебитическом синдроме изучены в меньшей степени. Основные работы выполнены с помощью рентгенолимфографии. Показано, что на лимфограмме у больного с этим синдромом наблюдаются расширение или, наоборот, сужение и извитость магистральных лимфатических сосудов, плохое контрастирование или отсутствие клапанного аппарата в лимфатических сосудах, их сегментарная облитерация, выраженная сеть патологических коллатералей, множественные анастомозы между лимфатическими сосудами, расширенная сеть лимфатических сосудов кожи, депонирование контрастного вещества с образованием лакун, особенно в области язв и тромбов, регургитация лимфы по лимфатическим сосудам, увеличение или, наоборот, уменьшение размеров паховых лимфатических узлов [2, 4, 9]. Выявлено также замедление эвакуации и изменение характера ресорбции радионуклидных препаратов на стопе.
В настоящей работе представлены результаты дальнейшего изучения основных форм отеков при посттромбофлебитическом синдроме. Наряду с изменениями в венах исследовались нарушения лимфооттока из нижних конечностей с помощью радионуклидной лимфосцинтиграфии.
Всего обследовано 218 больных (190 женщин и 28 мужчин) в возрасте 21 — 75 лет.
Стойкий лимфостаз нижних конечностей имел место у 50% больных с посттромбофлебитическим синдромом, как правило, при отечной и отечно-варикозной формах заболевания. При варикозно-трофической форме синдрома выраженный лимфостаз голеней и стоп встречался крайне редко. Лимфостаза нижних конечностей у больных трофической формой синдрома не наблюдалось. Все больные были прооперированы. У всех установлена реканализованная форма посттромбофлебитического синдрома.
Изучение состояния просвета вен и состоятельности клапанного аппарата поверхностных и глубоких вен нижних конечностей мы выполняли с помощью ультразвукового исследования, используя цветное допплеровское картирование потока крови и анализ спектра допплеровского сдвига частот.
Лимфоотток из нижних конечностей изучался с помощью функциональной радионуклидной лимфосцинтиграфии. Большинство авторов [15, 16] применяли этот метод для обследования больных с лимфедемой нижних конечностей. Лимфостазы при заболеваниях вен нижних конечностей изучены недостаточно.
Метод функциональной радионуклидной лимфосцинтиграфии основан на способности меченых коллоидных частиц после их подкожного введения в ткани поступать в лимфатические сосуды и узлы, которые являются региональными для зон инъекции радиофармакологического препарата. Для исследования применяли препарат лимфоцис, меченый 99m Tc (фирмы “Sorin”, Франция) в количестве 185 МБк в объеме 0,2-0,5 мл. Исследования проводили в гамма-камере. При положении больного лежа на спине радиофармакологический препарат вводили подкожно в первые межпальцевые промежутки стоп. В течение 5 мин после введения препарата больной находился в состоянии мышечного покоя. В это время наблюдали прохождение препарата по лимфатической системе голеней. Через 5 мин проводили трехминутную нагрузку (сгибание-разгибание стоп). После физической нагрузки у части больных отмечалось изменение характера продвижения радиофармакологического препарата на уровне коленных суставов и бедер. После достижения препаратом уровня паховых складок пациенту предлагали походить в течение 40 мин, после чего делали статические снимки области голеней, бедер, таза, печени.
Полученные данные свидетельствуют о том, что при отечных формах посттромбофлебитического синдрома отеки далеко не у всех больных можно объяснить регургитацией крови по магистральным венам, как считалось ранее [4].
При анализе результатов функциональной радионуклидной сцинтиграфии использовались следующие показатели.
1. Тип движения радиофармакологического препарата на сцинтиграмме. При этом различали: магистральное движение по лимфатическим коллекторам (у 25% больных); диффузное движение препарата по интерстицию мягких тканей (15%); смешанное заполнение, при котором отмечали продвижение препарата по магистральным лимфатическим сосудам и диффузную его эвакуацию (60%).
Диффузное движение радиофармакологического препарата на функциональной радионуклидной лимфосцинтиграмме — значимый симптом для определения отека мягких тканей. Он может быть использован, в частности, для диагностики скрытых отеков (латентная стадия лимфостаза), когда клинические данные вызывают сомнение.
2. Скорость движения радиофармакологического препарата (визуализация лимфатических путей голеней по всей длине продолжается в среднем 10 — 15 мин).
3. Характер контрастирования при функциональной радионуклидной лимфосцинтиграфии паховых и подвздошных лимфатических узлов.
Увеличение лимфатических узлов, уменьшение или отсутствие их изображения давали информацию о морфологических изменениях лимфатической системы как на преимущественно пораженной, так и на относительно здоровой конечности.
Исследования показали, что патогенез отеков при выраженном лимфостазе у больных с отечными формами посттромбофлебитического синдрома не может быть полностью объяснен рефлюксом крови по магистральным венам нижних конечностей. Так, у 70 из 81 больного с отечной формой заболевания при одностороннем поражении недостаточность клапанов глубоких вен была выражена в одинаковой степени как на больной, так и на относительно здоровой конечности. При отечно-варикозной форме синдрома недостаточность клапанов глубоких вен была одинаковой на больной и на здоровой конечностях у 38 из 77 больных, а при варикозно-трофической форме у 40 из 60. Следовательно, при отечных формах посттромбофлебитического синдрома рефлюкс крови по магистральным венам далеко не во всех случаях играет ведущую роль при стойких лимфатических отеках. Это нашло подтверждение и в других исследованиях [11]. С помощью ретроградной подколенной флебографии среди больных, страдавших обычным варикозным расширением вен, авторы выявили рефлюкс в системе подколенной вены у 71,1%, из них резко выраженный у 12%, причем лимфостаз у этих больных отсутствовал. Аналогичная закономерность наблюдается также у многих больных с варикозно-трофической формой посттромбофлебитического синдрома, у которых, несмотря на грубые анатомические изменения клапанного аппарата магистральных вен, выраженный лимфостаз нижних конечностей отсутствует.
Основное значение в патогенезе лимфостаза принадлежит нарушению лимфооттока, которое при посттромбофлебитическом синдроме осложняет заболевания периферических вен [10].
Из 218 больных лишь у 44 сохранился естественный для человека чисто магистральный тип движения радиофармакологического препарата, причем во всех случаях контрастирование лимфатических сосудов и регионарных лимфатических узлов было усилено вследствие хронического динамического застоя лимфы. У 121 больного наряду с движением препарата по магистральным лимфатическим путям отмечалось его диффузное перемещение по интерстицию. Предполагается, что диффузное заполнение происходит вследствие распространения радиофармакологического препарата по расширенной сети мельчайших лимфатических сосудов. Не исключено также прямое диффундирование радиофармакологического препарата при отеках по интерстицию из депо препарата на стопе (эффект растекания чернильного пятна по промокательной бумаге).
Наряду с характером продвижения радиофармакологического препарата на голенях, важное значение имела также скорость его распространения в проксимальном направлении. Оказалось, что этот параметр имел определенное прогностическое значение. У 62 больных с ускоренным движением препарата (3-6 мин) после операции на венах с лимфодренирующим вмешательством отмечался стойкий хороший результат. Рецидивов отека у этих больных не было на протяжении всего периода наблюдения (3-4 лет). Наоборот, при замедленной скорости движения препарата (20 мин и более) наблюдался хороший эффект в ближайшем послеоперационном периоде и рецидив отека в отдаленные сроки.
У больных со средней скоростью движения радиофармакологического препарата по голени (10-15 мин) непосредственные результаты после операции не были столь отчетливы, как у пациентов с ускоренным движением препарата. У 56% больных были отмечены рецидивы отеков разной интенсивности. Сложилось предварительное мнение, что скорость движения препарата определяется состоянием насосной функции лимфатических капилляров больной конечности.
Наиболее важным показателем анатомической проходимости путей лимфооттока было изображение подвздошных лимфатических узлов. У всех больных контрастирование подвздошных лимфатических узлов преимущественно на больной конечности было в разной степени снижено по сравнению с относительно здоровой конечностью. У 50 больных контрастирование подвздошных лимфатических узлов на стороне больной конечности отсутствовало, а на стороне здоровой конечности было удовлетворительным. Менее показательной оказалась функциональная радионуклидная лимфосцинтиграфия паховых лимфатических узлов. Из 218 больных у 143 включение радиофармакологического препарата в паховые лимфатические узлы на стороне поражения было снижено по сравнению со здоровой стороной. У 26 больных накопление препарата в паховых лимфатических узлах на стороне больной конечности было интенсивнее, чем на здоровой. У 49 больных паховые лимфатические узлы контрастировались симметрично на больной и здоровой стороне.
Клинически отеки классифицировали как проходящие, частично проходящие и не проходящие. При проходящих отеках избыточная величина окружности на уровне лодыжек по сравнению с относительно здоровой конечностью не превышала 1,5–2,5 см. При этой форме отеки возникали к концу рабочего дня и за ночь исчезали. Отечная жидкость у таких больных содержала относительно мало белка, по нашим данным, не более 15-20 г/л, что соответствует норме содержания белка в лимфе нижних конечностей [12].
Проходящие отеки хорошо поддавались лечению с помощью регулярной эластичной компрессии (бинты, чулки, колготы) и после операции на венах уменьшались, у большинства больных исчезая полностью. Проходящие отеки наблюдались преимущественно при варикозно-трофической форме посттромбофлебитического синдрома. Больные с проходящими, то есть преимущественно флебогенными, отеками в данное исследование не вошли. Частично проходящие отеки характерны для отечной и отечно-варикозной форм заболевания. При варикозно-трофической форме отеки этого типа встречались редко. У таких больных избыточная окружность голени в дистальных отделах достигала 4-5 см и более. Достаточно длительный постельный режим (до трех суток и более) приводил к частичному уменьшению отека: рассасывалась лишь так называемая “подвижная” водянистая часть отека. При этом периметр голени в относительно легких случаях уменьшался на 50-60%, в более тяжелых лишь на 10-15%. Основная, “стойкая”, не проходящая часть отека оставалась, несмотря на соблюдение больными постельного режима, компрессионную терапию и наружное дренирование. Содержание белка в тканевой жидкости после рассасывания проходящей части отека составляло 32-35 г/л, что соответствует данным литературы [12, 13].
Полученные результаты подтвердили, что при посттромбофлебитическом синдроме частично проходящие отеки образуются не только из-за венозной гипертензии, но и в результате затруднения лимфооттока, вызванного нарушением проходимости магистральных лимфатических сосудов и регионарных лимфатических узлов. Лимфостаз все более осложняет венозную недостаточность при посттромбофлебитическом синдроме нижних конечностей. Чем больше содержится в тканевой жидкости белка, тем более нарастает отек вследствие задержки воды в мягких тканях. При нарастании отека слабеет насосная функция лимфатических капилляров, одновременно снижается резорбционная способность кровеносных капилляров [17]. Отеки постепенно приобретают стойкий характер. Декомпенсация оттока тканевой жидкости развивается на протяжении ряда лет, иногда десятилетий.
При несвоевременном лечении отеки становятся постоянными. Клинически отеки приобретают черты лимфедемы (слоновости). У таких больных во время операций на конечностях отмечали гипертрофию подкожного жирового слоя (толщина его до 6-7 см). Избыточный жир располагался циркулярно, главным образом в дистальных сегментах голени. Жировые дольки патологически увеличивались до 3-3,5 см в диаметре.
В особенно тяжелых случаях в области лодыжечного сегмента наблюдали прогрессирующий фиброз межтканевых перегородок; у таких больных жировая ткань приобретала мелкодольчатое строение и крошилась, когда до нее дотрагивались. При отсутствии своевременного лечения к 50-60 годам у больных возникали тяжелые инвалидизирующие осложнения: грубо нарушался внешний вид голени и стопы, у некоторых пациентов возникала чрезкожная лимфорея, хронический дерматоз, вспышки рожистого воспаления, на голени появлялись обширные глубокие трофические язвы.
При хирургическом лечении отечных форм посттромбофлебитического синдрома одновременно производили операции на венах и лимфодренирующее вмешательство: формирование лимфовенозных анастомозов, фенестрацию фасции голени, наружное дренирование и липосакцию.
Итак, при посттромбофлебитическом синдроме имеют место три формы отека нижних конечностей: проходящие, частично проходящие и не проходящие. Проходящие отеки возникают в результате флебостаза. Они исчезают после операций на венах и последующей консервативной терапии. Причиной частично проходящих и непроходящих отеков является венозная недостаточность, осложненная нарастающим лимфостазом в результате нарушения проходимости магистральных лимфатических путей, паховых и, особенно, подвздошных лимфатических узлов, угнетения насосной функции лимфатических капилляров.
Полученные с помощью лимфосцинтиграфии данные помогают уточнить диагноз лимфостаза, установить уровень и протяженность блока лимфатической системы, степень нарушения ее функции, определить показания к проведению лимфодренирующих вмешательств при операциях на венах, выбрать наиболее целесообразный способ дренирования лимфы и прогнозировать результаты хирургического лечения.