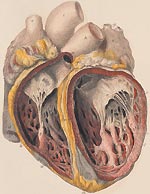
вегетация клапана сердца что такое
Кардиолог «СМ-Клиника» рассказала о течении инфекционного эндокардита
Если бактерии или вирусы попадают внутрь сердца, они могут привести к воспалению, которое чревато серьезными проблемами вплоть до инфарктов и инсультов. Что это за болезнь и как распознать ее вовремя?
АЛЕНА ПАРЕЦКАЯ
Врач-патофизиолог, иммунолог, член
Санкт-Петербургского общества патофизиологов
АННА ГРЕБЕННИКОВА
К.м.н., врач-кардиолог «СМ-Клиника»
При инфекционном эндокардите страдает не только внутренняя поверхность сердца, но и клапаны. В итоге развиваются тяжелые пороки, которые затем требуют операции, чтобы сердце могло нормально работать.
Что нужно знать об инфекционном эндокардите
Что такое эндокардит
Причины инфекционного эндокардита у взрослых
Наиболее часто к инфекционному эндокардиту приводит проникновение в кровь патогенных возбудителей. Это бактерии, вирусы, реже – грибки. Они разносятся по телу, оседают на внутренних стенках сердца, повреждая их и провоцируя образование тромбов.
При разных формах инфекционного эндокардита воспаление провоцируют разные виды микроорганизмов. Если это подострая форма (длящаяся более 2 месяцев) – это, как правило, стрептококк и стафилококк. Бактерии обычно попадают из полости рта и пищеварительной системы.
Если это острый эндокардит – его причинами чаще бывают гонококк, пневмококк и стафилококк. Нередко эти бактерии провоцируют пороки сердца.
После протезирования клапанов эндокардит связан с попаданием патогенов при операции. Опасны стафилококки, гемофильная палочка, грибки.
Эндокардит правой половины сердца часто вызван условно-патогенной флорой – кандидозом, стафилококком, может развиваться после катетеризации и введения препаратов.
Факторы риска для развития бактериального эндокардита:
Симптомы инфекционного эндокардита у взрослых у взрослых
Лечение инфекционного эндокардита у взрослых у взрослых
Диагностика
Заподозрить это заболевание только по симптомам сложно. Необходимо провести целый ряд дополнительных исследований. К ним относятся:
Современные методы лечения
– Согласно российским и европейским рекомендациям, успешное лечение инфекционного эндокардита основано на уничтожении возбудителей заболевания антимикробными препаратами, – говорит врач-кардиолог Анна Гребенникова. – Лечение следует начать немедленно. До получения результатов посева проводится антибактериальная терапия. При выделении конкретного возбудителя, определяют его чувствительность к антибиотикам.
Операцию назначают, если эндокардит вызван золотистым стафилококком или другими устойчивыми к антибиотикам бактериями. Так же она показана, если начался абсцесс клапанов сердца и околоклапанных структур – это жизнеугрожающее состояние и лечить одними антибиотиками такие осложнения нельзя. Основные задачи оперативного вмешательства – удаление пораженных тканей и восстановление функциональной анатомии сердца.
В целом, показаниями к хирургическому лечению являются:
И помните: чем раньше врач распознает эндокардит, чем скорее он назначит адекватную терапию, тем больше шансов и пациента выжить.
Профилактика инфекционного эндокардита у взрослых у взрослых в домашних условиях
Если есть повышенный риск развития инфекционного эндокардита, необходимо регулярно обследоваться у врача. Важно также пролечить все очаги инфекции – кариозные зубы, мочевыделительный тракт, больное горло.
При проведении любых манипуляций необходимо тщательно следить за состоянием здоровья, принимать все препараты, которые порекомендует врач для профилактики.
Также важно защищаться от инфекций – сделать прививку от гриппа, пневмококковой и гемофильной, менингококковой инфекции, защищаться от ОРВИ.
Популярные вопросы и ответы
Инфекционный эндокардит – тяжелое воспалительное заболевание эндокарда (внутренней оболочки сердца), чаще протекающее с поражением клапанов сердца, и реже поражающее другие структуры сердца: перегородки, хорды, стенки предсердий или желудочков, околоклапанные структуры. О том, чем опасна эта болезнь, нам рассказала врач-кардиолог Анна Гребенникова.
Часто ли болеют инфекционным эндокардитом?
В последнее время соотношение основных факторов риска заболевания изменилось. Наиболее важную роль стали играть инъекционная наркомания, кардиохирургические операции и инвазивные медицинские вмешательства (катетеризация вен, гемодиализ, имплантация кардиостимуляторов), что привело к смене ведущего возбудителя, которым в настоящее время является золотистый стафилококк и стрептококк (Streptococcus viridans).
Какие могут быть осложнения при инфекционном эндокардите?
На фоне инфекционного эндокардита могут возникать миокардиты (воспаление мышцы сердца) и перикардиты (воспаление сердечной сумки), которые приводят к различным нарушениям ритма сердца.
Также одним из осложнений являются инфекционные аневризмы – результат септической артериальной эмболии с последующим распространением инфекции.
Острая почечная недостаточность также является частым осложнением инфекционного эндокардита и может ухудшить прогноз заболевания. Ведение пациента после операции должно соответствовать обычным рекомендациям после хирургии клапанов.
Когда вызывать врача на дом при инфекционном эндокардите?
При подозрении на инфекционный эндокардит показано немедленное обращение к врачу с дальнейшей госпитализацией в стационар для ведения пациента «командой эндокардита» – мультидисциплинарной командой в составе кардиолога, сердечно-сосудистого хирурга, инфекциониста, клинического фармаколога.
Можно ли лечить инфекционный эндокардит народными средствами?
Самолечение и лечение инфекционного эндокардита народными средствами недопустимо.
Излечивается ли эндокардит или останутся последствия?
Согласно Европейским и Российским рекомендациям по инфекционному эндокардиту, пациентов следует обучить признакам и симптомам болезни после выписки. Они должны помнить о риске рецидива и о том, что появление жара, озноба и других признаков инфекции требует обязательного и немедленного обращения к врачу. Необходимо регулярно, особенно в течение первого года после перенесенного инфекционного эндокардита, наблюдаться у кардиолога, выполнять ЭхоКГ.
Необходимо также проводить санацию ротовой полости, избегать татуировок и пирсинга, регулярно проводить санацию хронических очагов инфекции.
Бактериальный эндокардит
Бактериальный эндокардит что это за заболевание и насколько оно опасное для жизни? Патология характеризуется воспалением эндокарда и имеет инфекционный генез. Поражает преимущественно клапаны сердца, реже — хорды, перегородки, стенки предсердий или желудочков. Если своевременно не начать лечение, то болезнь приводит к тяжелым последствиям: септический шок, эмболии в сердце, головной мозг, РДСН, сердечная недостаточность, летальный исход. Помимо этого часто развиваются осложнения на внутренние органы: страдают почки, печень, селезенка, НС, сосуды.
Чтобы не допустить подобных осложнений обращайтесь в «Клинику АВС» при малейших подозрениях на данную патологию. В нашем медицинском центре работают высококвалифицированные специалисты, имеющие научные степени, высшую категорию, профессорские звания. Это врачи с многолетним опытом в лечении сердечно-сосудистых заболеваний, поэтому быстро поставят верный диагноз и назначат индивидуальную программу лечения для каждого пациента, учитывая тяжесть протекания патологии, состояние здоровья, возраст и другие факторы.
Статистика
Бактериальный эндокардит это патология, которая поражает чаще лиц мужского пола. Смертность достаточно высокая и составляет порядка 25-30 % от общего количества больных с подобным диагнозом, у пожилых людей — более 40 %.
Описание
Расшифровка кода I33.0 по справочнику МКБ-10: болезнь «Подострый и острый эндокардит». Проявления патологии во многом зависят от формы ее протекания:
Причины
Бактериальный эндокардит это заболевание и что способствует его развитию? Чаще всего источником поражения служит зеленящий стрептококк, золотистый, эпидермальный стафилококк, энтерококк, пневмококк или же кишечная палочка. Присоединению патогенной микрофлоры к эндокарду способствуют местные и общие факторы. К числу последних относят: нарушение работы иммунной системы, алкоголизм, наркомания, пожилой возраст. Местные факторы: врожденные, приобретенные патологии сердца, нарушения гемодинамики при пороках сердца.
Развитию болезни способствуют условия, которые ослабляют иммунологическую реактивность организма. В группе риска лица с травматическими, атеросклеротическими и ревматическими повреждениями сердечных клапанов.
Высокая вероятность развития патологии у пациентов с ДМЖП, коарктацией аорты, гипертрофической кардиомиопатией, протезами клапанов, электрокардиостимуляторами. Часто болезнь развивается у наркозависимых.
Симптомы эндокардита у взрослых
Симптомы и лечение эндокардита у взрослых зависят от длительности протекания болезни, возраста пациента, разновидности возбудителя и других факторов.
При высокопатогенном возбудителе инфекции развивается острый эндокардит и синдром полиарганной недостаточности, поэтому можно выделить симптомы эндокардита у взрослых:
При подострой форме развиваются эмболии сосудов мозга, селезенки, почек тромбами, которые оторвались со створок сердечных клапанов. Подобная клиника сопровождается инфарктами в пораженных органах.
Обследования указывают на развитие миокардита, наличие функциональных шумов, которые связаны с анемией и поражением клапанов. Если повреждены створки митрального и аортального клапанов определяются признаки эндокардита их недостаточности.
В некоторых случаях признаки эндокардита включают стенокардию. Пороки клапанов и повреждение сердечной мышцы осложняются сердечной недостаточностью. Обнаруживается гепатоспленомегалия, гломерулонефрит, возможны артралгии, полиартрит.
Диагностика
Поскольку клиника вариабельна, неспецифична и часто развивается незаметно, диагностика требует высокой настороженности. Поэтому специалисты «Клиники АВС» используют разные методы диагностики: лабораторные и инструментальные.
Лечение
Лечение заключается в длительном курсе антибиотикотерапии (гликопептиды, цефалоспорины, иногда аминогликозиды, обычно в/в): 2-8 недель, поэтому в ряде случаев терапия амбулаторная. Потребность в оперативном вмешательстве может понадобиться при деструкции клапанов или резистентности к медикаментам. Предполагаемые первоисточники бактериемии должны быть устранены:
Если эффект от фармакотерапии отсутствует назначают операцию: установка протеза клапанов сердца и иссечение пораженных участков (но после стихания обострений патологии). Кардиохирурги «Клиники АПВС» проводят хирургическое вмешательство исключительно по показаниям и дополняют терапию приемом антибиотиков.
Ключевые моменты
Бактериальный эндокардит — тяжелая патология, прогноз которой зависит от своевременности диагностики и адекватности лечения. Если не обратиться за медицинской помощью при острой форме заболевания, то спустя несколько месяцев наступает летальный исход.
Не откладывайте визит к врачу, если имеются подозрения на заболевания сердца. Врачи «Клиники АВС» определят симптомы и лечение эндокардита, назначат адекватную антибактериальную терапию и при необходимости проведут хирургическое вмешательство, что поможет улучшить прогноз и качество жизни пациента.
«Клиника АВС» имеет безупречную репутацию, благодаря европейскому уровню медицинского обслуживания, высокотехнологичному диагностическому оборудованию, компетентности персонала.
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ: диагностика, клиническое течение, лечение
Инфекционный эндокардит (ИЭ) относится к числу тяжелых заболеваний с высоким уровнем летальности. В отсутствии лечения смертность при ИЭ составляет 100%. В последние годы отмечается значительный рост числа больных эндокардитом в нашей стране и за рубеж
Инфекционный эндокардит (ИЭ) относится к числу тяжелых заболеваний с высоким уровнем летальности. В отсутствии лечения смертность при ИЭ составляет 100%. В последние годы отмечается значительный рост числа больных эндокардитом в нашей стране и за рубежом. По данным различных авторов, сегодня выросла заболеваемость в пожилом и старческом возрасте, а также среди лиц в возрасте до 30 лет, использующих внутривенное введение наркотиков [1, 2].
Известно, что ИЭ представляет собой заболевание инфекционной природы с первичной локализацией возбудителя на клапанах сердца, пристеночном эндокарде, протекающее с проявлениями системной инфекции, сосудистыми осложнениями и иммунной реакцией [3, 4, 5].
Традиционно развитие ИЭ связывают с наличием «внутрисердечных» факторов риска, к которым относят врожденные и приобретенные пороки сердца, наличие протезированных клапанов, пролапсов клапанов и другие аномалии [6]. В последние годы к категории лиц повышенного риска отнесены больные с очаговой инфекцией, а также лица, у которых применялись инвазивные методы исследования, включая установку подключичного катетера [7]. Особую группу риска составляют наркоманы, практикующие внутривенное введение наркотиков, у которых ИЭ протекает с поражением интактных клапанов сердца.
В данной работе обобщен опыт диагностики и ведения больных ИЭ на базе общетерапевтического отделения Александровской больницы Санкт-Петербурга за период 1998–2003 гг. Диагностика заболевания осуществлялась в соответствии с критериями Duke [8]. Диагноз ИЭ оценивался как достоверный при наличии двух главных критериев, а именно:
Нами было проведено обследование 105 больных ИЭ, из них у 80 человек в возрасте от 18 до 30 лет (первая группа) основным фактором риска заболевания являлась инъекционная наркомания.
Во второй группе больных (25 чел.) основными предрасполагающими факторами развития ИЭ были врожденные и приобретенные пороки сердца, а также протезированные клапаны.
У лиц старшей возрастной группы дополнительным фактором риска являлись дегенеративно-дистрофические изменения клапанов сердца.
Взаимосвязь характера поражения клапанов сердца и факторов риска ИЭ представлена в таблице 1.
По данным эхокардиографического исследования, у 100% больных первой группы были выявлены подвижные вегетации на створках трикуспидального клапана (ТК), что сопровождалось формированием его недостаточности I—III степени.
Во второй группе больных ИЭ отмечалось поражение левых камер сердца с образованием вегетаций на створках аортального и митрального клапанов. Изолированное поражение митрального клапана наблюдалось у двух человек с ревматическим пороком сердца (митральный стеноз), у одной больной с врожденным дефектом межжелудочковой перегородки и в единственном случае обструктивной формы гипертрофической кардиомиопатии.
Среди лиц пожилого и старческого возраста у девяти человек (36%) определялось изолированное поражение аортального клапана в отсутствии признаков аортального стеноза. Наряду с этим, у пяти больных (20%) в возрасте от 72 до 87 лет ИЭ развился на фоне аортального порока атеросклеротического генеза, причем у всех пятерых было выявлено сочетанное поражение аортального и митрального клапанов. Дегенеративно-дистрофические изменения других клапанов сердца определялись у 100% больных старшей возрастной группы.
Образование вегетаций на створках аортального клапана наблюдалось у двух больных с третичной формой сифилиса на фоне имеющегося аортального порока, связанного со специфическим процессом в аорте.
В двух случаях мы наблюдали развитие эндокардита протезированных клапанов.
При сопоставлении результатов посевов крови в двух группах больных определялись существенные различия как в частоте выделения микробной флоры, так и в видовом составе возбудителей эндокардита. По нашим данным, возбудителем ИЭ у больных-наркоманов в 71,3% наблюдений (57 чел.) являлся золотистый стафилококк, тогда как во второй группе, наряду с кокковой флорой, чаще обнаруживались грамотрицательные микроорганизмы (28%). Отрицательные результаты посевов крови значительно реже наблюдались в первой, чем во второй, группе больных ИЭ: 18,7% и 56% — соответственно. Данные относительно этиологической структуры ИЭ в обследуемых группах больных представлены в таблице 2.
Клиническая характеристика и особенности течения ИЭ
Клиническое течение и характер осложнений инфекционного эндокардита во многом зависят от локализации клапанных вегетаций — в правых или левых камерах сердца, а также степени вирулентности возбудителя заболевания.
Течение ИЭ у больных-наркоманов отличалось особой тяжестью и полисиндромностью. Причиной госпитализации у большинства больных были острые осложнения основного заболевания. Значительная часть больных поступала в реанимационное отделение стационара с клиническими симптомами одно- или двухсторонней многофокусной пневмонии, причиной которой являлась септическая тромбоэмболия ветвей легочной артерии (72% больных). Течение пневмонии сопровождалось тяжелой дыхательной недостаточностью, нередко с развитием респираторного дистресс-синдрома (РДСВ) и очагами деструкции в легких (12%). Проявления вторичной нефропатии, которые обнаруживались у 100% больных в первой группе, иногда ошибочно трактовались как обострение хронического гломеруло- или пиелонефрита, мочекаменной болезни, что служило поводом для госпитализации этих больных в урологическое и нефрологическое отделения.
Во второй группе больных основной причиной госпитализации была длительная фебрильная лихорадка в сочетании с анемией и гепатолиенальным синдромом. Наряду с этим, у пяти человек (20%) поводом для госпитализации послужила прогрессирующая сердечная недостаточность.
Основные клинические синдромы, наблюдаемые у больных ИЭ первой и второй групп, представлены в таблице 3.
По нашим наблюдениям, характерной особенностью клинического течения ИЭ у больных-наркоманов являлась высокая частота септической ТЭЛА с формированием множественных очагов инфильтрации в легких. У многих больных легочные тромбоэмболии носили рецидивирующий характер (31,3% больных) и нередко осложнялись развитием деструктивных очагов в легких.
Образование вегетаций у 100% больных первой группы сопровождалось недостаточностью трехстворчатого клапана I—III степени с формированием потоков регургитации. Вместе с тем, у большинства пациентов не определялось тяжелых нарушений центральной гемодинамики, связанных с дисфункцией ТК. В данной группе больных характерной клинической особенностью был обратимый характер нарушений гемодинамики на фоне проводимой терапии. Острая сердечная недостаточность с дилятацией полостей сердца и снижением фракции выброса до 40% и ниже наблюдалась у 28 больных (35,3%) в связи с присоединением острого миокардита или на фоне сочетанного поражения клапанов сердца.
Вторичная нефропатия являлась одним из самых распространенных синдромов в первой группе больных ИЭ. Острая почечная недостаточность наблюдалась у 16 больных, причем у 10 из них она носила обратимый характер и была связана с острым ДВС-синдромом, а также с острой сердечной недостаточностью с отеками. Инфекционно-токсическая нефропатия регистрировалась в 73,8% наблюдений и сопровождалась мочевым синдромом — гематурией, протеинурией, лейкоцитурией — при достаточном уровне клубочковой фильтрации.
Характерной особенностью ИЭ во второй группе было подострое течение заболевания с длительным периодом лихорадки на догоспитальном этапе, причем в пожилом и старческом возрасте лихорадка носила субфебрильный характер с редкими подъемами температуры до фебрильных цифр.
Большинство больных подострым инфекционным эндокардитом (ПИЭ) поступали в стационар в стадии развернутой клинической картины заболевания с клиническими признаками тромбоэмболии сосудов большого круга кровообращения. В данной группе больных наиболее распространенными следует признать такие осложнения, как церебральные эмболии с развитием ишемических и геморрагических инсультов, эмболии почечных сосудов с болевым синдромом и гематурией, а также формирование острых очаговых изменений в миокарде, связанных с эмболией коронарных сосудов или прикрытием устьев коронарных артерий вегетациями [9].
Септические тромбоэмболии церебральных сосудов нередко сопровождались развитием гнойного менингоэнцефалита с летальным исходом. Вместе с тем, при посевах крови у 56% больных второй группы не получено роста микробной флоры. Обращает на себя внимание тот факт, что септицемия у больных с положительными результатами посевов крови в 28% наблюдений была обусловлена грамотрицательной микрофлорой. В этой категории больных источником бактериемии являлись очаги хронической инфекции в мочеполовой системе, а у двух больных (по данным аутопсии) был выявлен двухсторонний апостематозный нефрит.
У значительного числа больных ПИЭ (62%) определялись признаки острой недостаточности кровообращения с застойными хрипами в легких, легочной гипертензией, увеличением полостей сердца и периферическими отеками.
В этой группе больных чаще, чем в первой, наблюдалась преренальная азотемия и ОПН, связанные с развитием острой недостаточности кровообращения.
Острый диффузный миокардит, типичными проявлениями которого были различные нарушения ритма, диагностирован у 27% больных второй группы.
Анемия со снижением уровня гемоглобина до 80 г/л и менее выявлена у 100% больных второй группы. Значительное увеличение СОЭ (более 45 мм/ч) наблюдалось у 85,8% больных подострым ИЭ.
Кожные изменения в виде геморрагических высыпаний, пурпуры Шенлейн-Геноха, а также другие проявления иммунного воспаления в обеих группах больных встречались нечасто — 6,3 и 4% в первой и второй группах, соответственно.
Лечение больных ИЭ
Консервативная терапия больных ИЭ проводилось с использованием антибиотиков широкого спектра действия в сочетании со средствами дезинтоксикационной, антикоагулянтной и метаболической терапии. В составе антибактериальной терапии больные получали цефалоспорины III-IV поколений в комбинации с аминогликозидами и метронидазолом. Из группы цефалоспоринов назначались: цефтриаксон (лонгацеф) 2 г в сутки внутривенно (в/в), или цефотаксим (тальцеф) 2 г в сутки в/в, или цефепим (максипим) 2 г в сутки в/в в сочетании с аминогликозидами (амикацин в суточной дозе 1,5 г в/в) и метронидазолом по 1,5-2 г в сутки в/в. В случае, если такая терапия оказывалась неэффективной или существовали противопоказания к вышеперечисленным препаратам, применялись антибиотики группы линкозаминов: клиндамицин 1,2 г в сутки в/в или линкомицин 3 г в сутки в/в в сочетании со фторхинолонами (ципрофлоксацин 400 мг в сутки в/в). В условиях отделения реанимации в течение пяти–семи дней проводилась терапия имипинемом (тиенамом) в дозе 2—4 г в сутки в/в или рифампицином в суточной дозе 0,45—0,6 г в/в. Средняя продолжительность курса антибиотикотерапии в обследуемой группе больных составила 28 + 3,5 дней.
Дезинтоксикационная терапия включала в себя внутривенные инфузии реополиглюкина, гемодеза, поляризующих смесей в сочетании с петлевыми диуретиками. Объем вводимой жидкости составлял в среднем 2-2,5 л в сутки. В течение всего периода инфузионной терапии осуществлялся контроль за функциональным состоянием почек, электролитным составом крови, суточным диурезом. В условиях отделения реанимации у всех больных осуществлялся мониторинг ЦВД. Инфузионная терапия проводилась в течение всего острого периода заболевания до купирования проявлений интоксикационного синдрома. Средняя продолжительность курса составила 22 + 4,5 дня.
Развитие легочной эмболии, особенно в сочетании с признаками острого ДВС-синдрома в стадии гиперкоагуляции, служило основанием для назначения антикоагулянтной терапии. Начальная доза гепарина составляла 10 тыс. ЕД внутривенно, струйно, за-тем — по 1000 ЕД в час внутривенно, капельно с переходом на подкожное введение до 30 тыс. ЕД в сутки. Введение гепарина осуществлялось под контролем показателей коагулограммы и времени свертывания крови. Одновременно проводились внутривенные трансфузии свежезамороженной плазмы по 300 мл в сутки с добавлением 2500–5000 ЕД гепарина. Анемия тяжелой степени (Нb менее 80 г/л, Ht ≤25) корригировалась переливаниями эритроцитарной массы (пять–семь доз). При наличии гипопротеинемии использовалось введение растворов аминокислот, альбумина или нативной плазмы. Выявление клинических и рентгенологических признаков отека легких на фоне рецидивирующего течения септической ТЭЛА служило показанием для назначения кортикостероидов (преднизолон от 120 до 200 мг в сутки внутривенно капельно). Терапия антикоагулянтами прямого действия в сочетании с трансфузиями криоплазмы проводилась до стойкого улучшения показателей гемостаза. Критериями нормокоагуляции являлись уровень фибриногена в плазме 3-4 г/л, отсутствие тромбоцитопении, нормализация ВСК, АЧТВ, тромбинового времени, а также отрицательные паракоагуляционные тесты. По нашим данным, купирование проявлений острого ДВС-синдрома на стадии гиперкоагуляции у 75% больных отмечалось на седьмой–десятый день от начала комплексной терапии.
У части больных формировалась резистентность к проводимой антибактериальной терапии, которая характеризовалась нарастанием интоксикации, фебрильной лихорадкой, прогрессирующей анемией, а также высевами из крови возбудителя ИЭ – золотистого стафилококка — в 65% наблюдений. При рентгенологическом обследовании данной категории больных с большой частотой определялись очаги деструкции легочной ткани, а у трех больных гнойный выпот в плевральной полости.
Длительное применение антибиотиков широкого спектра действия у 70,3% больных (38 чел.) сопровождалось развитием побочных эффектов антибактериальной терапии. Кандидоз полости рта глотки, пищевода, а также кишечный дисбактериоз III-IV стадии был выявлен у 36 больных (66,7%). Применение антибиотиков с гепатотоксическими свойствами (цефалоспорины, линкозамины, метронидазол) у двух больных (3,7%) с хроническим гепатитом С и В приводило к прогрессированию печеночной недостаточности, которая сопровождалась высокой ферментемией (АЛТ 1500 ЕД, АСТ 1000 ЕД) и желтухой.
Развитие застойной сердечной недостаточности с появлением акроцианоза, влажных хрипов в базальных отделах легких, периферических отеков в сочетании с кардиомегалией и падением фракции выброса до 50—45% наблюдалось у пяти больных (9,3%) на фоне массивной инфузионной терапии.
Длительная антикоагулянтная терапия в 20,4% (11 чел.) наблюдений сопровождалась повышением толерантности плазмы к гепарину, что клинически выражалось в развитии периферических флеботромбозов, в то время как гепарининдуцированной тромбоцитопении в обследуемой группе больных мы не наблюдали.
Положительные результаты консервативной терапии были получены у 70,2% больных (56 чел.) с поражением ТК и лишь у 32% пациентов (6 чел.) из второй группы. Исходом ИЭ в обеих группах больных являлось формирование недостаточности клапанов сердца.
Госпитальная летальность при ИЭ у наркозависимых лиц составила 29,4% (24 чел.), тогда как у больных с поражением левых камер сердца (вторая группа) уровень смертности составил 68% (19 чел.).
По данным аутопсии, основными причинами смерти больных ИЭ были:
Таким образом, характерные особенности ИЭ у лиц с наркотической зависимостью — это острое течение заболевания с поражением правых камер сердца и рецидивами септической ТЭЛА. Возбудителем ИЭ у инъекционных наркоманов в 71,3% является высоковирулентный золотистый стафилококк. Формирование недостаточности трехстворчатого клапана I—III степени стало самым распределенным осложнением ИЭ у наркоманов. При этом у большинства больных не наблюдается тяжелых нарушений центральной гемодинамики, приводящих к развитию острой недостаточности кровообращения.
Подострый ИЭ у больных с предрасполагающими заболеваниями сердца, а также у лиц пожилого и старческого возраста протекает с преимущественным поражением левых камер сердца, причем в старшей возрастной группе преобладает моноклапанное поражение. Наличие сопутствующей патологии у лиц старше 60 лет маскирует течение основного заболевания, чем и обусловлены поздняя диагностика и высокая смертность больных. Для затяжного течения ИЭ характерна низкая высеваемость возбудителя, по сравнению с острыми формами заболевания. Развитие тромбоэмболий сосудов большого круга кровообращения является характерной клинической особенностью подострого ИЭ.
Положительный эффект от проводимой консервативной терапии наблюдается у большинства больных ИЭ с поражением ТК, тогда как при подостром эндокардите левых камер сердца консервативная терапия является малоэффективной у большинства больных.
Госпитальная летальность в обеих группах больных обусловлена диссеминацией возбудителя с формированием гнойных очагов и полиорганной недостаточностью, а также развитием острой недостаточности кровообращения и вторичной нефропатии.
Литература
В. И. Уланова
В. И. Мазуров, доктор медицинских наук, профессор
Медицинская академия последипломного образования, Санкт-Петербург