Лазерная абляция уретры что такое
Лазерная уретротомия стриктуры уретры (авторская методика)
При лазерной уретротомии стриктуры уретры проводится не только иссечение рубцово-суженного участка до границ с неизмененной слизистой, но и вапоризация рубцовой ткани. В отличие от традиционной уретротомии, при операции, проведенной по этой авторской методике, удается выполнить инцизию (рассечение) в разных направлениях с высокой точностью. При этом риск развития рецидива стриктуры в дальнейшем минимален. Кроме того, при проведении процедуры нет повреждения здоровых тканей, при этом кровотечение в ходе операции весьма незначительно, что обеспечивает возможность качественного визуального контроля.
Особенности методики
Оперативное вмешательство выполняется с использованием эндоскопического оборудования — уретроцистоскопа, который под видеоконтролем вводится в уретру к месту сужения. Показанием к проведению лазерной уретротомии являются короткие и средние стриктуры. При этом они могут быть как первичными, так и рецидивными, расположенными в переднем или заднем отделе, одиночными или множественными. При грубых стриктурах возможно сочетание лазерной и «холодной» уретротомии.
Процедура проводится под спинальной или сакральной анестезией. Ее длительность около 40-60 минут. Для лучшей регенерации или для создания покоя в области вмешательства проводится дренирование катетером в течение 5-7 дней. Безболезненность и короткий срок реабилитации — неоспоримые преимущества этой методики. Уже через 2 дня пациент может покинуть клинику, однако необходимо амбулаторное наблюдение. Самостоятельное мочеиспускание восстанавливается после извлечения уретрального катетера. Полное восстановление трудоспособности происходит, как правило, спустя 14 дней после проведения процедуры.
Заболевания
Стриктура уретры
Записывайтесь на консультацию: +7 (495) 782-50-10
Малоинвазивные методы лечения стриктур передней уретры
Введение
Стриктура уретры (СУ) у мужчин известна урологам давно и остается одним из самых часто встречающихся заболеваний в урологической практике. Представленный литературный обзор является отображением как современных взглядов, так и исторических фактов, по таким методикам ее лечения, как бужирование, внутренняя уретротомия и стентирование. Поиск литературы производили с использованием баз данных Medline, PubMed, Embase. Оценку данных осуществляли по шкале доказательств установленной Международной консультацией по урологическим заболеваниям (МКУЗ) в Оксфордском центре.
Самой простой и самой известной методикой лечения СУ является её бужирование (паллиативный метод) с использованием различных инструментов. Качественно новым подходом в лечении стриктурной болезни следует считать 1974 год, когда Sachse H. применил внутреннюю оптическую уретеротомию (ВОУТ) с рассечением зоны стриктуры [1]. Несмотря на то что открытая реконструкция считается радикальным методом лечения стриктуры, ВОУТ признали стандартом терапии в лечении передних стриктур уретры небольшой протяженности, потому что уретропластика требует опытности хирурга, обеспеченности операционной и предполагает более длительный послеоперационный период и реабилитацию пациента [2,3].
В ряде статей, начиная с 1990 года описывается множество удачно выполненных вмешательств с применением ВОУТ. При этом в технику рассечения стриктуры были внесены несколько модификаций, таких как использование лазера вместо уретротома и установку стента в передний отдел уретры. Но к существенным улучшениям результатов лечения СУ это не привело. В большей степени эффективность лечения была связана с оценкой критериев СУ, ее локализации и протяженности. Так же необходимо учитывать симптомы, показатели урофлоуметрии, данные уретрографии, наличие инфекции мочевых путей.
ВОУТ/дилатация стриктуры передних отделов уретры
Исследования показали, что в Америке 92,8% врачей-урологов, по одним источникам, и 85,6% ‒ по другим предпочитают использовать бужирование и/или рассечение стриктур в передних отделах уретры [4,5]. Такое предпочтение к ВОУТ/ бужированию связано с легкостью выполнения манипуляции, минимальными затратами, возможностью ее выполнения под местной анестезией в амбулаторных условиях, что не требует длительной реабилитации пациента [6,8].
Цель данной процедуры заключается в проведении минимально инвазивного вмешательства, призванного улучшить проходимость уретры с минимальными осложнениями [9]. Для тщательно отобранных пациентов с оптимальными характеристиками стриктуры (преимущественно стриктура бульбарного отдела, 4 cм уретропластику и пробную ВОУТ при длине стриктуры 2-4 см. Пациенты были исследованы на время возникновения рецидива болезни, и установление ПИС в течение 48 месяцев. Было установлено, что ранний рецидив ( 15% и 2) их следует относить к болезни.
Santucci R., Eisenberg L. пришли к выводам, что внутренняя уретротомия имеет более низкий показатель успеха, чем это ранее заявлялось. Они провели ретроспективное медицинское исследование на 134 пациентах, которым была выполнена внутренняя уретротомия с 1994 по 2009 годы. Были исключены 36 пациентов с комплексными стриктурами и 24, которые сами отказались от этого метода лечения. Показатели ПИС после 1-й, 2-й, 3-й, 4-й, 5-й внутренней уретротомии составили 8%, 6%, 9%, 0% и 0%, а средний период до развития рецидива ‒ 7, 9, 3, 20 и 8 месяцев [18]. Разные оценки эффективности и разные стандарты исследований по допустимости выполнения этих методик не всегда позволяют сравнить одни результаты с другими.
Повторная ВОУТ/ бужирование
У пациентов с общими характеристиками рецидива стриктуры (единичная, 6 месяцев), показывают, что эффективность выполнения повторной ВОУТ составляет 9%-53% (уровень 2-3) [10,17,18,21,22]. При большей длине, многофокусности поражения, дистальных пенильных стриктурах рассечение/бужирование обычно не выполняется [2,23]. ВОУТ не показана если рецидив заболевания возникает менее, чем через 3 месяца после выполнения 3-й по счету ВОУТ. Таким пациентам показана уретропластика [2,3,12,17,21].
Побочные эффекты ВОУТ
Наиболее частыми видами осложнений после ВОУТ являются геморрагия и образование перинеальной гематомы (в 20% случаев) [17]. По другим источникам, также встречаются отек (13%), образование ложных ходов (10%), ректальная перфорация, эпидидимоорхит, стеноз меатуса и недержание мочи (9%), гипертермия (3,6%), гематома (3,4%), бактериемия (2,7%), уросепсис (2,1%) и образование абсцессов (1,4%). Данные об ЭД обычно составляют от 2-10% [24], тем не менее Schneider T, et al. [25] провели исследования на 68 пациентах без ЭД перед операцией и выяснили, что после проведения ВОУТ только 1 пациент жаловался на ЭД в послеоперационном периоде.
Рентабельность
В некоторых исследованиях, затрагивающих проблему рентабельности показано, что проведение простой уретротомии при стриктурах передних отделов уретры имеет рентабельность в тех случаях, когда возможный успех можно прогнозировать в >35%-50% случаях. В противном случае первичная уретропластика выгоднее, чем повторная уретротомия. Wright et al. установил, что самый лучший вариант при коротких стриктурах в бульбарном отделе – это выполнение уретропластики, а не эндоскопическое вмешательство. При наличии длинной стриктуры, где прогнозируемый успех составляет
Лазерная уретротомия для восстановления просвета мочеиспускательного канала
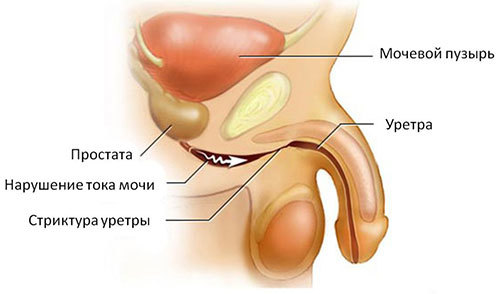
Стриктура уретры — патологическое состояние, при котором у мужчины резко сужается мочеиспускательный канал. Болезнь может возникнуть как нежелательное последствие операций на уретре, после травм или перенесенной инфекции. Рубцово-склеротический процесс нарушает нормальную структуру уретры и препятствует оттоку мочи. Опасность стриктуры состоит в том, что нарушается естественный процесс мочеиспускания, что в перспективе может грозить почечной недостаточностью.
Симптомами рубцового сужения просвета уретры могут быть:
Уретротомия — рассечение стриктур уретры. Операция проводится под эндоскопическим контролем при коротких стриктурах до 1 сантиметра. Оптическая уретротомия проводится с помощью «холодного ножа» или лазера. Рубцовая ткань, нарушающая структуру уретры, рассекается, а дальнейшее заживление происходит за счет эпителизации здоровых тканей. К сожалению, рецидивы встречаются достаточно часто. После операции пациенту устанавливают катетер, чтобы обеспечить полноценный отток мочи, срок катетеризации не превышает двух суток.
Также улучшить функцию мочеиспускательного канала помогает бужирование стриктуры уретры — процедура, которая помогает восстановить полноценный просвет органа. В полость уретры вводится инструмент в форме стержня, который расширяется и механически восстанавливает нормальную ширину мочеиспускательного канала.
Бужирование применяют при врожденных отклонениях в развитии, перенесенных инфекционных заболеваниях, рубцевании ткани, механических повреждениях мочеиспускательного канала.
Так как стриктура уретры — опасное состояние, которое может существенно ухудшать качество жизни и приводить к тяжелым последствиям для всей мочевыделительной системы, ее необходимо убирать. Для этого нужно обратиться к урологу, который сможет точно определить протяженность рубцовой ткани и предложит вариант лечения. Если вы столкнулись с урологическими патологиями, обратитесь в Клинику урологии имени Р. М. Фронштейна Первого Московского Государственного Медицинского Университета имени И.М. Сеченова (Государственный центр урологии), здесь могут провести лечение стриктуры уретры на самом высоком уровне.
Остались вопросы? Позвоните нам по телефону +7 (926) 242-12-12 или +7 (499) 409-12-45! В будний день прийти на консультацию к врачу возможно уже через несколько часов после заполнения онлайн-заявки. Не откладывайте посещение специалиста, если вас беспокоит здоровье мочеполовой сферы!
Критический обзор использования лазеров при доброкачественной гиперплазии предстательной железы (BPH)
Введение
Лазерная технология лечения свыше 15 лет используется для лечения симптомов со стороны нижних мочевыводящих путей, вторичных по отношению к BPH, и с самого начала ожидания в ее отношении были весьма высоки. От некоторых процедур лазерной терапии, появившихся на раннем этапе, пришлось отказаться вследствие необходимости продолжительной катетеризации, непредсказуемых результатов и высокого процента повторных операций. Однако успехи в сфере лазерной технологии, лучшее понимание взаимодействия тканей с лазером, технические усовершенствования (например, более высокие настройки мощности, конструктивные улучшения в сфере производства волокна) и рост клинической практики привели к возникновению техник и устройств, способных поставить под сомнение необходимость TURP.
В качестве альтернативы TURP внедрялись различные лазеры, в основном, это неодимовый лазер: на основе кристаллов иттрий-алюминиевого граната (Nd: YAG), гольмиевый лазер: YAG (Ho: YAG), лазер на основе кристаллов титанил-фосфата калия: YAG (KTP: YAG), тулиевый лазер (Tm) и диодный лазер. К техникам относятся коагуляция, вапоризация, резекция и энуклеация, в зависимости от длины волн, мощности и типа лазерного излучения (непрерывное или импульсное). Все эти различные методы лазерной терапии входят в общее понятие «лазерная эктомия предстательной железы». Однако этот термин может привести к неверному толкованию, так как доступные в настоящий момент лазеры и лазерные технологии имеют значительные различия в части обработки и взаимодействия между тканями и лазером.
Целью настоящей обзорной статьи является предоставление всей необходимой информации, способной помочь урологам научиться различать разные типы лазеров и критически оценивать роль разных лазерных методов лечения симптомов со стороны нижних мочевыводящих путей, обусловленных BPH, при использовании научно обоснованного подхода.
Методы
В базе MEDLINE был проведен электронный поиск за последние 15 лет с целью обнаружения публикаций на английском языке по теме лазерной терапии пациентов, страдающих BPH, с использованием ключевых слов: лазер, предстательная железа, BPH, гольмий, фотоселективная вапоризация предстательной железы (PVP), GreenLight KTP, триборат лития (LBO), тулий и диод. Мы также провели поиск в материалах (проведенных в течение 5 последних лет) конференций Европейской ассоциации урологии, AUA (Американской урологической ассоциации) и Эндоурологического общества. При использовании научно обоснованного подхода наш поиск был сконцентрирован на исследованиях высочайшего качества в отношении каждого варианта терапии, начиная от доступного мета-анализа и заканчивая рандомизированными клиническими исследованиями (RCT), а также крупными исследованиями отдельных случаев, поиск также базировался на систематическом анализе ранее опубликованных статей. Имеющиеся типы исследований также свидетельствуют о том, насколько экстенсивно исследовался каждый из методов эктомии предстательной железы.
Лазерная физика
Основные принципы
Акроним «LASER» (ЛАЗЕР) представляет собой сокращение от “Light Amplification by Stimulated Emission of Radiation – «усиление света посредством вынужденного излучения»). Лазер является источником коллимированного, монохроматического, когерентного света, излучаемого активизированным материалом лазера (полупроводником, кристаллом, газом или красителем). Ключевой определяющий фактор применения лазера основан на взаимодействии лазерного луча и целевой ткани, которое зависит от отражения, рассеивания и поглощения [1]. Поглощение является самым важным компонентом в процессе взаимодействия света и ткани и имеет определяющее значение для преобразования света в тепловую энергию. Преобразование лазерного луча в тепловую энергию приводит к повышению температуры целевой ткани и может вызвать либо коагуляцию, либо вапоризацию. Лазерная коагуляция происходит, когда ткань нагревается до температуры ниже температуры кипения/ температуры парообразования, однако выше температуры, необходимой для денатурации белка, в результате которой возникает коагуляционный некроз, с возможностью отсроченной морфологической циторедукции. Лазерная вапоризация происходит при выпаривании ткани посредством нагревания до температуры выше температуры кипения/ парообразования с использованием тепловой энергии лазерного луча повышенной плотности. Для достижения поглощения необходим хромофор, например, меланин (который не имеет большого значения для использования в урологии), оксигемоглобин и вода. При использовании лазерной эктомии предстательной железы, в целом, используемая энергия должна приводить к непосредственному удалению ткани. Следовательно, коэффициент поглощения представляет очень важную характеристику взаимодействия между длиной волны лазера и имеющимися хромофорами. Высокий коэффициент поглощения означает, что заданная длина волны лазера хорошо поглощается в выбранной среде. Низкий коэффициент поглощения соответствует более высокой степени прозрачности ткани, позволяющей свету глубже проникать в среду.
Еще одной ключевой характеристикой лазера является оптическая глубина проникновения в ткань для каждой отдельной длины волн. По этой причине было введено понятие длины затухания (определяемой как глубина, до которой 90% падающего на поверхность лазерного луча поглощается и преобразуется в тепло). Длина затухания является очень важной характеристикой, так как лазер с меньшей длиной будет передавать в ткань большее количество энергии на единицу площади. Это означает, что при одном и том же уровне мощности длина волны лазера с большей длиной затухания будет рассеивать переданную мощность и вызывать глубокий некроз, в то время как длина волны лазера с меньшей длиной затухания обеспечивает более концентрированную передачу энергии света, что приводит к повышению температуры до уровня выше температуры кипения/ парообразования и к непосредственной вапоризации ткани.
«Поглощение является самым важным компонентом процесса взаимодействия света и ткани»
Основные характеристики различных лазеров
| Тип лазера | Длина волны, нм | Хромофор | Глубина проникновения, мм | Режим | Применение |
| Nd: YAG | 1064 | вода и гемоглобин | 10 | импульсный или непрерывный | коагуляция |
| Ho: YAG | 2100 | вода | 0,4 | импульсный | вапоризация, резекция, энуклеация |
| KTP (LBO) | 532 | гемоглобин | 0,8 | псевдонепрерывный | вапоризация |
| Tm | 2000 | вода | 0,25 | непрерывный | вапоризация, резекция, энуклеация |
| Диодный | 940 980 1470 | вода и гемоглобин | различная | импульсный или непрерывный | вапоризация |
Современные техники лазерной терапии
Основными категориями техник лазерной терапии являются коагуляция, вапоризация, резекция и энуклеация. Исходя из вышеописанных данных, не удивительно, что не все лазеры можно использовать для всех техник лазерной терапии.
(1) Коагуляция
Исходное применение лазера Nd: YAG для лечения BPH сопровождалось огромным энтузиазмом. Однако в соответствии с полученными клиническими результатами оказалось, что лазеры Nd: YAG не способны немедленно удалять ткани. Лазеры, использующие длину волн, подобную Nd: YAG, приводили к глубокому коагуляционному некрозу с отсроченным (4-8 недель) отторжением некротических масс и вторичной абляцией закупоривающей ткани. Ткани для гистологического анализа не предоставлялись.
Еще одним фактором, ограничивающим использование VLAP и ILC, стал зафиксированный процент повторных операций 7,5 – 20% и 0 – 15,4% через 12 месяцев после первоначальной операции соответственно. Через 24 месяца после VLAP процент повторных операций достиг 26,7% [7]. В ходе исследования с более продолжительным периодом последующего наблюдения (в среднем 54 месяца, диапазон: 46 – 61 месяц) было установлено, что повторная операция потребовалась половине пациентов, которые подвергались ILC [8]. По причине неприемлемых нежелательных явлений, высокого процента повторных операций и появления более эффективных и технически усовершенствованных систем лазерной терапии методы VLAP и ILC перестали использоваться.
(2) Бесконтактная лазерная абляция или вапоризация
Это наиболее современная техника лазерной терапии, для бесконтактной абляции и вапоризации предстательной железы можно использовать все типы лазеров. В последнее время по причине технических преимуществ и повышенного коэффициента полезного действия «абляция» все больше переходит в «вапоризацию», так как вапоризация обеспечивает немедленное видимое удаление ткани во время операции.
Лазерный луч при помощи оголенного волокна направляется прямо или сбоку на ткань предстательной железы с использованием волокна бокового действия. Обычно во всей предстательной железе создается канал выпариваемой ткани. Ткань для гистологического исследования не предоставляется.
Абляция предстательной железы при помощи Но-лазера (HoLAP)
Первые сообщения о HoLAP датируются 1994 г., когда HoLAP была выполнена с использованием Ho-лазера мощностью 60 Вт. Интерес к чистой HoLAP пропал с развитием техник гольмиевой резекции и энуклеации. Однако интерес к HoLAP возродился после появления высокомощного Ho-лазера мощностью100 Вт, но данных все еще недостаточно.
Эффективность и частота осложнений: Сравнение HoLAP с TURP было выполнено в ходе лишь одного небольшого исследования RCT, в результате которого были получены сравнимые результаты в части облегчения симптомов по Международной шкале оценки симптомов заболеваний предстательной железы и показателя Qmax для 2 групп пациентов, участвовавших в исследовании, в ходе последующего наблюдения [9]. Время катетеризации и госпитализации было короче для пациентов, перенесших HoLAP. Кумар [10] сообщил предварительные результаты при использовании Ho-лазера мощностью 100 Вт для лечения пациентов с большим объемом предстательной железы (> 80 мл). Была продемонстрирована краткосрочная эффективность в части облегчения симптомов, оцениваемых по шкале оценки симптомов AUA (SS) и положительного изменения параметра Qmax, а также незначительная потеря крови, отсутствие недержания мочи при напряжении, а также непродолжительный период катетеризации и госпитализации. Недавно Эльзаят и др. [11] провели RCT, сравнивающее HoLAP (80 – 100 Вт) и PVP (80 Вт) предстательной железы. Функциональным результатом стало значительное облегчение симптомов и сравнимые результаты через 12 месяцев после операции. Более того, не было зафиксировано значительных различий в частоте возникновения осложнений между двумя процедурами, PVP выигрывает только по времени операции. В таблице 2 11 представлены клинические данные по HoLAP.
Стойкость результата: Тан и др. [17] зафиксировали стойкость результата для 34 пациентов при среднем периоде последующего наблюдения 7,4 года. Субъективные и объективные переменные опорожнения подтвердили стойкость результата: 47% сокращения в части AUA-SS и 83% увеличения в части Qmax в сравнении с данными показателями на момент начла исследования. Процент повторных операций составил 15% через 7 лет.
(3) Резекция или вапорезекция
Лазерная резекция представляет собой лазерную версию TURP и может выполняться как с использованием Ho-лазера, таки с использованием Tm-лазера. В данной технике используется волокно с продольным направлением излучения для выполнения двусторонних разрезов шейки мочевого пузыря, после чего средняя доля предстательной железы иссекается в виде многочисленных мелких кусочков предстательной железы, которые впоследствии вымываются из мочевого пузыря.
Имеются ткани для гистологического исследования.
Резекция предстательной железы при помощи Но-лазера (HoLRP)
HoLRP стала первым способом применения лазерной энергии для эксцизионной хирургии предстательной железы, она была внедрена в 1994 г. С момента внедрения устройства для кускования тканей HoLRP во многих случаях заменяется техникой энуклеации (HoLEP). В результате этого за последнее время по HoLRP не проводились исследования RCT, а также крупные исследования случаев из клинической практики. Эта техника остается релевантной для повторных операций и резекций «канала» в случае рака предстательной железы на поздней стадии.
Стойкость результата: В результате исследования с самым продолжительным периодом последующего наблюдения (4 года) было продемонстрировано, что HoLRP обеспечивает стойкость результата в части положительного изменения симптомов Qmax и QOL, эти показатели стойкости результата были сопоставимы показателями для TURP [42]. Кроме того, разницы по проценту повторных операций между двумя группами также не было зафиксировано.
(4) Энуклеация
«Лазерная энуклеация представляет собой эндоскопический эквивалент простой OP
Лазерная энуклеация представляет собой эндоскопический эквивалент простой OP и является наиболее прогрессивной формой лазерной хирургии предстательной железы. Ho-лазер был первоначальным источником энергии, применяемым во время процедуры, при использовании волокна без покрытия для контактной лазерной терапии для вхождения в плоскость хирургического вмешательства между аденомой предстательной железы и капсулой, а затем для выделения каждой доли предстательной железы из капсулы. Для удаления тканей, которые затем можно будет использовать для гистологического исследования, необходимо устройство для кускования тканей. В результате последних исследований поступили сообщения об использовании Tm-лазера для энуклеации предстательной железы.
HoLEP
Эффективность и безопасность применения HoLEP была продемонстрирована многочисленными исследованиями. Имеющиеся результаты системных анализов и мета-анализов сделали HoLEP наиболее изученной техникой лазерной терапии на настоящий момент.
Эффективность и частота осложнений: На основании системного анализа двух RCT и одного не рандомизированного контролируемого исследования был сделан вывод о том, что HoLEP имеет, по крайней мере, равную эффективность с TURP в части облегчения симптомов BPH [37]. Джиллинг и др. [44] выполнили первый мета-анализ четырех RCT, сравнивающих HoLEP и TURP. Они установили, что уродинамическое облегчение закупорки (давление детрузора при Qmax и степени Шеффера) было более значительным при HoLEP в сравнении с TURP, но только для объема предстательной железы 5 лет) продемонстрировали, что субъективное и объективное облегчение симптомов было стойким, в то время как процент повторной операции варьировался в диапазоне от 1,4% до 4,3% [56, 57].
Сравнение различных лазеров
Вследствие отсутствия прямых сравнительных исследований, а также вследствие того, что разные лазеры находятся на разных стадиях клинической разработки, их сравнение произвести достаточно сложно. Наиболее изученными опциями лазерной терапии являются HoLEP и PVP, которые в настоящий момент доминируют в сфере применения лазерных технология для лечения симптомов со стороны нижних мочевыводящих путей, связанных с BPH. Поэтому основное внимание при сравнении мы уделили HoLEP и PVP. Так как эффективность и частота возникновения осложнений были достаточно подробно рассмотрены выше, сферами непрямого сравнения будут являться особые подгруппы пациентов, кривая обучения и затраты.
Особые состояния
Пациенты, получающие антикоагулянтную терапию, с сопутствующими заболеваниями
Исследования GreenLight PV показали, что, по всей вероятности, данная процедура является безопасной и благоприятной для пациентов группы повышенного риска. В ходе исследования было оценено 66 пациентов с показателем по шкале ASA ≥ 3, при этом 26 из них продолжали получать антикоагулянтную терапию (OAT), а три пациента страдали тяжелым нарушением свертываемости крови [60]. Переливание крови не потребовалось ни в одном из случаев. Результаты эффективности продемонстрировали стойкое положительное изменение показателей Qmax и IPSS. Сандху и др. [61] сообщили результаты исследования использования лазера GreenLight мощностью 80 Вт для 24 пациентов, получавших различные формы OAT, включая варфарин (восемь пациентов) и ингибиторы агрегации тромбоцитов (PAI). Пациенты, принимавшие варфарин, прекратили прием препарата за 2 дня до операции и возобновили его через день после операции. В целом, вапоризация предстательной железы для всех пациентов прошла безопасно, без АЕ тромбоэмболии или кровотечения. Русзат и др. [62] оценили безопасность использования GreenLight PV в ходе самого крупного исследования случаев с участием пациентов, страдающих серьезными сопутствующими заболеваниями и принимающих кумадин или PAI. Осложнений в виде тромбоэмболии или кровотечения зафиксировано не было, необходимости в переливании крови не возникало, только процент преходящего промывания мочевого пузыря был значительно выше у пациентов, получавших ОАТ (17,2%), в сравнении с контрольной группой пациентов, подвергнувшихся GreenLight PV, которые не принимали антикоагулянты (5,4%) [62].
«Для оценки энуклеации с использованием лазера Tm:YAG необходимо больше исследований, включая RCT
Недавно предоставленные данные касательно использования GreenLight HPS также продемонстрировали значительное положительное изменение симптомов, как для пациентов получающих ОАТ, так и для пациентов, не получающих ОАТ [19]. Процент осложнений после операции был низким и сравнимым с контрольной группой, при этом переливание крови не потребовалось ни одной из групп [26].
Подобным образом, процедура HoLEP была успешно выполнена в отношении пациентов, которые обычно считаются несоответствующими установленным параметрам для TURP, в том числе пациентов с серьезными сопутствующими заболеваниями, такими как коагулопатия, антикоагулянтная зависимость и серьезная анемия [63]. Переливание крови потребовалось семи пациентам (8%), включая одного пациента, прекратившего прием ОАТ, пять пациентов, получавших замещающую терапию гепаринами с низкой молекулярной массой, и одного пациента, получавшего полную антикоагулянтную терапию. Кроме того, одному пациенту, прекратившему прием клопидогрела, потребовалась трансфузия тромбоцитов. В ходе еще одного исследования сравнивались результаты HoLEP для 39 пациентов, получавших OAT (13 кумадин и 25 аспирин) в момент хирургического вмешательства, и 37 пациентов контрольной группы [64]. Ни одному из 76 пациентов переливание крови не потребовалось, статистически значимых различий в части осложнения в виде кровотечения между пациентами, принимавшими кумадин, аспирин, и пациентами контрольной группы не зафиксировано.
В результате исключительного анализа лазерной терапии в отношении пациентов, получающих ОАТ, было сделано заключение о том, что лазерная эктомия предстательной железы, по всей видимости, снижает риск возникновения кровотечения у пациентов, принимающих PAI или производные кумарина [65]
Пациенты с задержкой
Исторически пациентов с задержкой ассоциируют с более высоким процентом осложнений, а иногда и с худшим исходом в части параметров опорожнения.
Было проведено исследование, сравнивающее исход для 70 пациентов с не поддающейся лечению задержкой и 113 пациентов, не страдающих задержкой [66]. Все пациенты в группе с задержкой через 1 месяц после терапии лазером GreenLight мощностью 80 Вт могли самопроизвольно опорожнять мочевой пузырь, также было отмечено значительное снижение параметра PVR: на 74,8% при выписке и на 82,7% через 12 месяцев после операции. В целом, функциональные результаты и осложнения во время операции были схожи для двух групп на протяжении всего 24-месячного периода наблюдения. Группа IGLU установила, что для группы пациентов, страдающих задержкой, подвергнувшихся терапии лазером мощностью 120 Вт, и для контрольной группы функциональные результаты были схожими, за исключением параметра Qmax, в то время как наиболее распространенным осложнением была дизурия (11,1%) и преходящая задержка, требующая повторной катетеризации (4,8 %) [19].
В результате исследования с участием пациентов, страдающих задержкой мочеиспускания, была подтверждена краткосрочная эффективность HoLEP. В результате исследования с участием 169 только трое из них (1,8%) не могли самопроизвольно опорожнять мочевой пузырь после лечения [67]. Продолжительность катетеризации и госпитализации (1,6 дней и 1,7 дней соответственно) были сравнимы с данными показателями для пациентов, не страдающих задержкой. Петерсон и др. [68] выполнили подобное исследование с участием 154 пациентов, страдающих задержкой. После операции все пациенты могли самопроизвольно опорожнять мочевой пузырь и им не требовалась повторная катетеризация в течение периода последующего наблюдения до 1 года после операции, хотя через 1 год после операции оценить удалось только 22% пациентов, изначально включенных в исследование. Среднее время катетеризации и госпитализации составило 22,5 ч и 33,7 ч соответственно.
Все эти исследования сообщают о краткосрочных результатах, следует подчеркнуть, что долгосрочные результаты для данной группы пациентов весьма ограничены.
Затраты
При сравнении всех стратегий лечения с однократной TURP в качестве общего сравнительного показателя оказалось, что HoLEP более рентабельна, чем однократная TURP, однако менее эффективна, чем стратегия, предполагающая повторную TURP в случае необходимости. С другой стороны, GreenLight PV менее эффективна и более затратна, чем TURP. В результате исследователи пришли к выводу, что TURP продолжает оставаться клинически эффективной и рентабельной.
Однако рентабельность всех техник зависит от наличия долгосрочных данных, затрат на устранение осложнений, различных систем оплаты в разных странах. Поэтому нельзя сделать однозначный вывод, применимый в отношении всех стран.
Заключение
Во время последнего десятилетия лазерная терапия быстро развивалась, от коагуляции до вапоризации, резекции и энуклеации. В свете этого развития от техник коагуляции (т.е., ILC и VLAP) полностью отказались, в то время как HoLAP и HoLRP стали предшественниками многих техник, применимых в настоящий момент (таких как фотоселективная вапоризация, техники с использованием диодных лазеров, вапорезекция с использованием Tm-лазера), но они пострадали от развития HoLEP. Краткосрочная эффективность появляющихся методов лазерной терапии (включая эктомию предстательной железы с использованием диодного лазера и Tm-лазера) базируется на результатах исследований низкого качества.
В настоящее время необходимость TURP более, чем когда-либо, поставлена под сомнение HoLEP и GreenLight PV, которые представляют собой действительную клиническую альтернативу TURP. Имеющиеся в настоящий момент доказательства подкрепляют вывод о том, что HoLEP обеспечивает благоприятный и стойкий эффект при лечении предстательной железы любого размера при низком проценте осложнений на ранней и поздней стадии. Эктомия предстательной железы с использованием лазера GreenLight получила высокое признание, несмотря на отсутствие долгосрочных результатов исследований высокого качества.