гипокинезия миокарда что это такое
Ишемическая кардиомиопатия (I25.5)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Ишемическая кардиомиопатия (ИКМП) — патологическое состояние миокарда, обусловленное комплексом диффузных морфофункциональных нарушений, развивающихся в результате хронической и эпизодов острой ишемии миокарда, основными проявлениями которого являются дилатация камер сердца и симптомокомплекс хронической сердечной недостаточности (ХСН).
Этиология и патогенез
В развитии заболевания участвуют факторы, играющие важную роль в патогенезе ХСН: дисбаланс в продукции эндотелием вазоконстрикторов и вазодилататоров с недостаточным синтезом последних, активация нейрогормональных факторов, гиперпродукция цитокинов, фактора некроза опухоли.
Эпидемиология
Признак распространенности: Редко
Больные ишемической дилатационной кардиомиопатией составляют около 5–8 % общего количества пациентов, страдающих клинически выражеными формами ИБС, а среди всех случаев кардиомиопатий на долю ишемической дилатационной кардиомиопатий приходится около 11–13 %.
Ишемическая кардиомиопатия встречается преимущественно возрасте 45–55 лет, среди всех больных мужчины составляют 90 %
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
В типичных случаях клиническая картина характеризуется триадой симптомов: стенокардией напряжения, кардиомегалией, ХСН. У многих больных отсутствют клинические и ЭКГ-признаков стенокардии.
Клиническая симптоматика ХСН не имеет каких-либо специфических особенностей и в основном идентична проявлениям СН у больных с идиопатической дилатационной кардиомиопатией. Сердечная недостаточность быстрее прогрессирует при ишемической кардиомиопатии по сравнению с дилатационной кардиомиопатией. Обычно речь идет о систолической форме СН, но возможно развитие диастолической СН или сочетания обеих форм.
Кардиомегалия при физикальном исследовании характеризуется расширением всех границ сердца и преимущественно левой. При аускультации обращают на себя внимание тахикардия, часто различные аритмии, глухость тонов сердца, протодиастолический ритм галопа. Аритмия обнаруживается при ишемической кардиомиопатии значительно реже (17%), чем при идиопатической дилатационной кардиомиопатии. Признаки тромбоэмболических осложнений в клинической картине ишемической кардиомиопатии наблюдаются несколько реже, чем при идиопатической дилатационной кардиомиопатии.
Диагностика
Диагностические критерии ишемической дилатационной кардиомиопатии
| Диагностические критерии | Примечания к критериям |
| 1. Наличие стенокардии в настоящее время или в прошлом, или перенесенного инфаркта миокарда, которые предшествуют развитию хронической сердечной недостаточности | Критерий подтверждается ЭКГ, ЭхоКГ. Стенокардия или перенесенный инфаркт миокарда не всегда предшествуют развитию ХСН, возможно наличие безболевой ишемии задолго до появления клиники ишемической кардиомиопатии. Иногда предшествовавшие приступы стенокардии исчезают или ослабевают |
| 2. Кардиомегалия | Определяется при перкуссии сердца, но должна быть верифицирована с помощью эхокардиографии |
| 3. Наличие клинических и эхокардиографических признаков сердечной недостаточности (уменьшение фракции выброса, увеличение конечного диастолического объема и давления, диффузная гипокинезия миокарда) | При выраженной застойной сердечной недостаточности обычно имеется комбинированная систолическая сердечная недостаточность (ФВ левого желудочка) и диастолическая дисфункция левого желудочка (доплер-эхографические признаки нарушения диастолического наполнения левого желудочка) |
| 4. Обнаружение в миокарде участков, находящихся в состоянии гибернации | Используются методы: стресс-эхокардиография с добутамином, позитронно-эмиссионная томография с фтор-флуородезоксиглюкозой; сцинтиграфия миокарда с 100Т1 и 221Тс и сравнением участков нарушения накопления изотопа с участками асинергии, выявленными при эхокардиографии |
| 5. Обнаружение при коронароангиографии выраженного атеросклеротического процесса с сужением просвета одной из главных | |
| 6. Отсутствие аневризмы желудочков и органической патологии клапанного аппарата, других причин кардиомегалии |
Электрокардиография
Могут выявляться рубцовые изменения после перенесенных ранее инфарктов миокарда или признаки ишемии в виде горизонтального смещения книзу от изолинии интервала ST в различных отделах миокарда. У многих больных обнаруживаются неспецифические диффузные изменения в миокарде в виде снижения или сглаженности зубца Т. Иногда зубец Т бывает отрицательным несимметричным или симметричным. Характерны также признаки гипертрофии миокарда левого желудочка или других отделов сердца. Регистрируются различные аритмии (чаще экстрасистолия, мерцательная аритмия) или нарушения проводимости. Суточное мониторирование ЭКГ по Холтеру часто выявляет скрыто протекающую, безболевую ишемию миокарда.
Эхокардиография
При ЭхоКГ обнаруживаются дилатация полостей сердца, небольшая гипертрофия миокарда, увеличение конечного диастолического объема, диффузная гипокинезия стенок левого желудочка, снижение фракции выброса. Фракция выброса правого желудочка у больных ишемической кардиопатией по сравнению с фракцией выброса левого желудочка снижена в меньшей мере, чем при идиопатической дилатационной кардиомиопатии.
При ишемической кардиомиопатии возможно развитие диастолической дисфункции, рестриктивный тип наблюдается значительно реже. При развитии изолированной диастолической СН систолическая функция левого желудочка сохранена, фракция выброса нормальная. При ишемической кардиомиопатии изолированная диастолическая недостаточность бывает редко, чаще при выраженной застойной СН речь идет о комбинированной систолической и диастолической дисфункции левого желудочка.
Рентгенологическое исследование
Определяет значительное увеличение размеров всех камер сердца.
Радиоизотопная сцинтиграфия
Выявляет мелкие очаги нарушения накопления таллия-201 в миокарде, что отражает ишемию и фиброз миокарда.
Коронароангиография
Обнаруживает значительно выраженное атеросклеротическое поражение коронарных артерий. При этом одна из артерий может быть сужена более чем на 50%.
Субэндомиокардиальная биопсия Дистрофические изменения кардиомиоцитов вплоть до некроза, интерстициальный фиброз, заместительный склероз, иногда небольшие лимфогистиоцитарные инфильтраты
Лабораторная диагностика
Биохимический анализ крови
Характерно повышение содержания в крови общего холестерина, холестерина липопротеинов низкой плотности, триглицеридов, что характерно для атеросклероза.
Дифференциальный диагноз
Дифференцировать ишемическую кардиомиопатию необходимо с различными видами дилатационной кардиомиопатии, в первую очередь, с идиопатической дилатационной и алкогольной кардиомиопатией, а также с заболеваниями, сопровождающимися синдромом кардиомегалии.
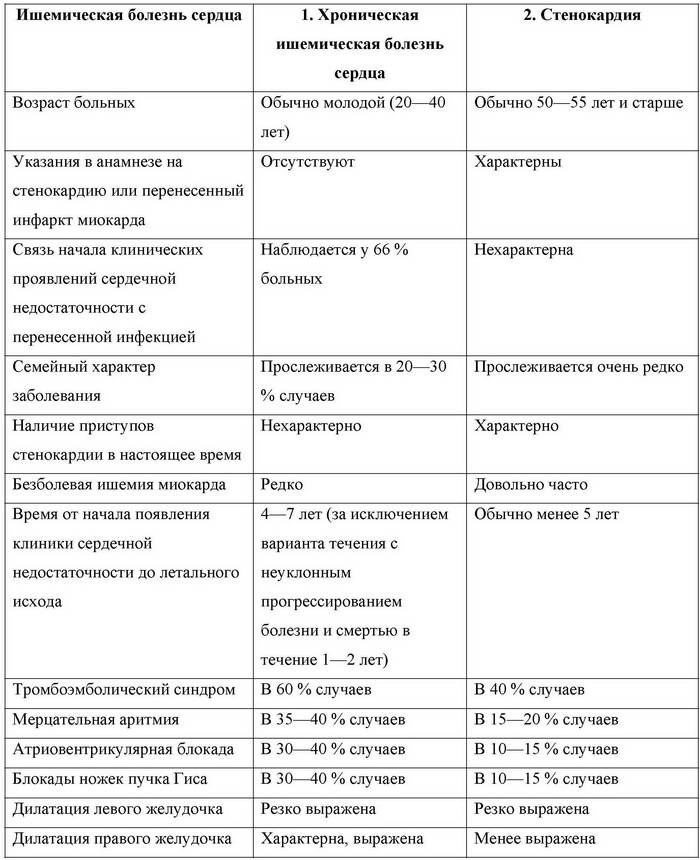
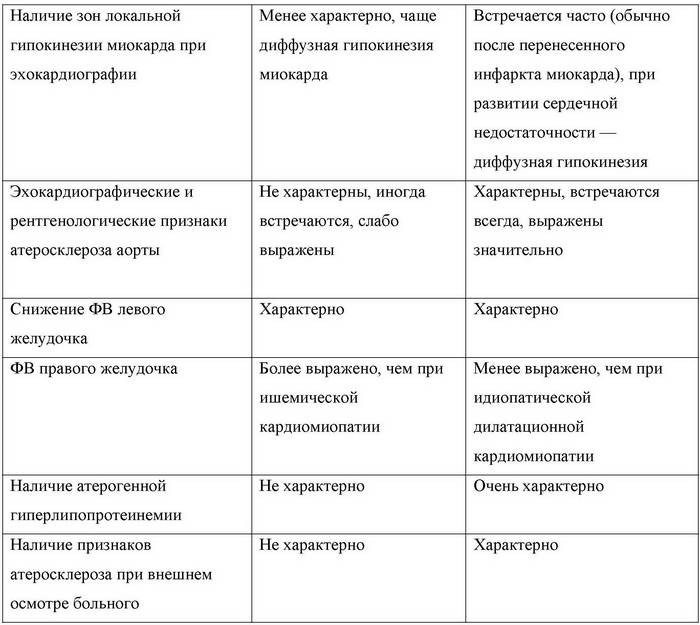
Дифференциально-диагностические различия между идиопатической и ишемической дилатационной кардиомиопатией.
Осложнения
Лечение
При переносимости и отсутствии противопоказаний типичная медикаментозная терапия включает в себя β-адреноблокаторы (в основном, карведилол), иАПФ (или БРА). Спиронолактон также следует назначать пациентам с уровнем креатинина ‹2,5 мг/дл и калия в сыворотке крови ‹5,5 ммол/л. Фуросемид или тиазидные диуретики показаны пациентам с симптомами и/или признаки застоя, в то время как дигоксин может назначаться в случае тахисистолической формы мерцательной аритмии. Когда требуется назначение антиаритмической терапии, необходимой при наджелудочковой или желудочковой тахиаритмии, препаратом выбора является амиодарон. Больным с фибрилляцией либо трепетанием предсердий или наличием в анамнезе внутрисердечного тромба следует добавить терапию антикоагулянтами для приема внутрь.
Возможность того, что регенерация миокарда при помощи клеточной терапии может улучшить функцию ЛЖ и прогноз у таких больных, является большой надеждой как пациентов, так и врачей, но пока эти формы лечения показали разочаровывающие результаты и, следовательно, требуют дальнейшего усовершенствования и оценки до того, как они смогут появиться в клинической практике.
Симптомы и лечение диффузного миокардита
Симптомы и лечение диффузного миокардита
Симптомный и бессимптомный, этиологический и идиопатический миокардит называют диффузным при поражении значительной области мышцы. Если это неидиопатический миокардит, то платформой для его развития может стать (это важно для распознавания и лечения диффузного воспаления) бактерия, грибок, вирус, инфекция.
Из-за обширного (или диффузного) поражения и клиники, часто смежной с симптоматикой ОРВИ / ОРЗ миокардит этого вида называют «простудой сердца». С точки зрения проявлений диффузного воспаления, это обосновано. Примерно 2/3 сигналов миокардита схожи с признаками гриппа, особенно в острой, подострой фазе.
От простуды диффузный миокардит отличают признаки нарушения проводимости сердца и дистрофические процессы. К ним относят такие симптомы диффузной формы, как одышка (в том числе, постопноэ – дефицит воздуха в горизонтальном положении), чувство замирания, остановки, стягивания сердца в тиски, болезненность в загрудинном пространстве и груди.
ИДЕНТИФИКАЦИЯ ОБШИРНОГО ВОСПАЛЕНИЯ МЫШЦЫ-МИОКАРДА
Распознавание диффузного воспаления (миокардита) начинается с отмежевания данной патологии от дистрофии миокарда. Оба заболевания схожи по клиническому описанию, но на электрокардиограмме их легко отличить.
Помимо ЭКГ при диффузном миокардите обязательно проводят исследование ультразвуком. Это база диагностики миокардита.
УЗИ покажет не только факт наличия патологии, но и:
Обычно для идентификации диффузного воспаления достаточно УЗИ, ЭКГ (иногда с ЭхоКГ) и рентгена груди. Последний нужен, чтобы просмотреть состояние каждого поврежденного миокардитом участка.
Из прочих манипуляций – стандартный набор:
ПРОГНОЗ, ОСЛОЖНЕНИЯ, ЛЕЧЕНИЕ И ПРЕДУПРЕЖДЕНИЕ РЕЦИДИВА
Прогноз при системном (диффузном) миокардите более чем в 50% случаев благоприятный. Особенно если миокардит себя обнаружил на (под)острой стадии. Исключение – диффузный идиопатический миокардит, который часто сопровождается осложнениями.
К последним могут относиться:
Самым распространенным осложнением миокардита остается СД.
Сколько времени займет лечение?
Схема лечения миокардита включает три обязательных пункта.
При идиопатическом остром и подостром диффузном миокардите часто рекомендуют к приему антибиотики, антигистамины и НПВС. Стационар (строгий режим гиподинамии, мониторинг гемодинамики, витаминизация) займет до месяца. Полное выздоровление – через год (или дольше).
Поскольку диффузная форма характеризуется крайне тяжелым протеканием миокардита, в течение минимум года после ремиссии человек остается на учете в кардиологии. На санитарно-курортное лечение можно отправляться не раньше чем через 10-12 месяцев.
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений и постепенно прогрессирующим течением с высоким риском развития жизнеугрожающих аритмий и внезапной смерти.
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов.
При ГКМП происходит массивная гипертрофия миокарда левого (и реже правого желудочка), чаще асимметричного характера за счет утолщения межжелудочковой перегородки, часто с развитием обструкции выходного тракта левого желудочка (ЛЖ) при отсутствии каких-либо явных причин.
Общепризнанной является представление о преимущественно наследственной природе ГКМП. В связи с этим, широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми, при этом основной тип наследования – аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
Гипертрофическая кардиомиопатия – это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений.
Возможны три гемодинамических варианта обструктивной ГКМП:
Cимптомы болезни разнообразны и малоспецифичны, связаны с гемодинамическими нарушениями (диастолическая дисфункция, динамическая обструкция путей оттока, митральная регургитация), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце. Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся медикаментозному лечению форм, сопровождающихся тяжелой симптоматикой.
Повышение диастолического давления в левом желудочке из-за диастолической дисфункции, динамическая обструкция выносящего тракта левого желудочка проявляются одышкой в покое и при физической нагрузке, утомляемости, слабости. Нарастание давления в малом круге кровообращения сопровождается развитием острой левожелудочковой недостаточности (чаще в ночные часы – сердечная астма, альвеолярный отек легких).
Падение фракции выброса при физической нагрузке или нарушениях сердечного ритма сопровождается ухудшением кровообращения головного мозга. Преходящая ишемия мозговых структур проявляется кратковременной потерей сознания (обморок) или предобморочными состояниями (внезапная слабость, головокружение, потемнение в глазах, шум и «заложенность» в ушах).
Методы исследования:
ЭХО-КГ – основной метод диагностики ГКМП. Критериями диагностики ГКМП на основании данных ЭХО-КГ являются:
Если в покое обструкции выносящего тракта левого желудочка нет, ее можно спровоцировать медикаментозными (ингаляция амилнитрита, введение изопреналина, добутамина) или функциональными пробами (проба Вальсальвы, физическая нагрузка), которые уменьшают преднагрузку или повышают сократимость левого желудочка.
Катетеризация сердца и коронарная ангиография проводятся для оценки коронарного русла перед миоэктомией или операцией на митральном клапане, а также чтобы выяснить причину ишемии миокарда. При этом к характерным признакам ГКМП относят:
Сцинтиграфия миокарда и позитронно-эмиссионная томография
При гипертрофической кардиомиопатии сцинтиграфия миокарда имеет некоторые особенности, однако в целом ее значение в диагностике ишемии такое же, как и обычно. Стойкие дефекты накопления указывают на рубцовые изменения после инфаркта миокарда, обычно они сопровождаются снижением функции левого желудочка и плохой переносимостью физической нагрузки. Обратимые дефекты накопления указывают на ишемию, вызванную снижением коронарного резерва при нормальных артериях или коронарным атеросклерозом. Обратимые дефекты часто никак не проявляются, однако, по-видимому, они повышают риск внезапной смерти, особенно у молодых больных с гипертрофической кардиомиопатией. При изотопной вентрикулографии можно выявить замедленное наполнение левого желудочка и удлинение периода изоволюмического расслабления.
Позитронно-эмиссионная томография – более чувствительный метод, кроме того, она позволяет учесть и устранить помехи, связанные с затуханием сигнала. Позитронно-эмиссионная томография с фтордезоксиглюкозой подтверждает наличие субэндокарлиальной ишемии, вызванной снижением коронарного резерва.
Современные подходы к лечению ГКМП
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза.
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск внезапной смерти (в частности, скрытых, прогностически значимых аритмий).
Общие мероприятия
Ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска внезапной смерти.
Медикаментозное лечение
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью внезапной смерти. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов. Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид (антиаритмический препарат IA класса) и амиодарон.
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
Инвазивные методы лечения:
1. Чрезаортальная септальная миэктомия
2. Вальвулопластики или протезирования митрального клапана
В ряде случаев при наличии дополнительных показаний для уменьшения выраженности обструкции и митральной регургитации одномоментно выполняется операция вальвулопластики или протезирования митрального клапана низкопрофильным протезом. Улучшить отдаленные результаты миэктомии позволяет последующая длительная терапия верапамилом, обеспечивающая улучшение диастолической функции ЛЖ, что не достигается при хирургическом лечении.
3. Иссечения межжелудочковой перегородки
В настоящее время разработаны и успешно применяются отличные от классической миэктомии методики. В частности, в НЦССХ им. А. Н. Бакулева под руководством академика Л. А. Бокерия разработана оригинальная методика иссечения зоны гипертрофированной МЖП из конусной части правого желудочка. Этот способ хирургической коррекции обструктивной ГКМП является высокоэффективным и может стать методом выбора в случаях одновременной обструкции выходных отделов обоих желудочков, а также в случаях среднежелудочковой обструкции ЛЖ.
4. Транскатетерная септальная аблация
Другим альтернативным методом лечения рефракторной обструктивной ГКМП является транскатетерная алкогольная септальная аблация. Методика предполагает инфузию через баллонный катетер в перфорантную септальную ветвь 1–3 мл 95% спирта, вследствие чего возникает инфаркт гипертрофированного отдела МЖП, захватывающей от 3 до 10% массы миокарда ЛЖ (до 20% массы МЖП). Это приводит к значимому уменьшению выраженности обструкции выходного тракта и митральной недостаточности, объективной и субъективной симптоматике заболевания.
В Волынской больнице отработана методика выполнения транскатетерной септальной аблации при ГКМП. Доказан положительный результат данного вмешательства при относительно низком риске развития осложнений.
Миокардит в повседневной практике врача ( 2 часть)
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
– Далее – инфекционные заболевания, поскольку нам необходимо было исключить инфекционный миокардит. Вы видите, что индикаторы вирусных инфекций (хламидии, уреаплазмы, трихомонады, микоплазмы, вирусы простого герпеса, бруцеллы и так далее) практически были отрицательны. То же самое в отношении цитомегаловируса. Неоднократно забиралась кровь на бактериальную культуру (посев) – и ни разу положительная культура выявлена не была. Следовательно, инфекционная природа патологии сердца также нами была отвергнута.
Эта возможность чрезмерной чувствительности к тем или иным препаратам иногда наблюдается у пациентов с теми или иными генетическими полиморфизмами регуляторных механизмов. В этом отношении мы провели генетические исследования и выявили, что наша пациентка оказалась гетерозиготной в отношении ангиотензин-превращающего фермента. Также она оказалась гетерозиготной по отношению к рецептору первого типа – ангиотензину II.
Но при том, что она гетерозиготна, по существу, не повлияло на наличие уровня ангиотензин-превращающего фермента. Он оказался в пределах нормы. Поэтому эта гетерозиготность по ангиотензин-превращающему ферменту и по рецептору ангиотензина первого типа к ангиотензину II, по существу, остается за скобками. Мы не можем в той или иной форме привязать эти данные к тем клиническим наблюдениям, которые мы имеем применительно к этой пациентке. Возможно, в перспективе мы сможем ответить на этот вопрос.
Вот электрокардиограмма 2010-го года. Мы не видим здесь электрической альтернации. Но обращает на себя внимание очень выраженное повышение электрической активности левых и правых отделов сердца. Блокада правой ножки. Но, что важно: по прошествии столь длительного времени сохраняется подъем сегмента ST в грудных отведениях V3, V4, V5. Этот подъем сегмента ST заставляет нас продолжать проводить дифференциальный диагноз у нашей пациентки, что вызывает у нее столь выраженную сердечную декомпенсацию.
На левом снимке – рентгенограмма грудной клетки 2008-го года. На правом – рентгенограмма 2010-го года. Вы видите некоторые отличия. Уменьшилось содержание жидкости в плевральных полостях. Несколько опустились границы диафрагмы. Прикорневой застой уменьшился. Тем не менее, сердце остается большим в поперечнике. Выбухает силуэт легочной артерии, правого предсердия. Следовательно, сохраняются все рентгенологические признаки застойной сердечной недостаточности. Отчетливо видны линии Керли 2. Признаки застойного интерстициального отека у нашей пациентки присутствуют.
При компьютерной томографии грудной клетки (стрелками показано) – довольно значительный выпад в плевральных полостях и большие камеры сердца. Здесь на примере левого предсердия – большое левое предсердие.
При компьютерной томографии грудной клетки – при положении пациентки на животе. Она не могла лежать на спине, поскольку ее душил кашель, не хватало воздуха. Мы видим признаки, подтверждающие наличие интерстициального отека, утолщения междолькового перибронхиваскулярного интерстиция. Данных за инфильтрацию легочной ткани нет.
На эхокардиограмме в октябре 2010-го года мы видим признаки увеличения камер сердца, желудочков, предсердий. Фракция выброса левого желудочка – 22%. Систолическое давление в легочной артерии – 65 миллиметров рт. ст. Специалисты отмечают нарастание степени дилатации левого предсердия, легочной гипертензии и давления в правом предсердии.
При ультразвуковом исследовании брюшной полости подтверждаются признаки правосердечной декомпенсации. Воротная вена незначительно расширена. А нижняя полая вена расширена до 32-х миллиметров. Печеночные вены расширены до 14-ти миллиметров. В брюшной полости свободной жидкости не определяется. Следовательно, подтверждается наличие правосердечной декомпенсации.
Для того чтобы все-таки решить вопрос с природой тех изменений в миокарде, с которыми мы встретились, была проведена серия исследований. В частности, пациентке была проведена перфузионная томосцинтиграфия. Вы видите результаты исследования верхушки и передней стенки.
Специалисты отмечают массивную зону гипоаккумуляции индикатора, указывающие на дефект перфузии в передне-перегородочно-задней локализации. Делают заключение о наличии признака крупноочагового поражения миокарда. По существу, эти изменения совпадают с теми изменениями на электрокардиограмме, которые мы видели на предшествующих электрокардиографических картинках.
Больной была проведена мультиспиральная компьютерная томографическая ангиография. Она поставила нас в сложное положение, поскольку было отмечено, что в дистальном сегменте правой коронарной артерии контрастирование отсутствует. Вновь встал вопрос о возможности перенесенной нашей пациенткой инфаркта миокарда. Это потребовало или прямого подтверждения, или отрицания этой возможности.
Здесь продолжение этого исследования. В области верхушки – подозрение на наличие тромба. Вот мы спроецировали на схеме те данные, которые получили с помощью электрокардиографии, эхокардиографии, сцинтиграфии и мультиспиральной компьютерной томографии. Выясняется, что верхушка, перегородка и латеральная стенка левого желудочка гипоперфузированы, то есть поражены.
Здесь правая коронарная артерия. Вы помните, что при мультиспиральной компьютерной томографии возникло подозрение об окклюзии правой коронарной артерии в дистальной ее части. При проведении коронарографии – видите, коронарная артерия – контуры ровные. По существу, она не изменена на всем своем протяжении, в том числе в дистальных отделах.
Следовательно, тромбоишемическая природа, то есть попросту инфаркт миокарда у этой пациентки нами был отвергнут. При чреспищеводной эхокардиографии обращает на себя внимание гиперэхогенность миокарда межжелудочковой перегородки, а также выраженная трабекулярность заднебоковой стенки левого желудочка, что позволяет думать о синдроме некомпактности миокарда с его инфильтрацией, то есть возможностью саркоидоза или амилоидоза. Хотя, конечно, сама по себе клиническая картина не совпадает с предположением о саркоидном гранулематозном или амилоидозном поражении миокарда.
Пациентке была сделана магнитно-резонансная томография сердца. Отмечено, что имеет место акинез передней и нижней стенок левого желудочка в верхушечном и среднем сегментах, межжелудочковой перегородке, верхушечном сегменте. Гипокинез межжелудочковой перегородки в среднем сегменте, базальных сегментов передней и нижней стенок. Отмечается повышенная трабекулярность верхушечного сегмента боковой стенки (без критериев некомпактности миокарда).
Следовательно, мы в значительной степени (с учетом клинической картины) можем не принимать во внимание амилоидоз и саркоидоз. А полученные данные совпадают с предшествующими исследованиями о массивном поражении миокарда у нашей пациентки.
Таким образом, данных за объемные поражения сердца, синдрома некомпактности миокарда не выявлено. Магнитно-резонансная картина, как отмечают специалисты, может соответствовать миокардиту с поражением левого и правого желудочка.
Возвращаемся к таблице проведения дифференциального диагноза. Итак, мы должны предположить, исходя из тех клинических данных, которые имеем. Эта таблица, конечно, не охватывает полностью всю симптоматику миокардитов. Здесь включены только те данные, которые наиболее ярко, рельефно были выявлены у нашей пациентки.
Первое – это подъем сегмента ST. При каких формах миокардитов, как правило, наблюдается подъем сегмента ST. Это или острый гиперсенситивый эозинофильный миокардит, или острый (или подострый) некротизирующий эозинофильный миокардит.
На что дальше нам следует обратить внимание. При каких формах миокардита мы можем встретиться с выраженным некрозом миокарда. Фактически при всех формах миокардита (инфекционном, аутоимуннном, гигантоклеточном) возможны очень небольшие участки некроза миокарда.
Но столь массивный некроз миокарда, который мы предполагаем у нашей пациентки, может встретиться или при остром гиперсенситивном эозинофильном миокардите, или при остром некротизирующем эозинофильном миокардите.
Но если говорить об этих двух формах, то при остром гиперсенситивном эозинофильном миокардите главной клинической картиной является нарушение ритма. Аритмия различного рода характеризует острый гиперсенситивный эозинофильный миокардит, протекающий с подъемом ST. Тогда как для острого некротизирующего миокардита (или подострого некротизирующего миокардита) характерно массивное поражение миокарда с развитием застойной сердечной недостаточности.
Теперь, если мы обратимся к темпам развития миокарда, характеризующим развитие всех этих неблагоприятных последствий, такое подострое течение характерно для идиопатического гигантоклеточного миокардита и подострого некротизирующего миокардита. При идиопатическом гигантоклеточном миокардите все-таки основной клинической формой являются тяжелые нарушения ритма. Они определяют течение и прогноз заболевания. Тогда как при подостром некротизирующем миокардите речь идет о быстром развитии, формировании застойной сердечной недостаточности.
Поэтому, исходя из таких критериев (плюс проведенный дифференциальный диагноз с привлечением многочисленных инструментальных исследований), мы все-таки остановились на возможности у нашей пациентки наличия подострого некротизирующего эозинофильного миокардита, вторичной дилатационной кардиомиопатии, легочной гипертензии. Относительной недостаточности митрального, трикуспидального клапанов. Относительно небольшие нарушения ритма и проводимости, неполная блокада правой ножки и так далее. Речь в данном случае шла, на наш взгляд, о подостром некротизирующем миокардите.
Естественно, такая неблагоприятная тенденция в падении сократительной функции заставила нас проконсультироваться, пригласить специалистов из Научно-исследовательского института трансплантологии и искусственных органов имени академика Шумакова. Мы договорились с директором Института академиком Готье. Он направил специалистов, и пациентка была переведена в Институт трансплантологии.
Там ей была проведена трансплантация сердца, и поставлен диагноз. Постмиокардитический кардиосклероз с дилатацией полостей сердца. Относительная недостаточность митрального и трикуспидального клапана и так далее. Наши представления о том, что она переносила миокардит, совпали.
К сожалению, нам не удалось получить результаты гистологического исследования, которые бы подтвердили или отвергли наше представление о характере миокардита. Но сам по себе факт совпадения нашего клинического диагноза и хирургического диагноза плюс наличие небольшой эозинофилии периферической крови и небольшого повышения иммуноглобулина Е все-таки утверждает нас в предположении о наличии подострого деструктивного некротизирующего миокардита.
Дальше, после трансплантации сердца пациентке были, естественно, рекомендованы необходимые препараты, которые здесь указаны.
Через год она вновь у нас в клинике. Мы видим, что она себя чувствует прекрасно. Она по-прежнему такая изящная – весит 55 кг, рост – 168. Частота дыхания – 17. Нормальное артериальное давление. Некоторая склонность к тахикардии, что типично, характерно.
Вот ее электрокардиограмма, собственно, кардиограмма трансплантированного сердца. Мы видим совершенно другую картину. На эхокардиограмме все хорошо, благоприятно. Размеры камер сердца соответствуют, неплохие. Они будут иметь тенденцию предсердию уменьшаться. Сократительная функция – фракция выброса почти 60%.
Наиболее часто хирурги выполняют трансплантацию при следующих патологиях:
1. Ишемическая болезни сердца.
2. Дилатационная кардиомиопатия.
3. Приобретенные пороки сердца.
4. Врожденные пороки сердца.
5. Ретрансплантации сердца.
6. Другие патологии.
Наша пациентка попадает в категорию дилатационной кардиомиопатии как результат перенесенного тяжелого некротизирующего миокардита. Это одна из наиболее частых форм показаний.
Какие конкретно показания к трансплантации, были ли они у нашей пациентки. Медикаментозно-рефрактерная конечная стадия хронической сердечной недостаточности у нашей пациентки, безусловно, уже сформировалась. Фракция изгнания левого желудочка – меньше 20%. У нашей пациентки – 15%.
Конечно-диастолическое давление в левом желудочке – более 25-ти. У нашей пациентки тоже было высокое конечное диастолическое давление. Сердечный индекс у нее был менее 2-х литров в минуту на квадратный метр. Следовательно, трансплантация сердца ей была проведена вовремя.
Каков прогноз. Наша пациентка живет уже полтора года. Прогноз неплохой. Годичная выживаемость – она вошла в эту группу (86%). Трехгодичная – 77%, пятилетняя – 69%. Мы будем надеяться, что наша пациентка постоянно будет находиться в этих удачных группах. Мы желаем ей здоровья и благополучия в ее дальнейшей жизни. Спасибо за внимание.
Оксана Драпкина: Спасибо большое, Владимир Трофимович. Уже поступают вопросы.
Вопрос: Почему этой женщине не проводили биопсию миокарда?
Владимир Ивашкин: Биопсия миокарда – это непростая процедура. Ее целесообразно проводить, когда состояние пациента или пациентки позволяет эту процедуру делать.
У нашей пациентки наблюдалась прогрессирующая сердечная декомпенсация. Поэтому тот большой объем консервативных диагностических исследований, который был проведен, убедил нас в том, что мы правы. Речь идет о миокардите, а не о каких-то других формах. Поэтому по согласованию с трансплантологами мы направили пациентку. Они ее приняли, и, видите, все прошло удачно.
Я надеюсь, что у этой пациентки хороший жизненный прогноз. Во-первых, она молодая женщина. Во-вторых, у нее нет никаких факторов риска. Видите, она изящная женщина с нормальным артериальным давлением. У нее абсолютно чистая коронарограмма (как вы посмотрели), нет никаких привходящих заболеваний. Ничто не омрачает ее будущего. Будем надеяться, что все будет благополучно.
Оксана Драпкина: Спасибо большое, Владимир Трофимович. Думаю, будут еще вопросы поступать. У нас закончилась секция «Лекции, мастер-классы, клинический разбор».