гиперваскулярное образование печени что это такое и как лечить
Нодулярная гиперплазия печени
Нодулярная гиперплазия печени – очаговое образование в паренхиме печени, морфологически представляющее собой разрастание нормальных гепатоцитов вокруг сосудистой мальформации. Причины развития данной патологии неизвестны, определенная роль отводится сосудистым аномалиям, приему гормональных препаратов. В течение длительного времени заболевание может никак не проявляться; при достижении опухолью определенных размеров беспокоит болевой синдром, диспепсические явления. Диагностика включает проведение УЗИ печени, КТ, МРТ, обязательна биопсия. Лечение при малых размерах гиперплазии не требуется, при крупном образовании с тенденцией к росту проводится энуклеация опухоли или сегментарная резекция печени.
Общие сведения
Нодулярная гиперплазия печени (очаговый цирроз, паренхиматозная гамартома) является второй по частоте доброкачественной опухолью печени после гемангиомы. Согласно данным аутопсий, распространенность нодулярной гиперплазии составляет около 2%. Диагностироваться данная патология может в любом возрасте, но в 95% случаев выявляется у женщин 30-40 лет. Чаще всего это одиночное образование, не имеющее капсулы и не превышающее в диаметре 5 см; крайне редко встречается множественное поражение.
В гастроэнтерологии выделяют два типа нодулярной гиперплазии печени: классический (диагностируется в 80% случаев) и неклассический. Классический тип характеризуется наличием трех признаков: аномальной структуры дольки, извилистых толстостенных сосудов и гиперплазии желчных протоков; в 60% наблюдений обнаруживается центральный рубец с измененными сосудами разного калибра. При неклассическом типе всегда есть гиперплазия протоков, а один из оставшихся признаков (измененные сосуды или аномальная узловая архитектура) может отсутствовать. Неклассический тип подразделяют на три подтипа: аденоматозный гиперпластический, телеангиэктатический и нодулярную гиперплазию печени с клеточной атипией.
Причины нодулярной гиперплазии печени
Этиология нодулярной гиперплазии печени окончательно не изучена. Предполагают, что гиперплазия печеночной паренхимы связана с наличием сосудистых мальформаций, нарушающих локальный кровоток, применением глюкокортикостероидов, высокодозированных комбинированных оральных контрацептивов, эндогенной гиперэстрогенией. Довольно часто нодулярная гиперплазия печени сочетается с гемангиомами; зарегистрированы случаи ее развития на фоне кавернозной трансформации или врожденного отсутствия воротной вены, воспалительных заболеваний печени, тромбоза печеночных вен, артериовенозного внутриорганного шунтирования, наследственных геморрагических телеангиэктазий и цереброваскулярных заболеваний.
Нодулярная гиперплазия печени макроскопически представляет собой плотный узел серо-коричневого цвета, четко отграниченный от окружающих тканей. Его размеры могут быть различными: от 1 до 25 сантиметров в диаметре. На разрезе определяется центральный рубец – фиброзная ткань, которая распространяется к периферии и разделяет образование на дольки. Микроскопическими признаками нодулярной гиперплазии печени являются дезорганизация печеночных долек: имеют место воспалительные клеточные инфильтраты, пролиферированные протоки, утолщенные сосуды и фиброзная ткань.
Симптомы нодулярной гиперплазии печени
В большинстве случаев данная патология протекает бессимптомно и выявляется при проведении обследования по поводу других заболеваний. Клинические признаки имеют место менее чем у половины пациентов, при этом они неспецифичны. Наиболее частый симптом – боль в животе, локализованная в правом подреберье. Чаще боль постоянная, ноющего характера, возможно чувство тяжести. Болевой синдром при нодулярной гиперплазии является следствием растяжения капсулы печени или сдавления соседних органов.
При нодулярной гиперплазии печени пациента также могут беспокоить диспепсические явления: тошнота, снижение аппетита. В случае больших размеров образования возможна его пальпация через переднюю брюшную стенку. Не установлена связь между размером опухоли и наличием симптомов, поскольку более важна локализация образования относительно окружающих органов. Крайне редко развиваются такие осложнения нодулярной гиперплазии печени, как механическая желтуха, кровотечение из опухоли и малигнизация.
Диагностика нодулярной гиперплазии печени
Консультация гастроэнтеролога обычно выявляет неспецифические признаки заболевания: диспепсические явления, болевой синдром малой интенсивности. При объективном обследовании пациента опухоль большого размера может быть обнаружена пальпаторно, в случае нарушения оттока желчи определяется желтушность кожи и склер. Лабораторные методы исследования не выявляют никаких специфических для нодулярной гиперплазии печени признаков. Редко обнаруживается некоторое повышение уровня аланинаминотрансферазы, билирубина. С целью дифференциальной диагностики со злокачественными новообразованиями печени обязательно проводится определение онкомаркеров: альфа-фетопротеина, СА 19-9, СЕА.
Диагностика нодулярной гиперплазии печени основана на инструментальных методиках. Характерным признаком данной патологии является «звездчатый шрам» в центре образования, но он выявляется не у всех пациентов, кроме того, может быть обнаружен при фиброламеллярной карциноме, внутрипеченочной холангиокарциноме и других заболеваниях. Это диагностическое ограничение относится ко всем методикам визуализации: УЗИ печени, КТ и МРТ печени. При проведении УЗИ органов брюшной полости единственным признаком нодулярной гиперплазии печени может быть смещение сосудов, иногда определяется гипоэхогенный ободок опухоли (сдавленные образованием сосуды и паренхима). Более информативно исследование в режиме допплеровского сканирования, при котором визуализируется гипертрофированная центральная артерия.
При проведении компьютерной томографии выявляется хорошо отграниченное образование, накопление контрастного вещества в области гиперплазии. МРТ дает аналогичные результаты: гиперинтенсивность контрастирования в артериальную фазу и гипоинтенсивность – в венозную. Неинвазивные методики обладают специфичностью только при классическом типе нодулярной гиперплазии печени. Высокой информативностью при проведении дифференциальной диагностики с другими гиперваскулярными образованиями обладает сцинтиграфия печени. В затруднительных случаях может быть выполнена ангиография, но данный метод также неспецифичен.
При невозможности установить диагноз в ходе неинвазивных исследований проводится биопсия, при этом большими критериями диагностики является наличие толстостенных сосудов, фиброзной прослойки, пролиферирующих протоков, узловой вид опухоли; малыми критериями – перисинусоидальный фиброз и синусоидальная дилатация. Диагноз достоверен при наличии трех больших критериев, вероятный – при определении двух больших и 1-2 малых.
Дифференциальная диагностика нодулярной гиперплазии проводится с другими доброкачественными и злокачественными образованиями печени, крупноузловым циррозом, а также с регенеративной гиперплазией при системных заболеваниях соединительной ткани.
Лечение и прогноз нодулярной гиперплазии печени
В большинстве случаев лечение нодулярной гиперплазии печени не требуется. Если опухоль не достигла больших размеров, не сдавливает соседние органы, не имеет тенденции к увеличению, основной целью является устранение этиологического фактора (если он известен). Отмены гормонального контрацептива, снижения дозировки системных глюкокортикостероидов может быть достаточно для уменьшения размеров образования и его полной регрессии. Однако пациент должен регулярно проходить обследование с целью контроля размеров опухоли и своевременного выявления показаний к хирургическому лечению.
Если нодулярная гиперплазия печени крупная, нарушает отток желчи, препятствует кровообращению или сдавливает соседние органы, проводится энуклеация опухоли или сегментарная резекция печени. Оперативное лечение также требуется в случаях, когда диагноз окончательно не установлен, и опухоль имеет тенденцию к увеличению (в такой ситуации удаление образования проводится даже при нормальных результатах биопсии).
Прогноз при нодулярной гиперплазии печени благоприятный. Заболевание в течение длительного времени может никак не беспокоить пациента, а осложнения развиваются крайне редко. Специфической профилактики не существует. Необходимо обоснованное назначение гормональных препаратов, а при установленном диагнозе обязательно регулярное проведение УЗИ печени для контроля над течением заболевания.
Некоторые аспекты диагностики фокальной нодулярной гиперплазии печени (фибронодулярной гиперплазии)
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Еще сравнительно недавно фокальная нодулярная гиперплазия печени (ФНГ) относилась к редким (3%) объемным образованиям печени. Однако, учитывая применение современных методов визуализации, в настоящее время ФНГ занимает 3-е место среди доброкачественных образований печени после гемангиомы и аденомы [8, 10, 14].
Согласно морфологической классификации опухолей печени, ФНГ относится к опухолеподобным процессам и характеризуется гиперплазией печеночной паренхимы, разделенной на узлы фиброзными прослойками в виде звездчатого рубца [14]. Гиперпластические узлы без четких границ переходят в окружающую ткань, не сдавливая ее. Опухоль состоит из гепатоцитов, элементов желчных протоков, купферовских клеток и фиброзной ткани.
ФНГ развивается в любом возрасте, одинаково часто у лиц разного пола. В то же время имеются данные о том, что подобные новообразования чаще диагностируются у женщин (в 82,2% случаев) [10, 17].
Макроскопически очаговая узловая гиперплазия представляет собой мягкоэластичный, четко ограниченный, иногда инкапсулированный узел серовато-коричневого цвета размером от 0,5 до 6 см. Узлы могут быть как одиночными, так и множественными и располагаться в периферических отделах правой (чаще) и левой доли. Иногда узлы заметно выбухают на поверхности печени, в редких случаях они имеют ножку. Узлы имеют дольчатую структуру с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
При микроскопическом исследовании узлов определяют нормальные гепатоциты, содержащие гликоген и формирующие трабекулярные структуры. Местами наблюдается полиморфизм величины и формы зрелых гепатоцитов, они образуют синцитий. В центре печеночной доли, как правило, располагается центральная вена, имеются синусоиды, выстланные купферовскими клетками (звездчатые ретикулоэндотелиоциты). Портальные прослойки сформированы правильно, достаточно деликатны. В зоне звездчатого рубца и по ходу стромы располагаются сосуды. Сосу дис тый компонент весьма разнообразен как по содержанию (венозные, толстостенные артериальные сосуды с миксоматозной дегенерацией среднего слоя), так и по форме (гемангиоматоз). По ходу портальных септ определяются пролиферирующие желчные протоки, единичные мелкие узлы регенерации и лимфоплазмоцитарные инфильтраты. Эти признаки служат основными дифференциально-диагностическими критериями, позволяющими отличить ФНГ от печеночно-клеточной аденомы [17].
Выделяют 2 типа ФНГ: классическая и неклассическая. При классическом типе выделяют все 3 признака: аномальная нодулярная структура, извилистые толстостенные сосуды, гиперплазия желчных протоков. Центральный рубец присутствует в 65% наблюдений. Он всегда содержит измененные сосуды разного калибра: большие извилистые артерии с гипертрофией интимы и медии, крупные и мелкие вены, капилляры. При неклассическом типе отсутствует один из двух признаков (нодулярная структура или измененные сосуды), но гиперплазия протоков есть всегда. Централь ный рубец отсутствует. В свою очередь неклассический тип делится на 3 подтипа: телеангиэктатический (склонный к кровотечениям), аденоматозный и ФНГ с клеточной атипией.
Опухоль в большинстве случаев (66,7-80,8% пациентов) не проявляет себя клинически и может быть случайно обнаружена при проведении ультразвукового исследования (УЗИ) по иному поводу [18]. Специфичные лабораторные симптомы отсутствуют. ФНГ не озлокачествляется и край не редко вызывает осложнения в виде внутрибрюшного кровотечения.
Ультразвуковая картина ФНГ
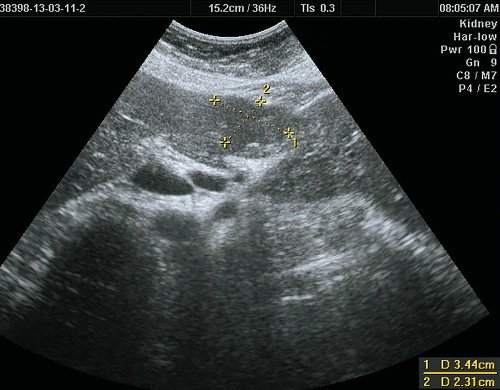
Так, при УЗИ в В-режиме вид ФНГ неспецифичен и вариабелен. Чаще всего ФНГ печени выглядит как единичное очаговое образование с нечеткими или четкими, ровными или неровными контурами, несколько неоднородное по своей внутренней структуре, без капсулы. В 80% случаев (рис. 1) очаг изоэхогенный или гипоэхогенный [3, 8, 9, 11-14].
а) В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Диагностика и лечение опухолей печени (рака печени)
Статья проверена 30.03.2021. Статью проверил специалист: Трандофилов Михаил Михайлович, профессор, д.м.н., хирург-онколог, специалист по онкологии печени и желчевыводящих путей.
Печень – жизненно важный орган, без которого наш организм не может функционировать. Печень выполняет важнейшие функции – очищает организм от токсинов и шлаков, синтезирует необходимые биологически активные вещества, поддерживает и защищает нас от инфекций, участвует в обменных процессах, накапливает питательные вещества…
Любое заболевание печение нарушает работу этих функций, что, естественно, сразу же сказывается на здоровье человека. Одной из самых серьезных проблем являются опухоли печени.
Опухоли в печени возникают в том случае, если в ткани органа присутствует хотя бы одна генетически поврежденная раковая клетка. Она начинает неконтролируемо делиться и, через некоторое время, значительно увеличивает число раковых клеток в этом месте. Если при помощи диагностических исследований можно обнаружить эту область, то можно говорить о том, что у человека опухоль печени.
Злокачественные опухоли печени делятся на две группы – это первичные опухоли печени и вторичные метастатические опухоли.
Первичные опухоли печени
Гепатоцеллюлярная карцинома
Гепатоцеллюлярная карцинома (ГЦК) – одна из самых распространенных первичных опухолей печени. Она встречается в 85% случаев первичных злокачественных поражений печени.
Заболевание широко распространено в Южной Африке, Японии, Китае, Юго-Восточной Азии. Опухоль исходит из гепатоцитов (клеток печени). Макроскопически опухоль представлена солитарным (одиночным) или несколькими узлами плотно-эластичной консистенции, белесоватого цвета, на разрезе с множественными очагами геморрагии, некроза и локального пропитывания желчью. Опухоль может иметь четко ограниченную капсулу, диффузно инфильтрировать печень или выступать над ней.
Реже встречаются такие опухоли, как холангиокарциномы (опухоли из эпителия внутрипеченочных желчных протоков). Опухоль диагностируется преимущественно у больных старше 50 лет и составляет до 25 % от всех злокачественных опухолей печени. Опухоль представлена каменистой плотности узлами белесовато-серого цвета. Выделяют также смешанные гепатохолангиокарциномы, и фиброламеллярные карциномы. Значительно реже встречаются саркомы печени, ангиосаркомы (опухоли исходящие из сосудов печени), цистоаденокарциномы.
Чаще всего опухолевый процесс развивается на фоне цирроза и хронических вирусных гепатитов. Как правило, с момента заболевания печени до клинически определяемой опухоли предположительно проходит 20-30 лет. Однако в 25% случае при гепатоцеллюлярной карциноме у пациентов не выявляется ни цирроз, ни какие-либо другие факторы риска развития опухоли.
По статистике, гепатоцеллюлярная карцинома занимает 6 место среди других онкологических заболеваний в мире и весьма высокое 3 место среди причин смертности от онкологических заболеваний. Распространенность опухоли составляет 2-3 случая на 1000000 человек. Среди пациентов преобладают мужчины 40-50 лет.
Симптомы
На ранних стадиях первичные опухоли печени протекают бессимптомно. Симптомы заболевания проявляются, как правило, при уже распространенном процессе. Больной, в основном, жалуется на тяжесть и боль в правом подреберье и правой половине брюшной полости, потерю веса. Как правило, при осмотре у таких пациентов есть признаки увеличения печени. Кроме того, могут выявляться симптомы цирроза и/или печеночной недостаточности (желтушность кожных покровов). Край печени выступает из-под края реберной дуги на 2-3 см, на ощупь – бугристый, при больших размерах опухолей пальпируются узлы в печени.
Диагностика
Для определения точного диагноза необходимо выполнение ультразвукового исследования (УЗИ) и компьютерной томографии печени с контрастированием для определения уровня специфического онкомаркера Альфа-фетопротеина (АФП), который повышен у 90% больных с гепатоцеллюлярной карциномой. Его выявление служит подспорьем в уточнении и подтверждении диагноза.
При наличии цирроза и гиперваскулярного узлового образования в печени (2 см), выявляемого при динамическом контрастном исследовании, при повышении уровня АФП выше 400 нг/мл ставится предварительный диагноз ГЦК.
Также с целью постановки диагноза больным выполняется биопсия печени с гистологическим исследованием материала, позволяющая в 100 % случаев поставить диагноз.
Методы лечения
Трансплантация печени – единственный путь к полному выздоровлению при гепатоцеллюлярной карциноме.
В России за последние 10 лет произведено около 40 трансплантаций при первичных опухолях печени.
При выполнении трансплантации печени соблюдаются строгие критерии отбора больных (миланские критерии), при которых максимальный размер одной опухоли не должен превышать 5 см или три опухолевых узла не больше 3 см в максимальном размере. При соблюдении вышеперечисленных критериев, 10-летняя выживаемость больных составляет 50-60 %.
К сожалению, существует большая проблема нехватки донорских органов и, вследствие этого, возникает длительный лист ожидания трансплантации. Кроме того, пациенты часто обращаются в такой момент, когда опухоль уже превышает размеры, допустимые для трансплантации печени.
Для увеличения продолжительности жизни пациентов, находящихся в листе ожидания на трансплантацию печени, им проводится радиочастотная деструкция опухолей печени.
Для того чтобы вовремя выявить пациентов с первичными опухолями печени, проводятся различные скрининговые программы ранней диагностики. К этой группе относят всех больных с циррозом печени, хроническими вирусными гепатитами и наличием очаговых поражений печени.
Этим больным в ходе диагностического поиска активно применяется алгоритм Bruix et al. (2001), основанный на мониторинге изменений при динамических сонографических исследованиях, компьютерной томографии и контроле уровня альфа-фетопротеина каждые 6 месяцев. При наличии очаговых образований в печени превышающих 1 см, повышении уровня альфапротеина, а также при усилении образования в артериальную фазу при контрастировании, больным выполняется биопсия печени с целью ранней диагностики первичных опухолей печени. И, в частности, гепатоцеллюлярной опухоли, как самой встречающейся формы рака печени.
Резекция печени – этот метод оперативного лечения рака печени проводится только в том случае, если у пациента нет цирроза печени, при отсутствии прорастания опухолью крупных сосудов печени и нижней полой вены, при поражении одной доли печени и отсутствии внеорганных метастазов. К сожалению, к этой подгруппе относится только около 20% больных.
Резекция может быть проведена у некоторых больных с циррозом только при условии сохранной функции печени, нормальном уровне билирубина и без портальной гипертензии.
Пациентам с высоким риском развития декомпенсации печеночной функции резекцию печени не проводят.
Наилучшие результаты после резекции получены в группе больных с опухолью менее 5 см, ограниченной пределами органа и без признаков проникновения опухоли в магистральные сосуды.
Проводятся следующие виды операций анатомические резекции печени различных объемов:
Радиочастотная деструкция (абляция) – проводится тем больным, которым противопоказано проведение резекции опухоли печени или невозможна трансплантация печени (вследствие наличия тяжелой сопутствующей патологии, выряженных явлений цирроза).
Проведение радиочастотной деструкции показано при максимальном размере опухоли до 5 см. Также возможно проведение деструкции при одновременном поражении двух долей печени, наличием внеорганных метастазов, печеночной недостаточности.
При таком лечении рака печени соблюдаются те же критерии, что и при резекции. Обязательно отступают на 10 мм от видимой зоны опухоли, с увеличением зоны термодеструкции превышающим размер опухоли на 10 мм (так называемая зона абластики).
Радиочастотная абляция выполняется чрескожно чреспеченочно под контролем ультразвука или лапароскопическим контролем. Вследствие этого наблюдается минимальное количество осложнений и отсутствуют летальные исходы.
Группе пациентов со стадией С, которым противопоказано хирургическое лечение рака печени, как правило проводится эмболизация питающей опухоль артерии, таргетная терапия.
Вторичные опухоли печени
Метастатические опухоли
Одним из характерных свойств опухолей является их способность метастазировать – раковые клетки «отрываются» от первичной опухоли, распространяются через кровь или лимфатические сосуды в другие, здоровые органы и ткани и дают в них начало новым очагам роста. Так образуются метастазы в печени.
Метастатическими опухолями называются опухоли, являющиеся злокачественными клетками первичной опухоли, попавшими в другой орган различными путями:
Этот процесс приводит к развитию в органе вторичной опухоли. Причем размер такой опухоли может превышать размер первичной опухоли в несколько раз.
Чаще всего метастазы в печени возникают при поражении опухолями желудочно-кишечного тракта, молочной железы, почек.
В последние годы увеличилось количество онкологических больных с метастазами в печени. Так в России раком ободочной кишки ежегодно заболевают 23 000 человек и раком прямой кишки – 17 000 человек. К тому времени, как устанавливается диагноз, метастазы в печени выявляются у 30 % больных. При раке молочной железы метастазы в печени обнаруживаются в 15-67 % случаев.
Симптомы
Клинические проявления заболевания, как правило, отсутствуют. При больших размерах опухолей или множественном поражении обоих долей печени появляются жалобы на общую слабость, тяжесть и боли в правом подреберье, желтушность склер и кожных покровов. При пальпации в области правого подреберья ощущаются плотные, не смещаемые бугристые образования, болезненные при глубоком нажатии.
Диагностика
Всем, кто уже ранее оперировался по поводу злокачественных опухолей желудка, толстой и прямой кишки, почки и молочной железы, необходимо проведение ультразвукового исследования печени, определения онкомаркеров, рентген грудной клетки раз в 3-6 месяцев – в зависимости от стадии развития первичной опухоли.
При проведении УЗИ возможно выявление опухолей более 1 см в диаметре, в виде гиперэхогенной опухоли с гипоэхогенным ободком.
При наличии подозрений на метастатическую опухоль печени выполняют рентгенкомпьютерную томографию печени с контрастированием или позитронно-эмиссионную томографию печени (ПЭТ). Контраст накапливается в опухоли и позволяет увидеть все опухоли печени диаметром от 0,5 см. С целью дифференциальной диагностики выполняется биопсия печени чрескожно чреспеченочно под контролем ультразвука.
Методы лечения
Показаниями к оперативному лечению больных с метастазами в печени традиционно является наличие одиночного метастаза большого размера (I стадия) или опухолей небольших размеров при их унилобарной локализации (II cтадия).
Количество больных с одиночными метастазами небольших размеров или одиночными метастазами больших размеров не превышает 14-18 % от числа всех больных с метастатическим поражением печени. Вследствие этого, резектабельность больных с метастатическим раком печени составляет 14-18%.
Резекция печени
При хирургическом лечении метастаз в печени применяются различные виды операций в зависимости от этиологии поражения органа.
Резекция печени – одна из наиболее часто встречающихся операций при лечении рака печени. По принципу выполнения в настоящее время их принято делить на типичные резекции (анатомические, центральные) и атипичные (периферические).
Атипичными периферическими резекциями печени называются резекции, при которых выделение удаляемой части печени осуществляется с помощью метода дигитоклазии с поэтапной перевязкой сосудов и желчных протоков. К атипичным резекциям относятся операции, выполненные без предварительной перевязки сосудисто-секторальной ножки.
При лечении рака печени больным выполняются анатомические и атипичные резекции различных объемов, такие как:
В настоящее время, несмотря на использование при резекциях печени современной хирургической техники и физических методов воздействия, остается довольно высокой частота интраоперационных и послеоперационных осложнений при выполнении резекции печени при метастатических раках печени. Эти показатели колеблются от 23 до 55 %.
При билобарной локализации вторичных опухолей печени (в двух долях), множественном распространении II и III степени объемов поражения печени с поражением забрюшинных лимфоузлов, лечение рака печени 4 стадии при помощи традиционных оперативных вмешательств затруднено из-за превышения риска оперативного пособия над эффектом от операции. Таким онкологическим больным требуется паллиативная помощь.
Вследствие этого, проводятся активные поиски новых малоинвазивных технологий хирургического лечения с целью улучшения качества и продолжительности жизни этой тяжелой и обреченной категории больных.
Радиочастотная деструкция (абляция)
Одной из современных малоинвазивных технологий при лечении рака печени является использование радиочастотной абляции метастазов в печени.
Радиочастотная деструкция проводится пациентам с размером опухоли до 50 мм, с увеличением зоны деструкции превышающим размер опухоли на 10 мм (так называемая зона абластики). Малоинвазивные операции выполняются чрескожно чреспеченочно под контролем ультразвука или лапароскопическим контролем.
Прогноз результатов лечения метастаз в печени методом радиочастотной деструкции благоприятный – наблюдается минимальное количество осложнений, отсутствую летальные исходы.
Преимуществами данной методики перед традиционными резекциями являются:
Всем больным после проведения радиочастотной деструкции проводится полихимиотерапия.
Непаразитарные кисты печени
Кисты печени делятся на паразитарные и непаразитарные кисты. В свою очередь непаразитарные кисты печени бывают:
Кисты в печени возникают в результате нарушения формирования желчных ходов в процессе внутриутробного развития. При этом образуются группы аберрантных (закупоренных) желчных капилляров, которые в последствие постепенно расширяются в связи со скоплением в них серозной жидкости. Кроме того, кисты могут образоваться на фоне воспалительных и дегенеративных изменений в желчных путях и печени.
В упрощенном варианте кисты печени можно подразделить:
Симптомы
Кисты печени в большинстве случаев протекают без клинических проявлений. Симптомы заболевания появляются только при наличии больших кист (чувство дискомфорта, ноющие боли в области правого подреберья), а также при возникновении осложнений (кровоизлияние, нагноение, перфорация, желтуха).
Простые кисты печени в 50% бывают одиночными, в остальных случаях — множественными. Размеры их могут достигать от 1,0 до 20 см. В редких случаях простые кисты могут по неизвестным причинам быстро увеличиваться в размерах, вызывая соответствующую болевую симптоматику, что наблюдается преимущественной у женщин старше 50 лет.
Диагностика
Для диагностирования кисты необходимо пройти ультразвуковое исследование (УЗИ) или компьютерную томографию.
Методы лечения
К радикальному удалению кисты следует прибегать только в случае цистаденомы и опасности ее опухолевого перерождения. Кисты печени менее 5 см в диаметре подлежат динамическому контролю, кисты диаметром от 5,0 до 10,0 см и более подлежат оперативному лечению
Операции на печени при непаразитарных кистах варьируются от простой пункции до резекции печени. Операции можно условно разделить на следующие основные группы:
1. Условно-радикальные:
2. Паллиативные:
Рациональный выбор паллиативной помощи онкологическим больным зависит от вида кисты, ее взаимоотношения с печенью, наличием или отсутствием осложнений, ее размеров и тяжести состояния больного.
Чрескожное чреспеченочное дренирование кисты под контролем ультразвука.
Кисты диаметром от 5,0 до 10,0 см в 90% случаев излечиваются пункционно-склерозирующим способом.
Под контролем УЗИ в полость кисты чрескожно чреспеченочно вводят дренаж, и после удаления содержимого кисты ее полость промывается спиртовым раствором. Содержимое кисты отправляют на цитологическое исследование. В редких случаях приходится прибегать к повторным пункциям. Дренаж в полости кисты оставляется на несколько дней. До склерозирования кисты, после сокращения кисты в размерах дренаж удаляют. Процесс лечения контролируется ультразвуковым исследованием в динамике.
Необходимость оперативного вмешательства возникает при симптоматических и рецидивирующих после пункций больших кистах печени (более 10,0 см), а также цистаденомах. С развитием эндоскопической хирургии появилась возможность иссечения кист под контролем видеолапароскопии.
Вылущевание, экстирпация или перицистэктомия кист печени – одна из самых распространенных операций. Оперативное вмешательство заключается в полном удалении стенок кисты.
Частичное иссечение стенок кисты
Паллиативная помощь онкологическим больным методом частичного иссечения стенок кисты с ушиванием и дренированием остаточной полости, обычно применяется при больших размерах кист, при расположении кист вблизи ворот печени, крупного сосуда или желчного протока. Важно отметить, что лишь при отсутствии примеси желчи в содержимом возможно иссечение купола стенки кисты, оставляя ее основание интактным в толще паренхимы печени.
Инфицированные кисты паразитарной и непаразитарной этиологии требуют выполнения наружного дренирования или марсупилизации.
При кистах, содержащих желчь необходима цистоэтеро- или гастростомия.