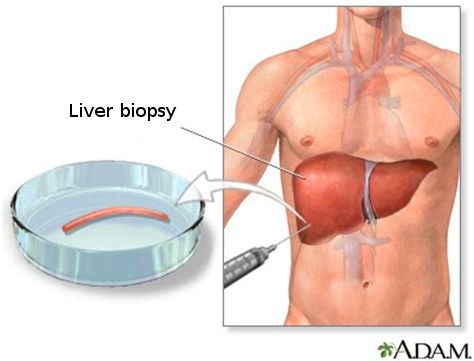
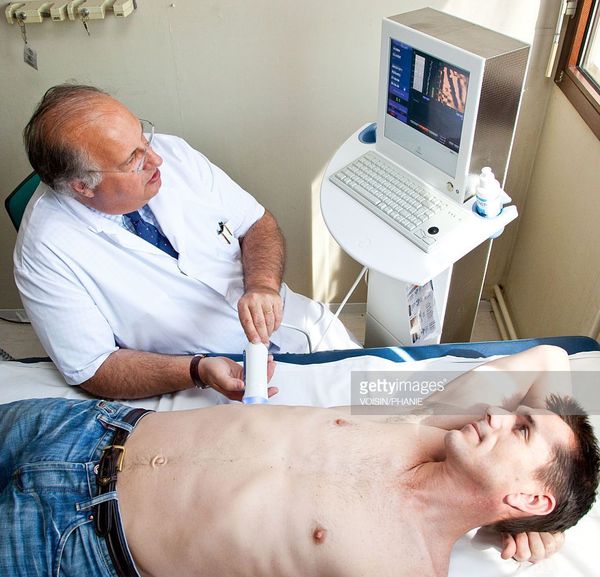
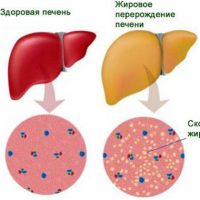
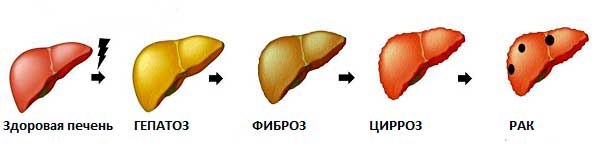
гипертрофия печени что это такое и как лечить
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, врача общей практики со стажем в 14 лет.
Определение болезни. Причины заболевания
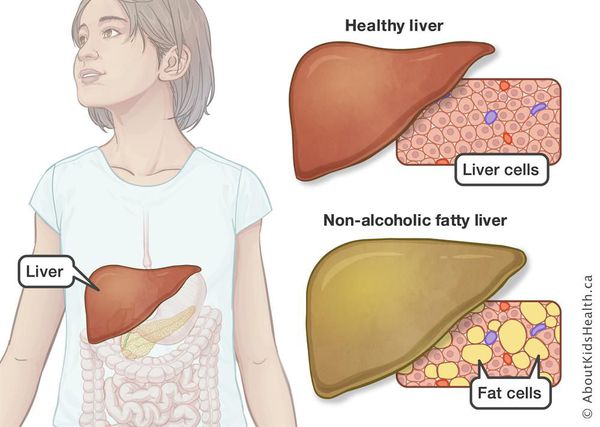
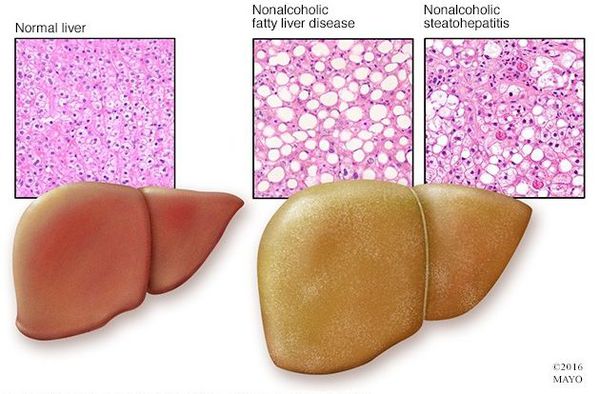
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
Все эти изменения неуклонно приводят к:
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
Основными причинам развития НАЖБП являются: [11]
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
У 50-75% больных могут появляться симптомы общей (хронической) усталости, снижение работоспособности, недомогание, слабость, тяжесть в области правого подреберья, набор веса, длительное повышение температуры тела без всякой причины, красные точки на коже в области груди и живота. Печень часто увеличена. Возникают расстройства пищеварения, повышенное газообразование, кожный зуд, редко — желтуха, «печёночные знаки».
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
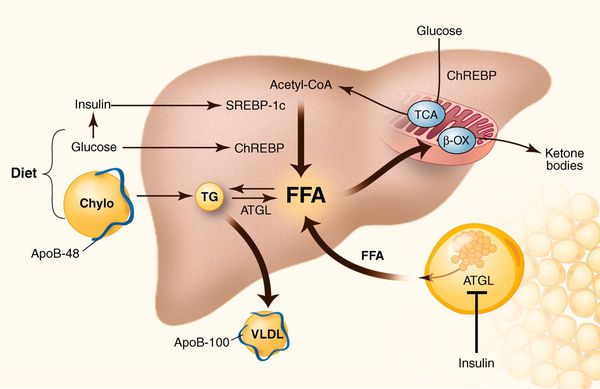
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
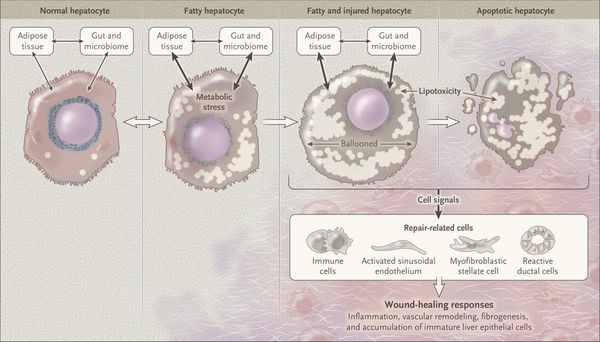
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
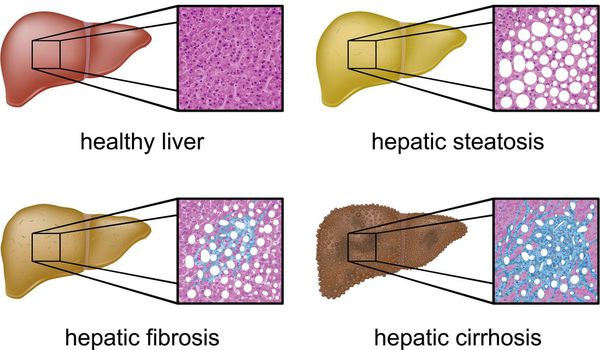
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
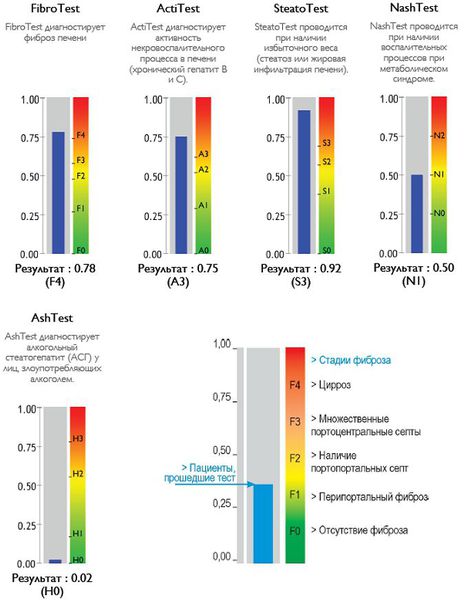
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
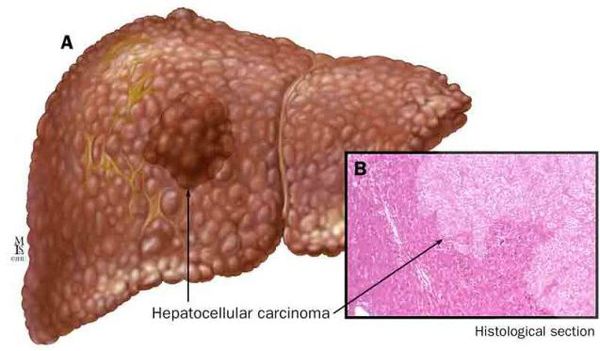
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Неалкогольная жировая болезнь печени (НАЖБП)
Термин «неалкогольная жировая болезнь печени» впервые сформулировал в 1980 году J.Ludwig et al., который изучал характер изменений в печени больных ожирением и сахарным диабетом 2 типа. У этих больных не было в анамнезе указаний на прием алкоголя в токсических для печени дозах и вирусных поражений печени, но при морфологическом исследовании были выявлены признаки патологического накопления жира внутри – и внеклеточно — в клетках печени (гепатоцитах).
Часто пациенты проходят ультразвуковое исследование органов брюшной полости и в заключении у них выявляются диффузные изменения печени, которые специалисты ультразвуковой диагностики называют или стеатоз, или жировая дистрофия печени, или гепатоз, но правильнее их называть неалкогольная жировая болезнь печени (НАЖБП). Так, что же все-таки это такое, и должны ли встревоженные пациенты идти к врачу?
Следует отметить, что стеатоз (накопление жира) — это первый признак поражения печени, какая бы причина не была установлена в дальнейшем. Стеатоз является обратимым процессом. Поэтому пройти обследование у врача, установить причину, получить рекомендации и не допускать прогрессирования болезни печени (НАЖБП – НАСГ (неалкогольный стеатогепатит) — НАСГ с фиброзом – цирроз) необходимо.
В России впервые была проведена статистическая оценка распространенности НАЖБП в 2007 году и показала, что она составляет 26.1% населения.
Причины возникновения заболевания
НАЖБП может выступать:
На неё оказывают токсическое воздействие:
В течение НАЖБП имеют большое значение состояние образование и выделение желчи печенью, т. к. с ней снижаются триглицериды из клеток печени. Причиной прогрессирования заболевания может быть состояние микрофлоры в кишечном тракте и возникновение эндотоксинов, которые нарушают кишечно-печеночную циркуляцию и нарушают, прежде всего, детоксикационную функцию печени и вызывают воспалительный процесс — неалкогольный стеатогепатит.
Клинические проявления НАЖБП
Неалкогольная жировая болезнь печени характеризуется бессимптомным течением, отсутствием жалоб со стороны печени у человека.
Выявление изменений печени обычно связано с обращениями пациентов за врачебной помощью по поводу других причин. Обычно – повышение сахара, артериальная гипертония, ожирение, проявления ишемической болезни и др. и реже — по поводу дискомфорта и тяжести в правом подреберье.
Могут наблюдаться диспепсические явления – отрыжка, тошнота, вздутие живота, неустойчивый стул и др.
Иногда наблюдаются неспецифические симптомы — повышенная утомляемость, слабость, ноющая боль в области правого подреберья без четкой связи с приемом пищи.
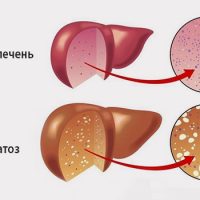
НАЖБП является диагнозом исключения прежде всего злоупотребления алкоголем и вирусных гепатитов В, С, Д, ТТV. И хотя мы говорим о бессимптомном течении болезни, опыт показывает, что 30% пациентов имеют жалобы, около 50% — увеличение печени и некоторое ее уплотнение.
Неалкогольная жировая болезнь печени. Диагностика
Анамнез: исключить злоупотребление алкоголем, инфекционную природу поражения печени. Проанализировать образ жизни человека- переедание, несбалансированное питание, недостаток физической активности, экологические факторы, прием лекарств.
Лабораторные исследования
Печеночные пробы: АЛТ и АСТ, гамма-ГГТ, ЩФ, билирубин, холестерин и фракции, альбумин, протромбиновый индекс, сахар крови, мочевая кислота, уровень инсулина.
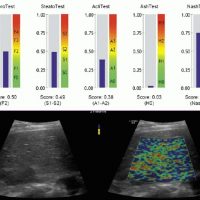
Наличие трех признаков ультразвукового исследования при отсутствии данных употребления алкогольных напитков и исключения других хронических заболеваний печени позволяет точно верифицировать НАЖБП.
Эластометрия
При прогрессировании НАЖБП важна информация о уровне фиброза (замещении клеток печени соединительной тканью), которую возможно получить при Эластометрии, которая неивазивным способом позволяет установить наличие или отсутствие фиброза в печени. Этот метод практически заменяет ранее проводившуюся биопсию печени.
Лечение НАЖБП
Лечение основывается на устранении причин и факторов риска возникновения заболевания и предупреждении прогрессирования процесса в печени, лечении заболеваний, вызывающих жировой гепатоз. Лечение включает в себя коррекцию образа жизни и использования фармакологических средств.
Питание и коррекция образа жизни

Рекомендуется снизить употребление углеводов, ограничить, но не исключать полностью животные и растительные жиры, потреблять достаточное количество овощей, фруктов для обогащения пищи витаминами и пищевыми волокнами, клетчаткой, липотропными веществами, содержащимися в твороге и кашах, бобовые, яйца, орехи и семена, морскую рыбу, сою и др. продукты.
Предупреждение! Если быстро снижать массу тела, то это приводит к ухудшению течения заболевания.
При начальных стадиях НАЖБП при нормальных показателях печеночных проб достаточно соблюдение ограничений в питании углеводов, жиров, отказ от алкоголя и консервированной пищи, некоторых медикаментов, контроль за массой тела, состоянием обмена углеводов, холестерина, мочевой кислоты. Обязательны физические нагрузки!
Медикаментозное лечение
Медикаментозное лечение назначается со стадии стеатогепатита (НАСГ), и применяются препараты различных фармакологических групп. Лечение осуществляется врачом с учетом индивидуального подбора препаратов, длительности и дозирования их. Наблюдение за такими больными производится 1 раз в 3-6 месяцев.
В течение года возможно провести 2-3 курса.
Назначение липотропных средств при жировой болезни печени, особенно препаратов эссенциальных фосфолипидов и содержащих желчные кислоты, может являться «терапией прикрытия» побочных эффектов коррекции метаболических нарушений в организме, а также токсического воздействия на печень лекарственных препаратов.
Неалкогольная жировая болезнь печени. Прогноз
Наблюдение за пациентами проводится разными специалистами в соответствии с имеющимися у человека болезнями (терапевт, кардиолог, эндокринолог, гастроэнтеролог) с обязательным контролем печеночных проб. Важной частью наблюдения являются лечебно-профилактические мероприятия тех заболеваний, которые вызывают НАЖБП – контроль питания, физических нагрузок, назначение курсов липотропных средств.
Прогноз заболевания зависит от своевременного устранения причинного фактора и лечения основных метаболических болезней.
Увеличение печени: причины, симптомы, лечение
Роль печени в организме человека трудно переоценить. К ее функциям относятся и обезвреживание чужеродных веществ в организме, и удаление избытка гормонов, хранение энергетических резервов и витаминов, а также участие в кроветворении и многое другое. Поэтому проблемы, возникающие при заболеваниях печени, касаются всего организма в целом.
Какие болезни опасны для печени, как они появляются и чем лечатся, рассказал Аганин Марк Анатольевич, инфекционист, врач высшей категории медицинского центра «Медлайн».
Марк Анатольевич, в чем может быть причина увеличения печени?
— Вообще, само по себе увеличение печени это всего лишь симптом заболевания. Необходимо в первую очередь выяснять причину заболевания, а потом устранять ее.
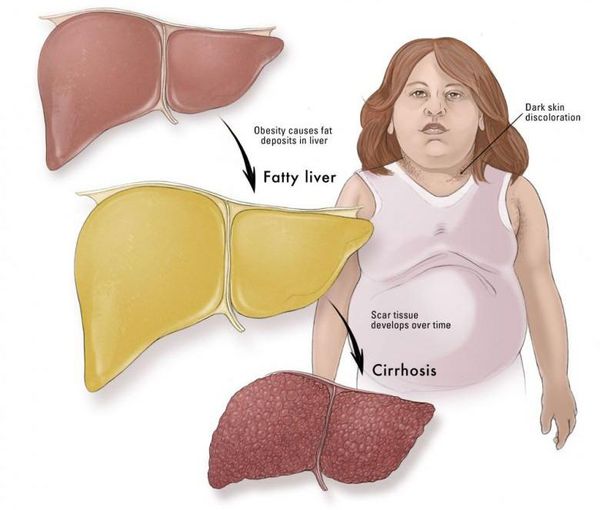
Болезни, способствующие увеличению печени — это цирроз и жировой гепатоз (ожирение печени).
Эти болезни являются хроническими, вызываются разными факторами, в том числе нарушением питания, злоупотреблением алкоголя либо инфекционными вирусными гепатитами.
Есть ли симптомы, по которым можно понять, что у человека увеличена печень?
— Специфических симптомов как таковых нет. Могут быть неспецифические, например, неприятные ощущения или ощущение инородного тела в правом боку, колющие ощущения в правом подреберье, изжога, отрыжка, неприятный привкус во рту, нарушение, разжижение стула, потемнение мочи. Все эти признаки могут свидетельствовать не только о заболевании печени, но и о совсем других болезнях.
Как диагностировать болезни?
— Диагностика проходит с помощью инструментальных и лабораторных методов, среди которых биохимический анализ крови, УЗИ брюшной полости и печени. Это основное.
Из вспомогательных методов — исследования на антитела к возбудителям вирусных гепатитов, компьютерная томография печени и другие углубленные методы.
В чем заключается лечение?
— Одна из самых частых причин болезней печени — это вирусные гепатиты. В этом случае назначается противовирусная терапия.
Если это токсический, алкогольный гепатит, то нужен отказ от алкоголя, медикаментозная поддержка и диета.
При жировом гепатозе, связанном с избытком массы тела, назначаются меры, направленные на снижение избытка массы тела, диета, медикаментозное лечение, хирургическое вмешательство в случае необходимости.
В случае циррозов, то есть уже более тяжелого поражения печени, лечение проходит более трудно, но оно возможно. В первую очередь, терапия направлена на устранение причин цирроза.
Следующим этапом будет лечение различными медикаментозными средствами, которые позволяют печени более оптимально функционировать. Ну и крайним методом лечения цирроза является трансплантация (пересадка) печени.
Есть ли какие-то меры по предотвращению болезней печени?
— Отказ от пагубного употребления алкоголя — одна из важнейших и эффективнейших мер в борьбе с заболеваниями печени.
Второе, это рацион, который не должен быть со слишком большим преобладанием жиров и легкоусвояемых углеводов.
Нужно контролировать свою массу тела, не допускать ее рост сверх нормы.
Профилактикой так же будет предохранение презервативом во время полового акта, потому что гепатиты B и C передаются в том числе половым путем.
Необходимо отказаться от употребления наркотиков, связанного с очень высоким риском заражения вирусными гепатитами, так как кровь — это еще один путь их передачи.
Кроме того, против гепатита В существует прививка, которую я рекомендую поставить всем.
Какие случаи из практики, связанные с болезнью печени, вам запомнились?
— Тяжелые поражения печени бывают при вирусном гепатите, когда человек долгое время не знал, что у него вирус, например, гепатита С. Этот гепатит долгие годы может протекать бессимптомно, в итоге приводя к циррозу печени.
То есть человек жил нормальной жизнью и вдруг у него начались проявления цирроза. При дальнейшем обследовании выяснилось, что функции печени пациента нарушены, болезнь уже на серьезной стадии, и человеку лежит дорога на операционный стол, на трансплантацию. Приходится бороться с таким циррозом, и речь уже идет о выживании, а не об излечении.
Что может сделать человек для того, чтобы не упустить болезни?
— Общий анализ крови не способен выявить проблемы с печенью. Есть точечные, скрининговые методы исследования.
Раз в год я бы рекомендовал делать тест на антитела к гепатиту С, гепатиту В, и биохимический анализ крови по двум показателям — АЛТ и АСТ. Ну и нужно следить за весом, за физической активностью, за диетой.
Сосудистые заболевания печени
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=825%2C550&ssl=1″ />
Заболевания сосудов печени — относительно редкие болезни, при них может нарушаться кровоток в печени, что приводит к ряду серьезных осложнений. В этой статье рассматриваются основные вопросы, связанные с патогенезом, клинической картиной и лечением.
Обструкция печеночной артерии
Определение
Это осложнение множества различных патологических состояний, приводящих к частичному или полному нарушению кровотока по этому сосуду.
Эпидемиология
Обструкция печеночной артерии встречается относительно редко и точных эпидемиологических данных по этому поводу нет. Тромбоз печеночной артерии, приводящий к обструкции, может быть осложнением (примерно 2% трансплантатов печени).
Патогенез
Обструкция печеночной артерии может быть вызвана атеросклерозом, тромбозом, эмболией, инфильтрацией печени или травмой. Это происходит в ходе истинной полицитемии, узелкового артериита, эндокардита и, как упоминалось выше, у небольшого процента пациентов после трансплантации печени.
Непроходимость может возникнуть в результате:
Клиническая картина
У многих пациентов обструкция печеночной артерии протекает бессимптомно и выявляется только при вскрытии. Из-за двойной васкуляризации печени, окклюзия просвета печеночной артерии, не является синонимом инфаркта печени (эмболизация печеночной вены, является, признанным методом лечения рака печени).
Тем не менее, одновременная и полная непроходимость печеночной артерии и воротной вен, почти всегда заканчивается летальным исходом. Клинически инфаркт печени проявляется болью в правой верхней части живота, тахикардией и падением артериального давления. В редких случаях может развиться острая печеночная недостаточность.
Диагностика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%94%D0%B8%D0%B0%D0%B3%D0%BD%D0%BE%D1%81%D1%82%D0%B8%D0%BA%D0%B0-1.jpg?resize=450%2C300&ssl=1″ alt=»Диагностика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Диагностика
Лабораторные исследования показывают повышение активности трансаминаз и увеличение протромбинового времени. Визуализирующие тесты играют важную роль в диагностике:
Допплерография
В случае тромбоза печеночной артерии, после трансплантации печени, клинические симптомы обычно появляются в течение нескольких дней после сеанса, а тесты показывают быстрое повышение активности трансаминаз и усиление холестаза. Это связано с быстро прогрессирующей ишемией желчевыводящих путей.
Пациентам с трансплантацией печени проводится тромбэктомия или повторная трансплантация. При окклюзиях другой этиологии может применяться тромболитическая терапия (стрептокиназа или рекомбинантный активатор плазминогена), или антикоагулянтная терапия (гепарин).
Тромбоз воротной вены
Кровоток в воротной вене может быть нарушен в результате тромбоза или инфильтрации опухоли. Клинически тромбоз воротной вены подразделяется: на острый и хронический. Этиология обоих состояний схожа, хроническая форма,- это чаще все продолжение острой формы. Однако методы лечения у них разные.
Факторы риска
Факторы риска тромбоза воротной вены обычно подразделяются на местные и общие. Наиболее частые местными факторы риска: рак брюшной полости и цирроз печени.
Тогда как наиболее распространенные общие факторы риска — это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции. Следует помнить, что диагностика местной причины тромбоза воротной вены не исключает одновременного наличия одной или нескольких общих причин.
Тромбоз воротной вены при миелопролиферативном синдроме
Тромбоз воротной вены — это клинический симптом миелопролиферативного заболевания. Поскольку портальная гипертензия приводит к отклонениям в анализе крови, (таким как анемия и тромбоцитопения), у большинства пациентов нет изменений в периферической крови, характерных для миелопроферативного синдрома, поэтому, диагноз расширяется до определения мутации гена JAK2 (киназа Януса 2 типа) и в таких ситуациях биопсия костного мозга находит полное оправдание.
Дифференциация
В соответствии с рекомендациями Американской ассоциации по изучению заболеваний печени, при диагностике тромбоза воротной вены на основании визуализационных исследований (УЗИ, КТ, в первую очередь следует исключить следующее:
Клинические формы
Острый тромбоз воротной вены — это внезапное образование сгустка частично или полностью закупоривающего воротную вену.
Клиническая картина
Выраженность клинических симптомов зависит от степени окклюзии воротной вены. Острый тромбоз проявляется:
Диагностика
Лабораторные тесты
Лабораторные исследования показывают увеличение показателей острой фазы. Чаще всего сохраняется функция печени, что объясняется компенсаторным кровотоком из печеночной артерии и коллатеральным кровообращением по мелким венозным сосудам в воротах печени. Однако, у некоторых пациентов наблюдается умеренное повышение уровня трансаминаз.
Визуальные исследования
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%92%D0%B8%D0%B7%D1%83%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5-%D0%B8%D1%81%D1%81%D0%BB%D0%B5%D0%B4%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F.jpg?resize=450%2C300&ssl=1″ alt=»Визуальные исследования» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Визуальные исследования
Визуальная диагностика имеет решающее значение для постановки диагноза:
Фармакотерапия
Антикоагулянтное лечение. Методом выбора является быстрое введение низкомолекулярного гепарина, предотвращающего инфаркт кишечника и значительно улучшает прогноз. Терапия пероральными антикоагулянтами (варфарин или не так часто, применяемый аценокумарол) возможна, если клиническое состояние пациента стабильно и хирургическое вмешательство не планируется.
Консервативное лечение дает шанс полной реканализации сосуда примерно у 40% пациентов. Оно должно длиться не менее 3 месяцев, хотя следует отметить, что полное восстановление тромбоза наблюдалось даже после 6 месяцев терапии. В случаях тромбофилии, для которой не существует радикальной терапии, антикоагулянтное лечение, скорее всего, следует использовать до конца жизни.
Антимикробное лечение. При появлении признаков инфекции требуется антибактериальная терапия.
Инвазивное лечение. Инвазивные процедуры, такие как: тромболизис стрептокиназой или тканевым активатором плазминогена, вводимыми непосредственно в воротную вену или в верхнюю брыжеечную артерию, не показывают более высокой эффективности, чем антикоагулянты, и имеют гораздо более высокий риск серьезных осложнений.
Конечно, в случае инфаркта кишечника, методом выбора будет хирургическая резекция некротических фрагментов кишечника. Это лечение можно сочетать с удалением сгустка из просвета сосуда.
Хронический тромбоз воротной вены
Это клиническое состояние, при нем в результате тромбоза воротной вены развивается коллатеральное кровообращение, соединяющее вены до и после сгустка, образуя сеть сосудов, известную как кавернозная трансформация.
Клиническая картина
Чаще всего хронический тромбо, диагностируется при поиске причины симптомов портальной гипертензии, проявляющейся кровотечением из варикозно расширенных вен пищевода или увеличением селезенки. Пациенты с хроническим тромбозом воротной вены переносят кровотечение из варикозно расширенных вен пищевода лучше, чем пациенты с циррозом, что в основном связано с хорошо сохраненной функцией печени.
Иногда сеть сосудов кавернозной трансформации может сужать желчные протоки, что приводит к портальной билиопатии, приводящей к симптомам холестаза и холангита. Иногда трудно отличимым от первичного склерозирующего холангита.
Физикальное обследование показывает характерное расширение поверхностных сосудов брюшной полости. Минимальная энцефалопатия наблюдается примерно у половины пациентов с хроническим тромбозом, что, однако, может ухудшить точность или способность управлять автомобилем.
Диагностика
Биохимия печени обычно в норме. Визуализирующие исследования, такие как УЗИ, КТ или МРТ, показывающие многочисленные коллатеральные сосуды в области воротной вены и невидимый (неконтрастный) фрагмент воротной вены, играют решающую роль в диагностике, (как при остром тромбозе). Иногда при допплеровском исследовании коллатеральные сосуды имитируют воротную вену, увеличение поджелудочной железы или опухоль желчевыводящих путей.
Нет хорошо задокументированных исследований эффективности бета-адреноблокаторов для первичной профилактики или бандажирования, при вторичной профилактике кровотечения из варикозно расширенных вен пищевода у пациентов с тромбозом воротной вены.
Аналогичная проблема существует при лечении этих пациентов антикоагулянтами. Кажется логичным, сначала лечить варикозное расширение вен пищевода с помощью бандажа пациентам, у которых был эпизод кровотечения, а затем начать антикоагулянтную терапию. Имеются сообщения о том, что хроническая антикоагулянтная терапия снижает риск рецидива тромбоза, без увеличения риска кровотечения из варикозного расширения вен. Пациентам с развивающимся симптомом портальной билиопатии, осложненной холангитом, оправдан эндоскопический стеноз.
Прогноз
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=480%2C320&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D0%B3%D0%BD%D0%BE%D0%B7.jpg?resize=450%2C300&ssl=1″ alt=»Прогноз» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?w=480&ssl=1 480w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Прогноз
Типичные осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии — это редкая причиной смерти у пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Тромбоз воротной вены у пациентов с циррозом печени
Тромбоз воротной вены у пациентов с циррозом печени коррелирует со степенью декомпенсации органа.Тромбоз может развиться у 1/4 пациентов, требующих трансплантации печени. Рак печени может быть причиной тромбоза у пациентов с циррозом.
Клиническая картина
Наиболее частые клинические симптомы тромбоза:
В этой группе чаще выявляются мутации фактора V Лейдена, гена протромбина или метилентетрагидрофолатредуктазы (MTHFR), чем у пациентов с циррозом печени без тромбоза.
К сожалению, никаких рекомендаций по лечению антикоагулянтами у этих пациентов не разработано. Рекомендуется принимать индивидуальные решения. Однако, у подавляющего большинства пациентов, ожидающих трансплантации печени, после начала антикоагулянтной терапии воротная вена восстанавливается.
Тромбоз воротной вены после трансплантации печени
Это осложнение может возникнуть у 2-3% пациентов и часто связано с разницей в диаметре воротной вены донора и реципиента, а также со спленэктомией, выполняемой во время операции по трансплантации.
Синдром обструкции синуса печени
Определение
Это процесс, нарушающий кровообращение в печени в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи печени. У некоторых пациентов в этот процесс также вовлекаются центральные вены.
Эпидемиология
В развитых странах синдром синусоидальной обструкции (SOS), ранее называвшийся (VOD) веноокклюзионная болезнь, является наиболее частым осложнением абляции костного мозга, при его подготовке к трансплантации, (в этом контексте, следует использовать термин — трансплантация гемопоэтических стволовых клеток). Острая обструкция синуса печени — это третья по значимости причина смерти пациентов, перенесших трансплантацию костного мозга.
Другие причины SOS включают:
Клиническая картина
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9A%D0%BB%D0%B8%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F-%D0%BA%D0%B0%D1%80%D1%82%D0%B8%D0%BD%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Клиническая картина» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Клиническая картина
Клинические симптомы могут имитировать синдром Бадда-Киари и включают наиболее распространенные:
Выделяют три степени тяжести симптомов: легкую, среднюю и тяжелую.
Если заболевание стало результатом применения циклофосфамида, первые признаки появляются через 10-20 дней после начала лечения. При других схемах миелоабляции симптомы могут развиться позже. На практике синдром обструкции синусовых сосудов печени диагностируется у пациентов:
Диагностика
Балтиморские критерии
Балтиморские критерии полезны при постановке диагноза. Синдром обструкции печеночного синуса подтверждается при соблюдении следующих условий:
Дифференциация
Дифференциальный диагноз должен включать:
Дополнительные исследования
В сомнительных случаях диагноз подтверждается если:
При допплеровском исследовании печеночных сосудов можно наблюдать изменение направления кровотока в воротной вене.
Профилактика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D1%84%D0%B8%D0%BB%D0%B0%D0%BA%D1%82%D0%B8%D0%BA%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Профилактика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Профилактика
Для профилактики закупорки сосудов синуса печени используются менее агрессивные, чем стандартные схемы миелоаблативной терапии, с применением флударабина, более низкие дозы бусульфана или дозы облучения.
Наибольший риск закупорки сосудов синуса печени связан с назначением циклофосфамида и облучением в дозе> 12 гр. Смертность у пациентов с синдромом обструкции синуса печени, получавших такое лечение может составлять 15-20%.
Кроме того, в профилактике используются:
Руководящие принципы Американской ассоциации по изучению заболеваний печени (AASLD) не рекомендуют какие-либо из этих методов лечения, поскольку рандомизированные испытания не подтвердили их эффективность. Антикоагулянтная терапия, также может привести к опасным для жизни кровотечениям.
Симптоматическое лечение перегрузки жидкостью включает:
Из-за отсутствия достаточных данных не рекомендуется использовать дефибротид, тканевый активатор плазминогена или TIPS (трансъюгулярный внутрипеченочный портосистемный шунт).
Трансплантация печени может быть терапевтическим вариантом у пациентов с незлокачественными заболеваниями, например, аутоиммунными заболеваниями.
Прогноз
Плохой прогноз определяется:
Тромбоз печеночной вены (синдром Бадда-Киари)
Тромбоз печеночной вены (синдром Бадда-Киари)
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A2%D1%80%D0%BE%D0%BC%D0%B1%D0%BE%D0%B7-%D0%BF%D0%B5%D1%87%D0%B5%D0%BD%D0%BE%D1%87%D0%BD%D0%BE%D0%B9-%D0%B2%D0%B5%D0%BD%D1%8B-%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC-%D0%91%D0%B0%D0%B4%D0%B4%D0%B0-%D0%9A%D0%B8%D0%B0%D1%80%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Тромбоз печеночной вены (синдром Бадда-Киари)» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Тромбоз печеночной вены (синдром Бадда-Киари)
Определение
Нарушение кровотока, возникающее на любой стадии оттока крови из печени, от мелких печеночных вен, до места соединения главной вены с правым предсердием.
Разделение
Синдром Бадда-Киари делится на:
Причины
Клинически заболевание может иметь вид:
Существуют значительные расхождения между клинической картиной и длительностью тромбоза. Например, у пациентов с симптомами острого тромбоза очень часто встречаются признаки длительного заболевания, такие, как выраженный фиброз и цирроз.
Общие клинические симптомы включают:
Заболевание протекает бессимптомно примерно у 20% пациентов с развивающимся коллатеральным кровообращением.
Диагностика
Биохимические исследования
Биохимические тесты выявляют нарушения разной степени тяжести, в зависимости от клинического состояния. Асцитная жидкость имеет характеристики транссудата.
Изображение венозных сосудов
При допплеровском исследовании печеночные вены демонстрируют расширение в сочетании с отсутствием или изменением направления кровотока. Кроме того, могут быть расширенные коллатеральные сосуды, соединяющие печеночную вену с меж реберной и диафрагмальной венами. Магнитно-резонансная томография с контрастным веществом позволяет точно визуализировать обструкцию в просвете сосудов или источник внешнего давления на печеночные вены или нижнюю полую вену.
Гипертрофия хвостатой доли
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%93%D0%B8%D0%BF%D0%B5%D1%80%D1%82%D1%80%D0%BE%D1%84%D0%B8%D1%8F-%D1%85%D0%B2%D0%BE%D1%81%D1%82%D0%B0%D1%82%D0%BE%D0%B9-%D0%B4%D0%BE%D0%BB%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Гипертрофия хвостатой доли» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=825%2C550&ssl=1 825w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=768%2C512&ssl=1 768w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Гипертрофия хвостатой доли
У большинства пациентов с синдромом Бадда-Киари наблюдается увеличение хвостатой доли. Это связано с тем, что хвостатая доля имеет венозное соединение с нижней полой веной, независимо от печеночных вен. Таким образом, в случае обструкции печеночных вен, по хвостатому отростку протекает гораздо больше крови, что приводит к его компенсаторной гипертрофии.
Регенеративные узелки
У пациентов с синдромом Бадда-Киари все визуальные исследования могут показать макро регенеративные узелки, демонстрирующие усиление артериальной фазы, и могут морфологически напоминать гепатоцеллюлярную карциному.
Эти узелки имеют иную этиологию, чем регенеративные, при циррозе печени. Их дифференциация от гепатоцеллюлярной карциномы может быть трудной. Многочисленные небольшие узелки указывают на довольно доброкачественные поражения, в то время, как единичные, увеличивающиеся поражения, могут указывать на рак.
Патоморфологическое обследование
При типичных симптомах синдрома Бадда-Киари в биопсии печени нет необходимости, более того, зачастую она невозможна по техническим причинам (нарушения свертываемости, асцит). Гистопатологическое исследование показывает расширение пазух с признаками застоя и фиброза в центральной части долек. Иногда в крошечных венах можно увидеть сгустки крови.
Мероприятия по порядку:
Антикоагулянтное лечение
Согласно рекомендациям AASLD, во время диагностики синдрома Бадда-Киари следует начать антикоагулянтную терапию (низкомолекулярные гепарины), а затем перейти на пероральные антикоагулянты, поддерживая нормализованный индекс активности протромбина (INR) в диапазоне 2- 3. Только противопоказания или серьезные осложнения, дают право прекратить лечение антикоагулянтами.
Чрескожная ангиопластика
Ангиопластика и протезирование печеночной вены следует рассматривать у всех пациентов с симптомами, чьи результаты визуализационных исследований показывают, что такое вмешательство возможно, например, в случае сегментарного стеноза или тромбоза.
Если антикоагуляция не улучшается, рассматривается возможность портальной системной трансъюгулярной внутрипеченочной фистулы (TIPS), очевидно, с предварительным подтверждением проходимости воротной вены.
TIPS у пациентов с синдромом Бадда-Киари — технически, очень сложная процедура, иногда она требует введения проводника непосредственно из просвета нижней полой вены, поэтому выполняется только в нескольких медицинских центрах в мире.
Пересадка печени
Показанием к трансплантации печени может быть мгновенная недостаточность органов. Трансплантация также должна рассматриваться, когда хирургия портальной системной трансцервикальной внутрипеченочной фистулы невозможна или неэффективна.
Прогноз
Независимые прогностические факторы при синдроме Бадда-Киари — это компоненты шкалы Чайлда-Тюркотта-Пью. Прогноз для этого синдрома значительно улучшился за последнее десятилетие и часто больше зависит от прогрессирования основного заболевания, (например, миелодиспластического синдрома), чем от симптомов печеночной недостаточности. Около 80% пациентов выживают через пять лет после трансплантации печени.
Резюме
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A0%D0%B5%D0%B7%D1%8E%D0%BC%D0%B5.jpg?resize=450%2C300&ssl=1″ alt=»Резюме» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Резюме
Причиной обструкции печеночной артерии могут быть: атеросклероз, тромбоз, эмболия, инфильтрация печени, травмы, заболевания сосудов. Обструкция также может быть осложнением трансплантации печени.
Из-за двойной васкуляризации печени окклюзия печеночной артерии не является синонимом инфаркта органа. Визуализирующие исследования играют важную роль в диагностике: допплерография, компьютерная томография с контрастным веществом и магнитно-резонансная томография.
Тромбоз воротной вены подразделяется на острый и хронический. Оба состояния имеют схожую этиологию и чаще всего второе будет продолжением первого. Однако, методы лечения различаются. Наиболее частые факторы риска тромбоза воротной вены — это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции.
Общие осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии, являются редкой причиной смерти пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Синдром заложенности носовых пазух печени приводит к нарушениям кровообращения в ней, в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи.
Это наиболее частое осложнение миелоаблативного лечения при подготовке пациентов к трансплантации костного мозга.
Балтиморские критерии полезны в диагностике. Профилактика основана на менее агрессивных режимах миелоаблативной терапии, чем при стандартной терапии.
Тромбоз печеночных вен (синдром Бадда-Киари) может проявляться, как фульминантная, острая или хроническая печеночная недостаточность. В курс лечения входят: антикоагулянтная терапия, чрескожная ангиопластика, TIPS и трансплантация печени. Благодаря такому режиму лечения до 90% пациентов живут больше 5 лет.
Добавить комментарий Отменить ответ
Вы должны быть авторизованы, чтобы оставить комментарий.