гиперсенситивный пневмонит что это такое
Гиперчувствительный пневмонит: симптомы, диагностика, лечение
Аллергический альвеолит
Гиперчувствительный пневмонит (ГП), также известный как внешний аллергический альвеолит, является результатом не-IgE-опосредованного иммунологического воспаления. ГП вызван повторной ингаляцией нечеловеческого белка, который может иметь естественное растительное или животное происхождение, или может быть результатом химического конъюгата с белком человеческого белка, таким как альбумин. Воспаление при ГП проявляется в альвеолах и дистальных бронхиолах. Клинические проявления ГП зависят от концентрации и частоты воздействия.
Клинические синдромы — острый, подострый и хронический ГП — проявляются по-разному. Некоторые авторы сообщают, что существует только два клинических синдрома; однако они различаются в зависимости от того, группируются ли они с подострой, с острой или хронической формой. Многие случаи ГП вызваны профессиональным воздействием.
Этиология
Были идентифицированы множественные возбудители. Двумя наиболее часто встречающимися агентами являются бактерии (например, термофильные актиномицеты, ответственные за различные синдромы, включая «фермерское легкое», багасозз и легкие собирателя грибов) и белки животных (например, птичьи белки, ответственные за болезни, в том числе легкие заводчиков голубей, и болезнь любителей попугаев), а также воздействие крупных сельскохозяйственных животных.
Грибы были зарегистрированы как источники антигенов, и реактивные химические вещества, такие как ангидриды кислот (болезнь легких эпоксидной смолы), диизоцианаты и агенты, используемые при обработке металлов, также являются известными причинами синдромов ГП.
С начала XXI века в Великобритании воздействие металлообрабатывающей жидкости стало самой распространенной причиной профессионального ГП, на которое приходится около половины всех случаев. Ингредиенты, такие как нитрофурантоин, метотрексат, рокситромицин и ритуксимаб, могут вызывать синдром гиперчувствительного пневмонита, вызванный лекарственными средствами. Кроме того, в опубликованном отчете о заболевании описывается травяная добавка аюрведической медициной как причина ГП.
Патофизиология
Иммунопатогенные механизмы, которые приводят к характерному воспалению при ГП, не полностью поняты. Относительный вклад гуморального и клеточного ответа неясен. Потенциально важную роль клеточного адаптивного иммунитета как причины ГП подтверждается тем фактом, что у людей с гипогаммаглобулинемией может развиться ГП. Исследование бронхоальвеолярного лаважа у пациентов с симптоматическими ГП указывают на то, что важными клетками являются CD3 + Тлимфоциты, которые являются либо CD8 +, либо CD4 + с фенотипом Th1.
Воспаление при ГП имеет характерный, но не патогномоничный характер. Клеточный инфильтрат состоит в основном из лимфоцитов, плазматических клеток и нейтрофилов. Кроме того, имеются неказеозные гранулемы и активированные пенистые макрофаги. Воспаление имеет тенденцию быть бронхоцентрическим или бронхиолоцентрическим при распространении. На более поздних стадиях лимфоцитарный альвеолит менее выражен, и обычно возникает интерстициальный фиброз с утолщенными коллагеном бронхиальными стенками.
При остром ГП лихорадка, тахипноэ, одышка, легочные инфильтраты, рестриктивные отклонения функциональных легочных проб (ФЛП) и снижение диффузионной способности легких по монооксиду углерода (DLCO) вызваны лимфоцитарным альвеолитом.
В подострой фазе воспаление не так интенсивно, и часто наблюдается значительный фиброз, приводящий к бессимптомному развитию в течение многих недель недомогания, одышки, кашля, смешанных результатов дыхательной функции и уменьшенной DLCO.
Наконец, при хроническом ГП воспаление выражено мало; фиброз, который характеризует эту форму ГП, приводит к одышке, потере веса, недомоганию, смешанным результатам дыхательной функции и снижению DLCO.
Классификация
Рекомендации по клинической оценке гиперчувствительного пневмонита
- Острый (развивается через несколько часов после воздействия) Подострый (развивается в течение недель и месяцев после воздействия) Хронический (развивается через месяцы и годы после воздействия).
Первичная профилактика
Первичная профилактика заключается в уменьшении воздействия окружающей среды на антигены, которые могут вызвать ГП; например, фермеры теперь используют системы вентиляции и осушения, чтобы значительно снизить вероятность того, что термофильные бактерии будут расти в сене в зимний период. Это экологическое вмешательство значительно снизило распространенность синдрома «фермерского легкого» среди фермеров молочных ферм.
Диагностика
С начала XXI века в Великобритании воздействие металлообрабатывающей жидкости стало самой распространенной причиной профессионального ГП, на которое приходится около половины всех случаев. Ингредиенты, такие как нитрофурантоин, метотрексат, рокситромицин и ритуксимаб, могут вызывать синдром гиперчувствительного пневмонита, вызванный лекарственными средствами. Кроме того, в опубликованном отчете о заболевании описывается травяная добавка аюрведической медициной как причина ГП.
У меньшего количества пациентов, особенно с хроническим ГП, анамнез обследований не всегда доступен. Особенно важными являются непредвиденные скрытые воздействия, такие как подушки / или пуховые одеяла, или плесень под половицами.
Единственным тестом для выявления патогномоничных признаков служит ингаляционная провокационная проба, хотя она и является потенциально опасной для здоровья. Подтверждающие исследования демонстрируют высокий титр антител к потенциальному антигену, аномальные результаты рентгенографии/КТ органов грудной клетки и аномальные показатели функциональных легочных проб (ФЛП).
Бронхоальвеолярный лаваж может быть необходим, если диагноз неясен: например, хронический ГП. Однако, если есть анамнез временного связывания антигена и положительного осаждения этого антигена, и улучшение с удалением из предполагаемого антигена, бронхоальвеолярный лаваж обычно не выполняется.
Биопсия и ингаляционний тест как исследования при ГП обычно не выполняются из-за их инвазивного характера. Однако хирургическая биопсия легких иногда необходима в случаях с атипичными особенностями или отсутствием анамнеза воздействия. Типичные гистологические особенности включают бронхоцентрический инфильтрат, состоящий из лимфоцитов, плазматических клеток, нейтрофилов, пенистых макрофагов и не казеозных гранулем. На более поздних стадиях преобладает интерстициальный фиброз.
Клиническая оценка
Клинический анамнез, симптомы и признаки зависят от того, является ли ГП острым, подострым или хроническым. В остром случае речь идет о гриппоподобной болезни, включая лихорадку, озноб, недомогание, непроизводительный кашель и одышку, начинающуюся через 6-18 часов после острого, высокого уровня воздействия, с двусторонними хрипами при обследовании. Подострое заболевание характеризуется недомоганием, одышкой и продуктивным кашлем в течение недель и месяцев.
При хроническом ГП клиника напоминает идиопатический фиброз легких, характеризуется развитием одышки, продуктивным кашлем и потерей веса из-за низкоуровневого воздействия, возникающего в течение многих месяцев или даже лет, и диффузными хрипами при аускультации. При хроническом заболевании может также быть изменения пальцев. Рецидивирующее гриппоподобное заболевание или интерстициальное заболевание легких должны повышать высокий индекс подозрительности относительно ГП.
Лабораторные методы
ОАК, СОЭ и альбумин имеют ограниченную ценность, но могут указывать на воспалительный процесс и / или хроническое заболевание. В острых условиях могут появляться неспецифические признаки, такие как повышенная СОЭ и лейкоцитоз со сдвигом влево. При хронических состояниях часто встречаются неспецифические признаки, такие как низкий альбумин и анемия. Осаждающие антитела являются подтверждающими.
Визуализационные методы
Рентгенография органов грудной клетки при остром и подостром заболевании обычно характеризуется неоднородными, узловыми инфильтратами, а при хроническом ГП — фиброзом.
При хроническом заболевании проводится компьютерная томография высокого разрешения, которая демонстрирует ослабление затухания в виде матового стекла и пятнистые микронодулы фиброза преимущественно в верхних долях.
Физиологические методы
ППФ обычно являются аномальными, демонстрируя либо рестрикцию, либо обструкцию, либо и то, и другое, а диффузионная способность легких по монооксиду углерода (DLCO) снижается при острых и хронических процессах. В случаях, когда диагноз может быть неясным (например, хронический ГП), бронхоальвеолярный лаваж может потребоваться для подтверждения диагноза или исключения различий.
Дифференциальная диагностика
Диагностические критерии
Диагностические критерии Terho
- Основные критерии:
- Воздействие известных причин ГП Совместимый анамнез одышки, кашля и недомогания Инфильтраты на рентгенограмме ОГК
Второстепенные критерии:
- Хрипы при осмотре Аномальные показатели функциональных легочных проб; рестриктивные нарушения Снижение диффузионной способности легких по монооксиду углерода (DLCO) Гистологические изменения при биопсии (обычно не выполняется) Положительная ингаляционная проба (обычно не выполняется).
Лечение
Важнейшим элементом любого аллергического заболевания легких является избегание этиологического антигена. В случае профессионального контакта, избегание человеком экспозиции обычно означает переназначение рабочего места. Тем не менее, экологические вмешательства, такие как снижение влажности и улучшение вентиляции, могут привести к достаточно низкому воздействию антигена, чтобы избавиться от необходимости переназначения.
В случае воздействия, не связанного с профессиональной деятельностью, экологическое вмешательство, как правило, является лучшим решением; примеры включают очистку заплесневелого пространства.
Фармакотерапия
Существует несколько исследований фармакологической терапии для ГП. Пероральные кортикостероиды обычно вводятся при острых и под-острых формах, потому что есть сообщения об улучшении симптомов и легочной функции. С предотвращением контакта с антигеном кортикостероиды можно сузить примерно до 6 недель. Пациентам с хроническим ГП может потребоваться длительная низкодозная терапия кортикостероидами.
Гиперчувствительный пневмонит
(экзогенный аллергический альвеолит)
, MD, MAS, University of Colorado Denver
Этиология
Более 300 антигенов способны вызывать гиперчувствительный пневмонит, хотя антигены, встречающиеся у фермеров, птицеводов, а также при загрязнении воды, составляют 75% случаев его возникновения.
Антигены обычно классифицируются по типу и роду занятий пациента ( Примеры гиперчувствительного пневмонита Примеры гиперчувствительного пневмонита Гиперчувствительный пневмонит – это синдром, включающий кашель, одышку, усталость и вызванный сенсибилизацией и последующей гиперчувствительностью к экзогенным (часто профессиональным) антигенам. Прочитайте дополнительные сведения 
Патофизиология
Циркулирующие преципитины (антитела к антигену) не играют первичной этиологической роли, а наличие аллергических заболеваний в анамнезе (бронхиальной астмы или сезонных аллергий) не является предрасполагающим фактором. Курение задерживает или предотвращает развитие заболевания, возможно, вследствие снижения иммунного ответа легких на ингаляционные антигены. Однако курение может вызвать обострение заболевания при установленном диагнозе.
Гиперчувствительный пневмонит имеет клинические сходство с другими расстройствами, которые имеют отличную патофизиологию.
Например, токсический синдром органической пыли (легочной микотоксикоз, зерновая лихорадка) представляет собой синдром, проявляющийся лихорадкой, ознобом, миалгией, а также диспноэ, что не требует предварительной сенсибилизации и, как полагают, вызван вдыханием токсинов, продуцируемых грибами или другими загрязняющими веществами органической пыли.
Профессиональная бронхиальная астма Профессиональная бронхиальная астма Профессиональная бронхиальная астма – это обратимая обструкция дыхательных путей, которая развивается при постепеннной (от нескольких месяцев до нескольких лет) сенсибилизации к аллергену на. Прочитайте дополнительные сведения вызывает появление одышки у лиц, сенсибилизированных к вдыхаемому антигену, но другие проявления, в частности обструкция дыхательных путей, эозинофильная инфильтрация и различия триггерных антигенов, позволяют дифференцировать ее от гиперчувствительного пневмонита.
Клинические проявления
Жалобы и симптомы зависят от того,
Только у небольшой части лиц, подвергшихся воздействию, развиваются симптомы, и в большинстве случаев – только по прошествии нескольких недель или месяцев воздействия и сенсибилизации.
Острый гиперчувствительный пневмонит
Острая форма заболевания встречается у ранее сенсибилизированных людей, которые контактировали с антигеном в высокой концентрации, и проявляется лихорадкой, ознобом, кашлем, сильным чувством стеснения в груди с двух сторон (подобно как при астме) и одышкой от 4 до 8 часов после воздействия. Могут также присутствовать анорексия, тошнота и рвота. При объективном обследовании выявляют тахипноэ, диффузные мелко- или среднепузырчатые инспираторные хрипы; почти у всех пациентов отсутствуют сухие хрипы.
Хронический пневмонит гиперчувствительности
Подострый гиперчувствительный пневмонит
Подострый вариант заболевания является промежуточным между острым и хроническим вариантами и проявляется кашлем, одышкой, недомоганием и анорексией, развивающимися в промежуток времени от нескольких дней до нескольких недель, или наложением острых симптомов на хронические.
Диагностика
Рентгенография органов грудной клетки и КТ высокого разрешения (КТВР)
Исследование функции легких
Гистологическое исследование и серологическая диагностика
Характерные признаки в истории включают в себя:
Повторяющиеся атипичные пневмонии
Появление симптома после смены места работы или жительства
Горячая ванна, сауна, бассейн, или другие источники стоячей воды, или плохое качество воды в доме, или регулярный контакт с ними в других местах
Содержание птиц в качестве домашних животных
Обострение и облегчение симптомов в связи с конкретными условиями или без них
Обследование часто не оказывает помощи в постановке диагноза, хотя могут выслушиваться хрипы и наблюдаться утолщения концевых фаланг пальцев по типу «барабанных палочек».
Методы визуализации
Лучевые исследования обычно выполняют пациентам, имеющим характерный анамнез и клинические проявления.
Рентгенография органов грудной клетки не является ни чувствительной, ни специфичной при диагностике заболевания и часто не показывает никаких отклонений у пациентов с острой и подострой формой заболевания. Это может проявляться в виде ретикулярных или узелковых затемнений, обычно при наличии симптомов. В хронической стадии более вероятно усиление легочного рисунка или очаговые затемнения в верхних отделах легких наряду с уменьшением объема легких и формированием «сотового легкого», как при идиопатическом легочном фиброзе.
Патологические изменения чаще обнаруживаются при выполнении КТ высокого разрешения, которая считается стандартом для оценки паренхиматозных изменений при гиперчувствительном пневмоните. Наиболее типичным результатом при КТВР во время острой и подострой стадии болезни является наличие профузных, плохо определяемых центролобулярных микроузелков. Иногда затемнение по типу «матового стекла» является преобладающим или единственным изменением. Данные затемнения обычно диффузные, но иногда не затрагивают периферические отделы вторичных долек легкого. Очаговые зоны повышенной интенсивности, подобные тем, которые присутствуют при облитерирующем бронхиолите, могут быть выраженным признаком у некоторых пациентов (например, мозаичное ослабление плотности легочного рисунка с задержкой воздуха на экспираторной КТВР).
Исследование функции легких
У всех пациентов с подозрением на гиперсенситивный пневмонит исследование функций легких Исследование функции легких (Overview of Tests of Pulmonary Function) При исследовании функции легких определяются скоростные и объемные показатели, показатели газообмена и функции дыхательных мышц. Основные функциональные легочные тесты, доступные в амбулаторных. Прочитайте дополнительные сведения должно проводиться как часть стандартных исследований. Заболевание может вызывать обструктивный, рестриктивный или смешанный тип нарушений. Терминальная фаза заболевания обычно сопровождается рестриктивными изменениями (уменьшением легочных объемов), снижением диффузионной способности легких по монооксиду углерода (DLco) и гипоксемией. Обструкция дыхательных путей при остром заболевании встречается редко, но может развиваться при хроническом варианте.
Бронхоальеволярный лаваж
Исследование трансформации лимфоцитов – это исследование сенсибилизации in vitro, которое дают наилучшие результаты при выявлении сенсибилизации к металлам. Для исследование можно использовать периферическую кровь, но лучше – промывные воды бронхоальвеолярного лаважа. В процессе исследования лимфоциты пациента подвергаются воздействию антигенов. Если лимфоциты трансформируются в бласты и пролиферируют, значит, они (и пациент) сенсибилизированы к данному антигену.
Биопсия легких
Хирургическая биопсия легких показанав случаях, когда неинвазивные испытания являются неокончательными. Данные исследований варьируют, но, как правило, включают в себя перибронхиолоцентричный лимфоцитарный альвеолит, плохо сформированные гранулемы без некротизации и организующуюся пневмонию. В хронических случаях может присутствовать интерстициальный фиброз.
Другие исследования
Другие методы исследования назначаются для получения дополнительной информации для постановки диагноза или для установления других причин интерстициального заболевания легких. Циркулирующие преципитины (специфичные преципитирующие антитела к антигену) указывают на воздействие, которое может быть причиной заболевания. Однако, наличие циркулирующих преципитинов не является ни чувствительным, ни специфическим. Выявление специфического преципитирующего антигена может требовать детализированного аэробиологического и/или микробиологического исследования рабочего места специалистами по промышленной гигиене, но обычно руководствуются известными источниками провоцирующих антигенов (например, наличие Bacillus subtilis на производстве детергентов).
Кожные пробы не имеют значения; эозинофилия отсутствует.
Прогноз
Патологические изменения при гиперсенситивном пневмоните полностью обратимы, если заболевание обнаружено на ранней стадии и устранено воздействие антигена. Острое заболевание разрешается самопроизвольно при удалении антигена; симптомы обычно уменьшаются в течение нескольких часов. Хроническое заболевание имеет менее благоприятный прогноз: развитие фиброза делает заболевание необратимым, хотя при прекращении контакта с повреждающим агентом наступает стабилизация.
Лечение
Лечение острого или подострого гиперчувствительного пневмонита проводится с применением кортикостероидов; обычно используется преднизон в дозе 60 мг перорально 1 раз в день в течение 1–2 недель, затем дозу постепенно снижают до 20 мг 1 раз в день в течение следующих 2–4 недель, далее производят снижение дозы на 2,5 мг/неделю до полной отмены препарата. Этот режим позволяет купировать начальные проявления заболевания, но не влияет на отдаленные результаты.
Лечение хронического гиперчувствительного пневмонита обычно проводят длительными курсами преднизона 30–40 мг перорально 1 раз в день с со снижением в зависимости от клинического ответа. Некоторым пациентам требуются кортикостероид-щадящие средства (например, микофенолата мофетил, азатиоприн) для длительного лечения.
Профилактика
Наиболее важным аспектом долгосрочного контроля гиперсенситивного пневмонита является предотвращение воздействия антигена. Однако полное изменение образа жизни и работы редко возможно в реальных условиях, особенно у фермеров и других рабочих; в этом случае применяются меры по снижению запыленности (например, предварительное увлажнение компоста перед работой с ним), использование воздушных фильтров и защитных масок. Фунгициды могут использоваться для предотвращения размножения микроорганизмов (например, в сене или сахарной свекле), но отдаленная безопасность этого подхода не доказана. Тщательная очистка увлажняющих систем вентиляции, удаление сырых ковров и поддержание низкой влажности также эффективны в некоторых случаях. Пациентам необходимо разъяснить, что эти меры могут не дать эффекта при продолжении контакта с антигеном.
Основные положения
Гиперсенситивный пневмонит является реакцией гиперчувствительности IV типа, которая может быть вызвана большим числом аллергенов.
У пациентов, подверженных риску, а также имеющих сравнимые симптомы, следует установить подробную историю производственного, любительского, и домашнего контакта.
Провести рентгеноскопическое исследование грудной клетки, КТ с высоким разрешением и исследования функции легких, а если диагноз неясен, возможно, бронхоальвеолярный лаваж и биопсию.
Лечение большинства пациентов преднизоном перорально.
Гиперсенситивный пневмонит: клиническая и радиологическая семиотика, лечение
Гиперсенситивный пневмонит (ГП) – заболевание, в основе которого лежит иммунологически индуцированное воспаление легочной паренхимы с вовлечением в патологический процесс стенок альвеол и бронхов вследствие неоднократного вдыхания разнообразных органических антигенов [1].

Основной причиной возникновения ГП служат бактериальные, грибковые, белковые антигены животного происхождения, антигены растительного происхождения и медикаментозные аллергены [4].
Чаще всего ГП развивается у тех, кто трудится в сельскохозяйственном секторе экономики (на птицеводческих фермах, в животноводческих комплексах, зерновых хозяйствах и др.), а также на предприятиях пищевой (производство пива, молочных продуктов, дрожжей, сыров и др.), текстильной и швейной (обработка меха, хлопка, льна), химической и фармацевтической (производство моющих средств, пластмасс, красителей, лекарственных препаратов), деревообрабатывающей (обработка древесины, производство бумаги) промышленности [5]. В последние годы наблюдается значительный рост заболеваемости ГП, что связано прежде всего с вдыханием бытовых аллергенов [4].
Основную роль в патогенезе ГП играют иммунокомплексные аллергические реакции, хотя возможны аллергические реакции другого типа (цитотоксического и замедленного) [6]. Циркулирующие иммунные комплексы и специфические антитела активизируют систему комплемента и альвеолярные макрофаги. Последние выделяют интерлейкин‑2, хемотаксические факторы, протеолитические ферменты, активные кислородные радикалы, способствуют росту фибробластов, продукции коллагена. В результате развивается альвеолобронхиолит, происходит фиброзирование интерстиция. При длительном или многократном поступлении в легкие антигена или вещества, обладающего адъювантным свойством, развивается аллергическая реакция замедленного типа, что приводит к образованию гранулем [7].
Различают острую, подострую и хроническую формы ГП.
Острая форма ГП
Патоморфологическим субстратом острой формы ГП является альвеолит, часто в сочетании с бронхиолитом. Отек и инфильтрация альвеол, межальвеолярных перегородок, стенок бронхиол лимфоцитами, плазматическими клетками, нейтрофилами, гистиоцитами характерны для острой формы ГП.
Клинические проявления острой формы ГП развиваются, как правило, через 4-12 ч после попадания антигена в легкие. Характерными симптомами болезни являются озноб, повышение температуры тела, одышка, кашель (сухой или со скудной слизистой мокротой), общая слабость, боль в груди, мышцах, суставах, головная боль. Наряду с этим у некоторых больных могут возникать приступы затрудненного дыхания, явления вазомоторного ринита.
В период острой фазы болезни при аускультации определяется крепитация, нередко над всей поверхностью легких. При наличии явлений бронхоспазма прослушиваются сухие свистящие хрипы.
В случаях прекращения контакта с антигеном перечисленные симптомы могут исчезать без лечения в течение сравнительно короткого времени (12-48 ч). Если же контакт с причинным агентом продолжается, острая форма болезни принимает прогрессирующее течение и прогноз заболевания становится значительно более серьезным.
В клиническом анализе крови у больных острой формой ГП часто присутствуют лейкоцитоз, сдвиг влево лейкоцитарной формулы, увеличение скорости оседания эритроцитов. У некоторых пациентов может определяться умеренная эозинофилия. Указанные изменения неспецифичны и должны учитываться в первую очередь для оценки активности и тяжести патологического процесса [4].
При рентгенографии органов грудной полости обычно определяется диффузное снижение прозрачности по типу матового стекла, иногда с усилением легочного рисунка. Часто имеют место явления легочной диссеминации.
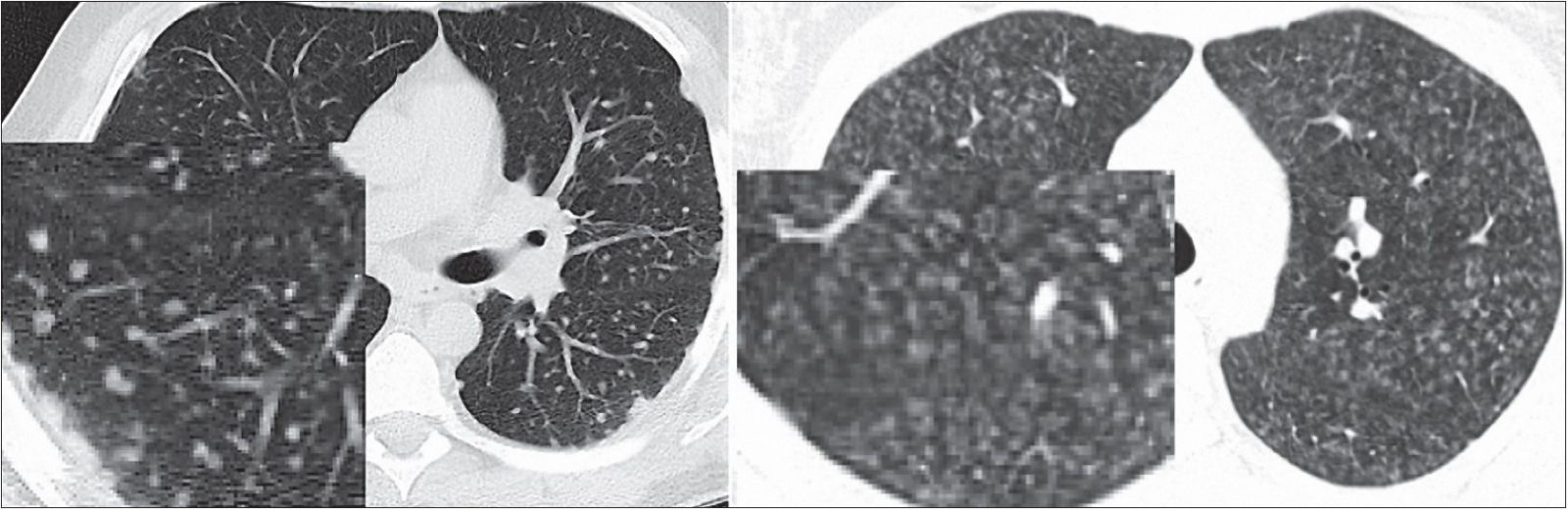
Наиболее точно признаки альвеолита идентифицируются методом компьютерной томографии (КТ) высокого разрешения. КТ-паттерн альвеолита представлен узелками (nodules), расположенными плотно друг к другу и занимающими практически всю площадь среза. В отличие от узелков, расположенных в интерстиции бронхососудистых пучков, междольковых перегородок (саркоидоз и другие гранулематозные заболевания), имеющих плотную структуру и четкие очертания (sharp nodules), узелки, обусловленные отеком и инфильтрацией альвеол, имеют малоинтенсивную плотность и размытые границы (blurry nodules) – рисунок 1.
Рис. 1. Слева – КТ больного М., 38 лет, саркоидоз легких: узелки, расположенные в интерстиции; справа – КТ больного И., 31 года, альвеолит как проявление ГП: узелки, локализованные в альвеолярных пространствах
При распространении отека со стенок альвеол на септальный интерстиций (перегородки между ацинусами и вторичными легочными дольками) узелковый паттерн трансформируется в диффузное снижение прозрачности паренхимы по типу матового стекла (рис. 2).
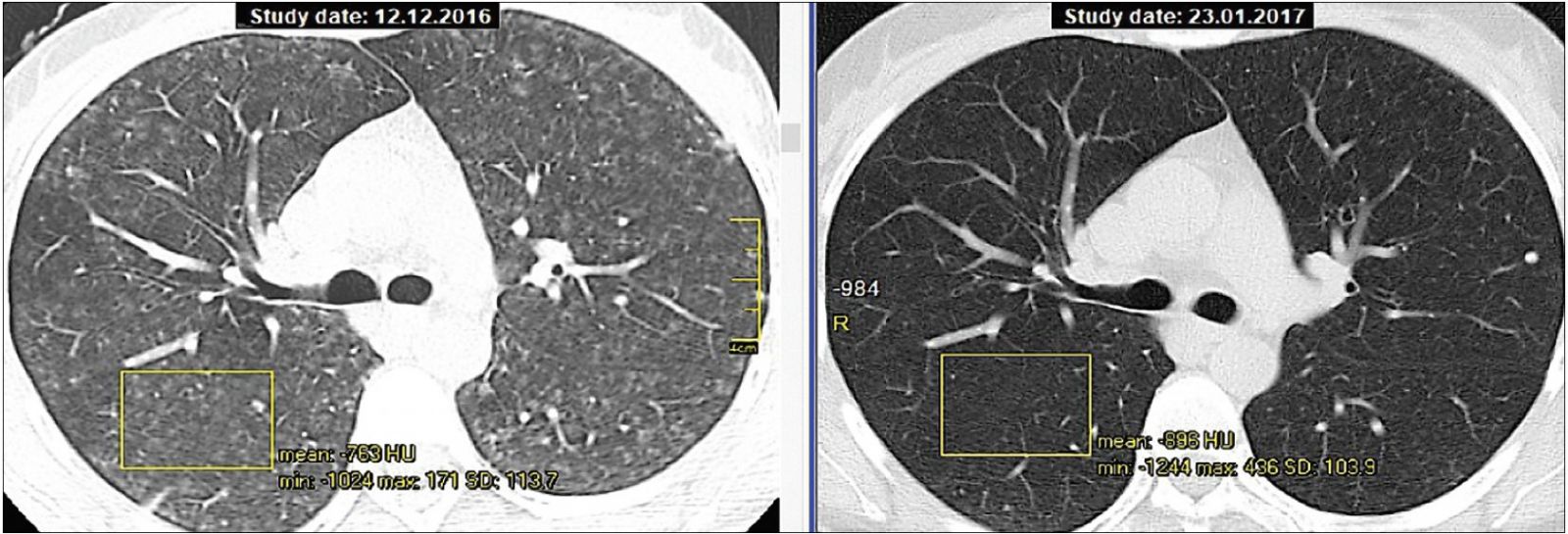
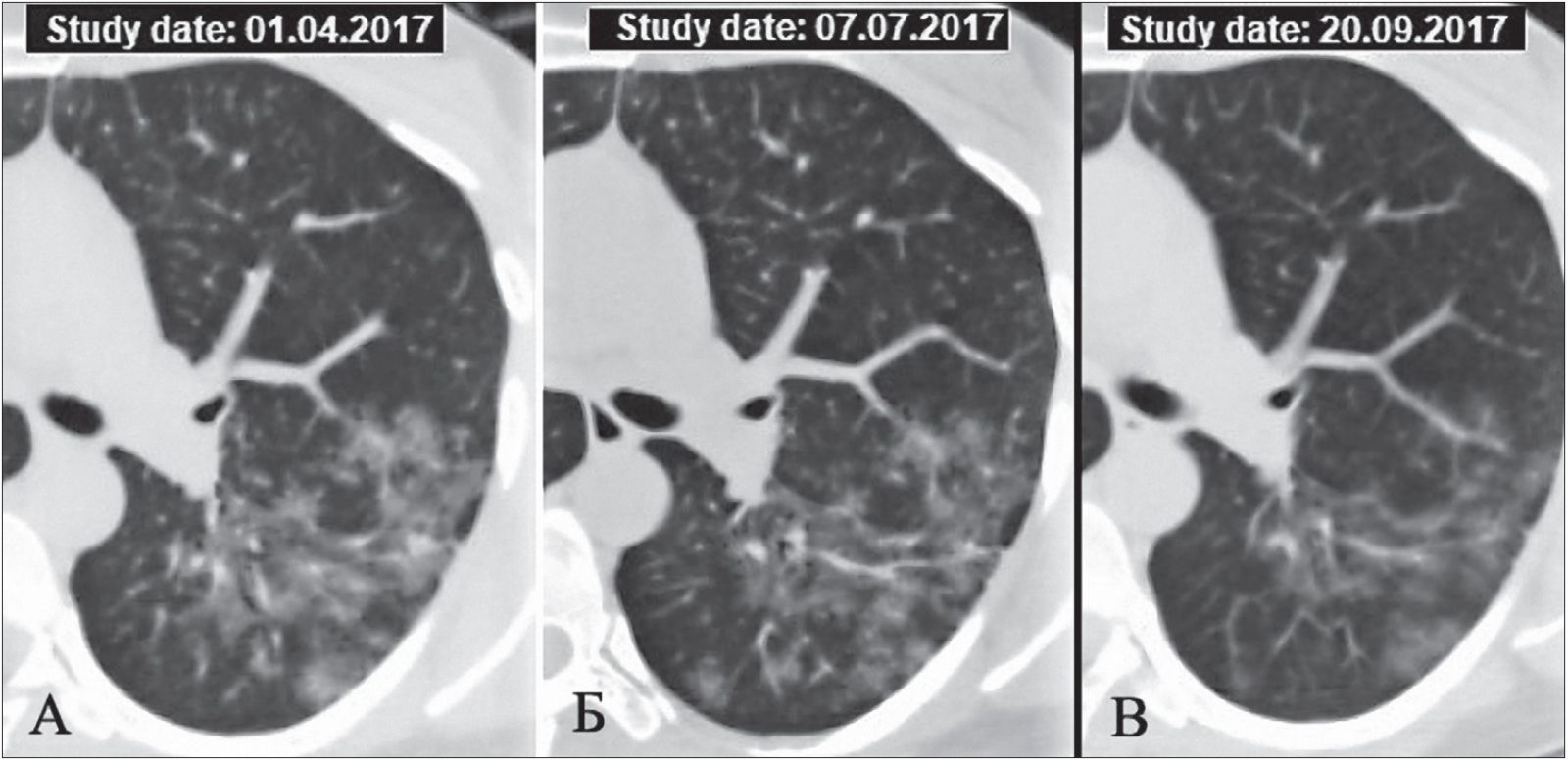
Острая форма ГП обычно хорошо поддается лечению глюкокортикостероидами (ГКС). На рисунке 3 продемонстрирована динамика КТ-данных после проведения ГКС-терапии в течение 1 месяца.
Детальный опрос больного в большинстве случаев позволяет установить источник аллергена, а последующее аллергологическое обследование – провести его идентификацию.

Подострая форма ГП
При воздействии на организм небольших доз антигена далеко не всегда удается выявить четкую временную взаимосвязь между поступлением антигена в организм и клиническими проявлениями болезни. В таких случаях начало болезни имеет слабо выраженный характер, и больные далеко не всегда обращаются к врачу своевременно. Постепенное развитие признаков болезни затрудняет (как для врача, так и для больного) выявление связи между симптомами и воздействием какого-либо конкретного профессионального или бытового фактора. В этих случаях речь идет о подострой форме заболевания.
Патоморфологической основой подострой формы ГП является образование эпителиоидноклеточных неказеозных гранулем саркоидного типа.
Клиническая картина подострой формы ГП характеризуется одышкой при умеренной физической нагрузке, кашлем с небольшим количеством слизистой мокроты, субфебрильной температурой тела, повышенной утомляемостью, снижением апатита, потерей веса.
В диагностике ГП определенное значение придается выявлению специфических преципитинов (преципитирующих антител), относящихся к классу иммуноглобулинов G [9]. Однако следует отметить, что выявление преципитирующих антител у лиц, контактирующих с определенным антигеном, не имеет самостоятельного значения. Обнаружение преципитинов в первую очередь свидетельствует о контакте с соответствующим антигеном и наличии к нему гиперчувствительности. Так, например, у фермеров, не имеющих признаков ГП, в 10-50% случаев выявляются специфические антитела [10].
Полезная информация может быть получена при исследовании жидкости бронхоальвеолярного лаважа. Изменения клеточного состава лаважной жидкости характеризуются увеличением общего числа клеток и процентного содержания лимфоцитов (от 20-30 до 70-90% общего клеточного состава) [11].
Ряд исследователей предлагают применять для диагностики ГП ингаляционный провокационный тест [12]. Он оценивается как положительный в случаях, если после вдыхания аэрозолей, содержащих предполагаемые антигены, субъективное состояние больного ухудшается (оценивается больным как гриппоподобное), повышается температура тела, частота дыхания, уменьшается жизненная емкость легких, снижается их диффузионная способность. Проведение провокационных ингаляционных тестов в острой стадии наиболее информативно, однако сопряжено с ухудшением состояния больного, менее информативно – в подострой, практически бесполезно – в хронической стадии болезни. Кожные тесты не получили широкого распространения из-за высокого процента отрицательных результатов при наличии развернутой клинической картины болезни [13].
Таким образом, несмотря на наличие лабораторных тестов, диагноз ГП остается клиническим. Самое главное в диагностике ГП – помнить о возможности его развития, проводить детальный анализ производственных факторов, бытовых условий, географических и климатических особенностей местности проживания больного и использовать метод исключения альтернативных диагнозов.
Изменения на КТ у больных подострой формой ГП кардинально отличаются от КТ-паттерна острой формы [14, 15]. Эпителиоидноклеточные гранулемы, диффузно локализованные в субплевральном интерстиции, расположенном под висцеральной плеврой, и в интерстиции междольковых перегородок, обусловливают образование участков матового стекла с довольно четкими границами (рис. 4).

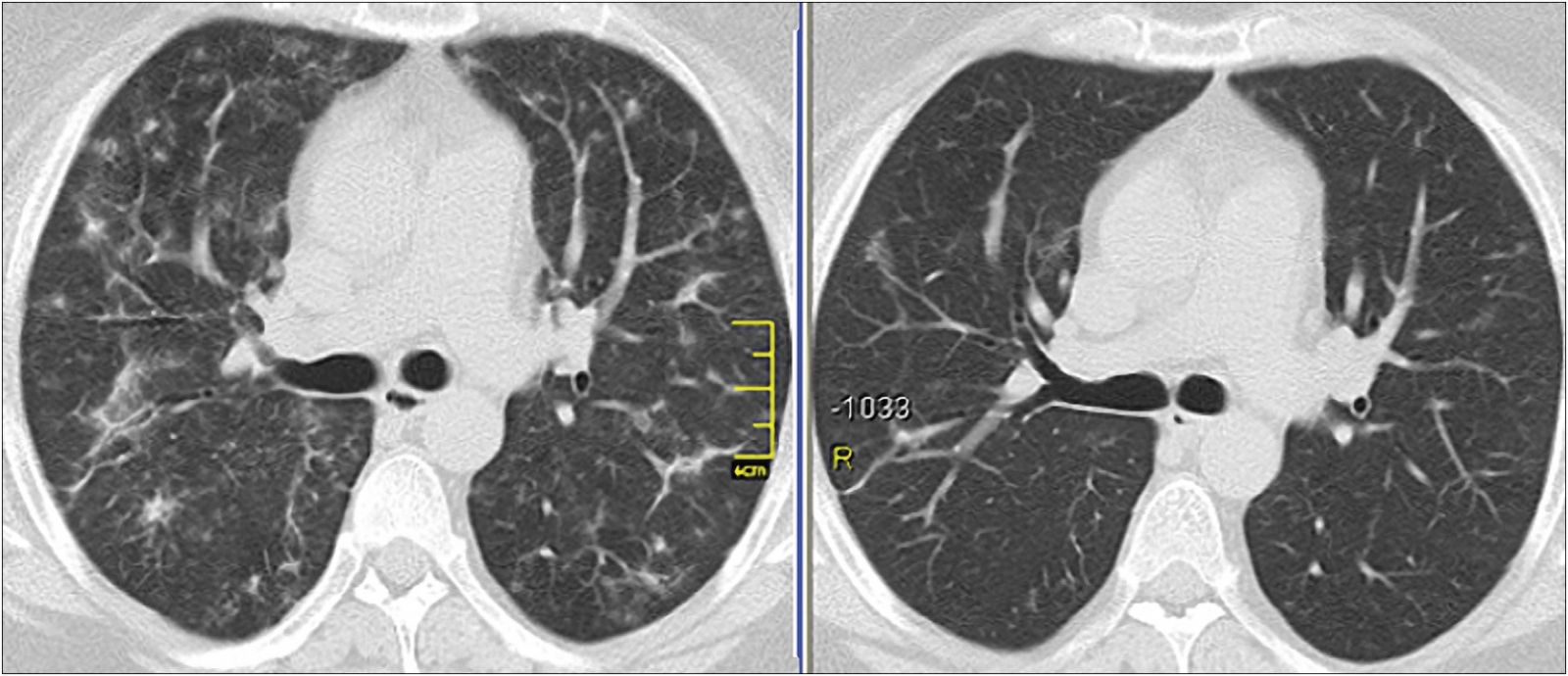
Часто гранулемы сливаются в конгломераты, образуя узелки различной величины и уплотнения вдоль бронхососудистых пучков (рис. 5).
У пациентов с подострой формой ГП часто наблюдается увеличение бронхопульмональных лимфатических узлов, однако, в отличие от лимфаденопатии при саркоидозе, размеры прикорневых узлов по короткой оси редко превышают 15 мм.
ГКС-терапия больных подострой формой ГП, как правило, эффективна, вместе с тем сроки разрешения процесса могут варьировать в широких пределах – от нескольких недель (рис. 4) до нескольких месяцев (рис. 5).
Необходимо отметить, что, в отличие от острой формы ГП, при которой в значительной части случаев удается определить связь развития симптомов с ингаляцией аллергена, диагностика подострой формы часто затруднена.
Клиническая семиотика (одышка, непродуктивный кашель, субфебрильная температура тела) у больных подострой формой ГП имеет неспецифический характер и может рассматриваться только по критерию совместимости с диагнозом.
Достаточно специфичным для ГП является КТ-паттерн патологических изменений в паренхиме – множественные участки снижения прозрачности по типу матового стекла, распределенные в различных зонах легких. Этот паттерн существенно отличается от характера КТ-изменений при идиопатических интерстициальных пневмониях, но он также характерен и для токсических, прежде всего лекарственно-индуцированных, пневмонитов – такой диагноз всегда должен рассматриваться в качестве альтернативного.
Таким образом, в случаях неустановленной связи развития клинических симптомов с ингаляцией какого-либо аллергена диагностика ГП должна основываться на характерных КТ-признаках, исключении альтернативных диагнозов при наличии совместимой клинической семиотики.
Рис. 5. КТ больной О., 54 лет, ГП, подострая форма; слева – до лечения: участки снижения прозрачности паренхимы по типу матового стекла в сочетании с узелками и уплотнениями вдоль бронхососудистых пучков; справа – спустя 6 мес после проведения терапии МП: разрешение процесса
Хроническая форма ГП
При продолжении контакта с аллергеном и отсутствии специфической терапии с течением времени в легких начинают преобладать пролиферативные процессы, гранулемы трансформируются в соединительнотканные структуры. Морфологическая картина хронической стадии ГП полностью теряет черты своей относительной специфичности. В связи с этим отсутствие гранулем в биопсийном материале не исключает диагноз ГП [16].
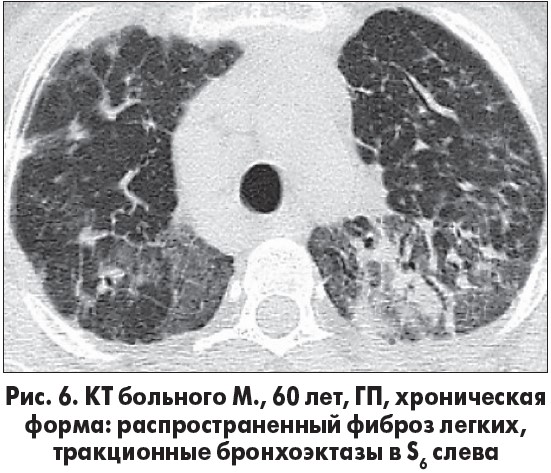
В клинической картине доминируют симптомы респираторной недостаточности, а на КТ – признаки распространенного фиброза легких (рис. 6).
Установить, предположительно, ГП в качестве причины фиброза легких можно лишь на основании данных профессионального анамнеза – длительный стаж работы в контакте с органическими аллергенами. Поскольку в этих случаях невозможно исключить наличие активного гранулематозного процесса в легких, пациенту целесообразно назначить пробную ГКС-терапию с оценкой эффективности на основании клинических и функциональных данных, прежде всего динамики показателя диффузионной способности легких. Вместе с тем необходимо отметить, что пациенты с хронической формой ГП, как правило, относятся к старшей возрастной группе и помимо респираторной недостаточности имеют сопутствующие заболевания, ограничивающие возможности применения ГКС. В связи с этим решение о назначении ГКС-терапии следует принимать после тщательного анализа соотношения «польза-риск».
Лечение
ГКС являются препаратами выбора в лечении больных ГП [4, 13]. При острой форме заболевания рекомендуется применение ступенчатой терапии: дексаметазон внутривенно (по 8-16 мг в сутки в зависимости от тяжести течения) на протяжении 7-10 дней с последующим приемом МП перорально в дозе 0,2-0,4 мг/кг/сут с учетом степени тяжести альвеолита. Дексаметазон в среднем в 5 раз превосходит МП по степени противовоспалительной активности, в связи с этим его применение обеспечивает максимальный противовоспалительный эффект на старте терапии. Дозу МП сохраняют неизменной в течение 4 нед, после этого ГКС-терапию продолжают в режиме снижения дозы на 2 мг/нед до полной отмены.
При подострой форме ГП лечение начинают с приема таблетированного МП в дозе 0,4 мг/кг/сут в течение 4 нед, затем – в режиме снижения дозы такими темпами, чтобы к концу 3-го мес она составила 0,2 мг/кг/сут. После этого проводят контрольное КТ-исследование, при наличии положительной динамики лечение продолжают в режиме постепенного снижения дозы до 0,1 мг/кг/сут к концу 6-го месяца. Основанием для отмены ГКС-терапии является разрешение процесса.
У некоторых пациентов с подострой формой ГП наблюдается резистентность к ГКС-терапии, которая довольно часто отмечается и при других гранулематозных заболеваниях. По нашим данным, у больных саркоидозом легких резистентность к ГКС-терапии встречается в 17% случаев.
Резистентность к ГКС-терапии дифференцируют на абсолютную и относительную. Случаи абсолютной резистентности регистрируются у больных с признаками прогрессирования или стабилизации процесса через 3 мес лечения МП в стартовой дозе 0,4 мг/кг/сут в течение 1-го мес с последующим снижением дозы до 0,2 мг/кг/сут к концу 3-го месяца. То есть абсолютная резистентность означает отсутствие какого-либо положительного эффекта от использования адекватной дозы препаратов и режима терапии. Относительная резистентность к ГКС-терапии констатируется в случаях прогрессирования или стабилизации процесса при снижении дозы МП с 0,2 мг/кг/сут до поддерживающей (0,1 мг/кг/сут) в период с 4-го до 6-го мес при наличии признаков регрессии на этапах стартовой терапии на фоне использования первоначально более высоких доз МП.
Абсолютная резистентность служит основанием для отмены ГКС и назначения метотрексата в дозе 15 мг/нед. В случаях относительной резистентности проводится комбинированное лечение ГКС и метотрексатом – необходимо вернуться к дозе МП, равной 0,2 мг/кг/сут, и добавить метотрексат по 10 мг/нед. Лечение метотрексатом требует мониторинга количества лейкоцитов, тромбоцитов и содержания аланинаминотрансферазы в периферической крови (через 2 нед после начала терапии, далее – 1 раз в 3-4 нед).
Рисунок 7 демонстрирует положительный эффект комбинированной терапии после безуспешного лечения МП при снижении его дозы до поддерживающей.
Рис. 7. КТ левого легкого больной Р., 38 лет, ГП, подострая форма:
А. Визит 2 – спустя 3 мес после назначения МП в стартовой дозе 24 мг/сут с последующим снижением; пациентка принимает МП по 12 мг/сут, назначено продолжение ГКС-терапии в режиме снижения дозы до 6 мг/сут к концу 6-го мес;
Б. Визит 3 – спустя 6 мес после начала лечения; доза МП – 6 мг/сут: существенной динамики КТ-данных не наблюдается, назначен метотрексат по 10 мг/нед, доза МП увеличена до 12 мг/сут;
В. Визит 4 – после 3-месячной комбинированной терапии: площадь участков матового стекла и узелковая диссеминация уменьшились
В заключение следует отметить, что случаи резистентности к ГКС-терапии у пациентов с подострой формой ГП все же достаточно редки, у большинства больных своевременное лечение ГКС позволяет достичь разрешения процесса с восстановлением вентиляционной функции и диффузионной способности легких.
Литература
1. Costabel U. Chronic hypersensitivity pneumonitis // Clin Chest Med. – 2012. – Vol. 33. – P. 151-163.
2. Campbell J.A. Acute symptoms following work with hay // BMJ. – 1932. – Vol. 2. – P. 1143-1144.
3. Pepys J. Hypersensitivity to inhaled organic antigens // J. Roy. Coll. Physicans. – 1967. – Vol. 2. – P. 42-51.
4. Spagnolo P., Rossi G., Bonifazi M. et al. Hypersensitivity pneumonitis: a comprehensive review // J.Investig. Allergol. Clin. Immunol. – 2015. – Vol. 25 (4). – P. 237-250.
5. Glazer C.S. Chronic hypersensitivity pneumonitis: important considerations in the work-up of this fibrotic lung disease // Curr. Opin. Pulm. Med. – 2015. – Vol. 21. – P. 171-177.
6. Selman M., Pardo A., King T.E. Hypersensitivity pneumonitis: insights in diagnosis and pathobiology // Am. J. Respir. Crit. Care Med. – 2012. – Vol. 186. – P. 314-324.
7. Selman M., Buendia-Roldan I. Immunopathology, diagnosis, and management of hypersensitivity pneumonitis // Semin. Respir. Crit. Care Med. – 2012. – Vol. 33. – P. 543-554.
8. Castonguay M.C., Ryu G.H., Yi E. et al. Granulomas and giant cells in hypersensitivity pneumonitis // Hum. Pathol. – 2015. – Vol. 46. – P. 607-613.
9. Fenoglio C.M., Reboux G., Sudre B. et al. Diagnostic value of serum precipitins to mould antigens in active hypersensitivity pneumonitis // Eur. Respir. J. – 2007. – Vol. 29. – P. 706-712.
10. Cormier Y., Belanger J., Durand P. Factors influencing the development of serum precipitins to farmer’s lung antigen in Quebec dairy farmers // Thorax. – 1985. – Vol. 40. – P. 138-142.
11. Reynolds H.Y. Present status of bronchoalveolar lavage in interstitial lung disease // Curr. Opin. Pulm. Med. – 2009. – Vol. 15. – P. 479-485.
12. Ohtani Y., Kojima K., Sumi Y. et al. Inhalation provocation tests in chronic bird fancier’s lung. // Chest. – 2012. – Vol. 118. – P. 1382-1389.
13. Selman M., Schwartz M.I., King T.E.. Hypersensitivity pneumonitis // Interstitial lung disease. Shelton (CT): People’s Medical Publishing House-USA. – 2011. – P. 597-635.
14. Clazer C.S., Rose C.S., Lynch D.A. Clinical and radiologic manifestations of hypersensitivity pneumonitis // Thorac Imaging. – 2002. – Vol. 17. – P. 261-272.
15. Patel R.A., Sellami D., Gotway M.B. et al. Hypersensitivity pneumonitis: patterns on high resolution CT // J. Comp. Assist.Tomogr. – 2000. – Vol. 24. – P. 265-270.
16. Churg A., Muller N., Flint J. et al. Chronic hypersensitivity pneumonitis // Am. J. Surg. Pathol. – 2006. – Vol. 30. – P. 201-208.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (42), лютий 2018 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Вушні сіркові корки (ВСК) (рис. 1, 2) протягом життя з’являються в ≈5% дорослих, 10% дітей та ⅓ осіб похилого віку, а також у хворих з когнітивними розладами (Roeser R.J., Ballachanda B.B., 1997; Sevy J.O., Singh A., 2020); вони спричиняють такі симптоми, як погіршення слуху, шум і біль у вусі, запаморочення, кашель, а також суттєво погіршують якість життя (Horton G.A. et al., 2020; Michaudet X., Malaty J., 2018; Schwartz S.R. et al., 2017; Harkin H., 2019).
Гострі респіраторні вірусні інфекції (ГРВІ) посідають перше місце за поширеністю серед усіх інфекційних захворювань. При цьому патологічний процес локалізується переважно у верхніх відділах дихальних шляхів, зокрема в носоглотці. Одним із проявів ГРВІ є назофарингіт – запалення слизової оболонки та лімфоїдної тканини носоглотки, що проявляється симптомами утрудненого дихання й закладеності носа.
У вересні під егідою Асоціації алергологів України й Асоціації з інтенсивного лікування інфекційних захворювань (INCURE), за підтримки журналу «Астма та алергія» відбувся телеміст «Респіраторні захворювання лікуй респіраторно: чи все так однозначно, як здається?». У заході взяли участь провідні пульмонологи, оториноларингологи, інфекціоністи й інші спеціалісти.