генерализованная вирусная инфекция что это такое
Вирус Эпштейна-Барра
Что такое вирус Эпштейна-Барра?
Вирус Эпштейна-Барра — это человеческий герпес-вирус 4-го типа, который считается главным виновником развития инфекционного мононуклеоза и опухолей, в частности лимфомы Беркитта. Это самый распространенный на планете вирус, носительство достигает 95% среди населения Земного шара.
Описание заболевания
При любом ослаблении иммунитета или воздействии вредных факторов вирус становится причиной таких заболеваний:
Симптомы вируса Эпштейна-Барра
Классическое проявление поражения вирусом Эпштейна-Барра — инфекционный мононуклеоз. У маленьких детей заболевание никак не проявляется, а вот у детей старшего возраста и взрослых развивается характерная клиническая картина.
Период от заражения до клинических проявлений или инкубация длится месяц-полтора. Далее появляется триада симптомов: лихорадка, воспаление горла и увеличение лимфатических узлов. Температура тела высоко поднимается вечером, а днем нормальная, и такая ситуация продолжается около 3-х недель. Воспаление горла (фарингит) протекает тяжело, с сильной болью. Поражаются шейные лимфатические узлы, как правило, симметрично, но может быть увеличение лимфоузлов по всему телу.
С течением времени присоединяется увеличение печени и селезенки, изменяется состав крови.
В течение месяца или немногим более клиническая картина угасает, заболевание заканчивается полным клиническим выздоровлением, однако вирус остается в организме навсегда.
Редко бывают осложнения: неврологические симптомы в виде энцефалита или менингита, разрыв селезенки, сужение дыхательных путей.
Другие проявления инфицирования в виде опухолей, рассеянного склероза или синдрома хронической усталости протекают по своим законам. Связь заболевания с вирусом обнаруживается только при углубленном целенаправленном обследовании.
Причины вируса Эпштейна-Барра
Любой вирус — это внутриклеточный паразит, который не может существовать вне человеческого тела. Проникает вирус через слизистые оболочки ротоглотки и верхних дыхательных путей. Момент заражения установить невозможно, поскольку никаких клинических проявлений нет. Недомогание бывает только у крайне ослабленных больных. Вирус попадает в кровь и лимфу, постоянно находится в нервной ткани.
Паразитирование вируса провоцирует ускоренное деление клеток, которые становятся источником опухолей различной локализации. Азиаты, зараженные вирусом, болеют раком носоглотки, жители Африки — опухолями яичников и почек, европейцы переносят вторжение вируса преимущественно как тяжелую ОРВИ.
При других заболеваниях, перечисленных выше, вирус обнаруживается почти всегда, но продолжаются дискуссии о его роли в формировании данных болезней.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
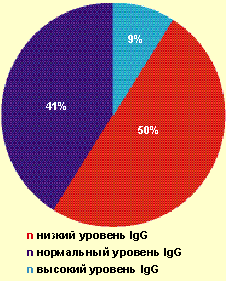 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
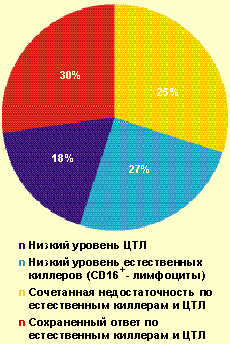 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Вирусная инфекция
Содержание статьи:
Вирус – это крошечный агент, который живет внутри живых клеток или клеток-хозяев. Вирусы нуждаются в живых клетках, чтобы иметь возможность воспроизводиться. Существуют тысячи вирусных инфекций человека, некоторые из которых встречаются чаще, чем другие. Например, простуда и грипп – это вирусы, но встречаются они чаще, чем Эбола и ВИЧ. Обычно инфекции вирусного характера у взрослых протекают нетяжело у относительно здоровых людей, но могут быть довольно тяжелыми для людей с ослабленной иммунной системой. Практически любой вирус может привести к осложнениям, присоединению микробной инфекции.
Основные вирусные инфекции
Вирусной инфекцией является заболевание, которое возникает при проникновении в тело патогенных вирусных частиц. Вирусы «захватывают» нормальные живые клетки тела. Они используют эти клетки для репликации и размножения, в конечном итоге разрушая клетку-хозяина – это то, что вызывает признаки заболевания вирусной инфекцией. Важно понимать различия вирусной и бактериальной инфекции. В отличие от бактериальных инфекций, которые поддаются лечению антибиотиками, вирусные инфекции не так просто лечить. Многие, такие как ОРВИ, проходят своим чередом, и тело восстанавливается самостоятельно, а другие, например ВИЧ, – нет.
Вирусные заболевания – это чрезвычайно распространенные инфекции. Есть много типов возбудителей, вызывающих самые разные вирусные заболевания. Самый распространенный тип вирусного заболевания – простуда, вызванная вирусной инфекцией верхних дыхательных путей (носа и горла). Другие распространенные вирусные заболевания:
Для вирусных инфекций характерна высокая заразность, они передаются от человека к человеку, когда вирус проникает в организм и начинает размножаться. Источником является больной человек (животное) или носители. Распространенные пути и механизмы передачи вирусов от человека к человеку включают:
Вирусные заболевания в своем развитии и течении имеют определенные отличия, вызывают широкий спектр симптомов, которые различаются по характеру и степени тяжести в зависимости от конкретной причины вирусной инфекции и других факторов, включая возраст человека и общее состояние здоровья.
Вирусная инфекция: основные симптомы заболевания
Симптомы вирусных заболеваний различаются в зависимости от конкретного типа, характеристики вируса, вызывающего инфекцию, пораженной области тела, возраста, истории болезни пациента и других факторов, изначального состояния при вирусной инфекции. Симптомы вирусных заболеваний могут затронуть практически любую область тела или систему организма. Они могут включать:
У младенцев картина вирусной инфекции также может включать:
Серьезные признаки, которые могут указывать на опасные для жизни осложнения
В некоторых случаях нужно строго контролировать то, как проявляется инфекция. Немедленно нужно обратиться за медицинской помощью, если наблюдаются какие-либо из следующих симптомов:
Методы диагностики
Большинство ОРВИ и грипп в эпидемический сезон диагностируют клинически, учитывая особенности симптомов, тяжесть заболевания и сроки развития болезни (инкубационный период). В зависимости от того, сколько длится период инкубации – от момента контакта с больным, до первых признаков болезни, можно уточнить тип ОРВИ.
Лечение вирусной инфекции у взрослых
Терапия вирусных инфекций зависит от конкретного вируса и других факторов. Общие лечебные меры направлены на облегчение симптомов, чтобы человек мог отдохнуть, поддержать свои силы и выздороветь без развития осложнений. Чем лечить инфекции, определяет врач.
Общие препараты для лечения и немедикаментозные методы вирусных инфекций включают:
Важно знать, что антибиотики при вирусной инфекции не показаны, они применимы только при развитии или угрозе присоединения микробных осложнений.
В зависимости от типа вирусной инфекции и наличия осложнений может потребоваться широкий спектр других методов лечения. Например, инфекцию, вызванную вирусом папилломы человека (ВПЧ), которая приводит к дисплазии шейки матки, можно лечить путем хирургического удаления аномальных клеток на шейке матки женщины.
В некоторых случаях для лечения вирусных заболеваний могут быть назначены определенные лекарства:
Возможные осложнения после вирусных инфекций
Меры профилактики и защиты
Вирусы распространяются по-разному, в зависимости от их классификации и особенностей. Гепатит С, заболевание печени, передается через биологические жидкости. С другой стороны, грипп может передаваться при контакте с вирусом, оставленным на каком-либо объекте, например телефоне, или через капли в воздухе, если больной гриппом чихает или кашляет перед вами. Не все вирусные инфекции можно предотвратить, но можно снизить риск заражения вирусом несколькими способами:
Источники статьи:
Вирус Эппштейн-Барр: лечить или не лечить?
О вирусе Эппштейн-Барр слышали немногие, но к 40 годам его носителями становятся до 97% людей.
Кому-то повезет, и такое «соседство» пройдет незамеченным, а у иных оно может обернуться синдромом хронической усталости или даже злокачественным заболеванием крови.
Прививок от ВЭБ пока не придумали, лечить его по большому счету особо нечем. Однако в ряде случаев диагностику на него считают жизненно необходимой — иначе лечение пойдет не по тому пути и может серьезно навредить пациенту.
ВЭБ — причина хронической персистирующей инфекции из группы герпесвирусных возбудителей (вирус герпеса 4-го типа).
Источником заражения ВЭБ является больной человек или вирусоноситель.
Передача вируса может происходить:
ВЭБ может наблюдаться в любом возрасте, но особенно у детей и молодых.
Клинические проявления инфекции крайне разнообразны, что затрудняет диагностику. Как правило, проявления ВЭБ развиваются на фоне снижения иммунитета, что свойственно всем герпесвирусным инфекциям.
Первичные формы заболевания и его рецидивы всегда связаны с врожденным или приобретенным иммунодефицитом. У людей с выраженным иммунодефицитом наблюдаются генерализованные формы инфекции с поражением центральной нервной системы, печени, легких и почек.
В настоящее время установлено, что ВЭБ также ассоциирован с целым рядом онкологических, преимущественно лимфопролиферативных и аутоиммунных заболеваний (классические ревматические болезни, васкулиты, неспецифический язвенный колит и др.). Кроме того, ВЭБ вызывает манифестные и стертые формы заболевания, протекающие по типу острого и хронического мононуклеоза.
У людей с нормальным иммунитетом после заражения ВЭБ возможны два варианта.
Инфекция может протекать бессимптомно либо проявляться в виде незначительных признаков, напоминающих грипп или ОРВИ. Однако в случае заражения на фоне уже имеющегося иммунодефицита у пациента может развиться картина инфекционного мононуклеоза.
В случае развития острой инфекции возможны несколько вариантов исхода заболевания:
1. выздоровление (выявляется ДНК вируса в единичных клетках);
2. бессимптомное вирусоносительство или латентная инфекция (вирус определяется в слюне или лимфоцитах лабораторно);
3. развитие хронического рецидивирующего процесса:
Исход острой инфекции, вызванной ВЭБ, зависит от наличия и степени выраженности иммунного дефицита, а также от наличия ряда внешних факторов (стрессы, сопутствующие инфекции, операционные вмешательства, гиперинсоляция, переохлаждения и др.), способных нарушать работу иммунной системы.
XXI век — век герпетических инфекций. И это действительно так. Мы стали неожиданно уязвимыми к вирусам, которые еще пару сотен лет назад не представляли для нас никакой угрозы. Сегодня нет ни чумы, ни холеры, ни оспы — зато есть герпетические инфекции, и это большая проблема.
Клинические проявления заболеваний, вызванных ВЭБ, зависят от остроты процесса.
Также имеет значение первичность инфекционного процесса или возникновение клинической симптоматики хронической инфекции.
В случае развития острого инфекционного процесса при заражении ВЭБ наблюдается картина инфекционного мононуклеоза.
Развитие данного заболевания приводит к появлению следующих клинических признаков:
В случае развития хронически активной ВЭБ-инфекция наблюдается длительное рецидивирующее течение заболевания.
Обычно эта симптоматика имеет волнообразный характер.
У пациентов с иммунной недостаточностью возможно:
Генерализованные формы ВЭБ-инфекции могут привести к летальному исходу.
Учитывая то, что клинически диагноз «ВЭБ-инфекция» выставить невозможно, ведущим в определении заболевания являются методы лабораторной диагностики.
Их можно разделить на две группы:
К скрининговым можно отнести те, которые наряду с клинической симптоматикой позволяют заподозрить ВЭБ-инфекцию.
В клиническом анализе крови могут наблюдаться: незначительный лейкоцитоз, лимфомоноцитоз, возможно, тромбоцитопения.
В биохимическом анализе крови выявляются: повышение уровня трансаминаз и других ферментов, белков острой фазы — С-реактивный белок, фибриноген и др.
Однако эти изменения не являются строго специфичными для ВЭБ-инфекции (их можно обнаружить и при других вирусных инфекциях).
Важным исследованием, позволяющим установить наличие возбудителя в организме, является серологическое обследование: повышение титров антител к ВЭБ, является критерием наличия инфекционного процесса в настоящее время или свидетельством контакта с инфекцией в прошлом.
Однако наличие антител не позволяет однозначно говорить о том, что клинические проявления заболевания вызваны ВЭБ.
Для получения наиболее достоверных результатов используется ДНК-диагностика.
С помощью метода полимеразной цепной реакции (ПЦР) определение ДНК ВЭБ проводят в различных биологических материалах: слюне, сыворотке крови, лейкоцитах и лимфоцитах периферической крови.
При необходимости проводят исследование в биоптатах печени, лимфоузлов, слизистой кишечника и т.д.
Таким образом, для постановки диагноза ВЭБ-инфекции, помимо проведения общеклинических обследований, необходимы серологические исследования (ИФА) и ДНК диагностика инфекции в различных материалах в динамике.
Лечение ВЭБ инфекции
Во-первых, я бы советовала не заниматься самолечением.
Во-вторых, найти врача, которому Вы можете доверить здоровье своего ребенка и Ваше (педиатр, аллерголог-иммунолог, гематолог, инфекционист и т.д. желательно с опытом ведения таких пациентов).
В-третьих, не паниковать, т.к. обнаружение ВЭБ инфекции у человека не означает, что его необходимо немедленно лечить, спасать.
В настоящее время общепринятых схем лечения ВЭБ-инфекции не существует.
Объем терапии больных, как с острой, так и с хронической активной ВЭБ-инфекцией различный, в зависимости от длительности заболевания, тяжести состояния и иммунных расстройств.
В комплексном лечении используются различные группы препаратов:
Еще важно осознать некоторые закономерности:
1. Иммунная система получает все необходимое для своей работы из продуктов питания, которые мы потребляем.
2. Обязательно для иммунной системы нужны: витамины и микроэлементы, омега-3, витамин Д.
3. Необходимо, чтобы ребенок соблюдал режим дня (высыпался, не просиживал часами за компьютером и др. гаджетами, прогулки на свежем воздухе, физическая деятельность).
